습윤황산공정
Wet sulfuric acid process습식 황산 공정(WSA 공정)은 오늘날 시판되고 있는 주요 기체 탈황 공정 중 하나이다. 덴마크 촉매기업 할도르 탑쇠가 1980년대 후반 이 기술을 도입해 특허를 낸 이후 고압증기를 동시 생산하면서 상업용 품질의 황산(HSO24) 형태로 각종 공정가스에서 황을 회수하는 효율적인 공정으로 인정받고 있다. WSA 과정은 황 제거가 이슈가 되는 모든 산업에 적용된다.
습식 카탈루션 프로세스는 다음과 같은 스트림을 포함하는 황을 처리하는 데 특히 적합하다.[1]
- 아민 가스 처리 장치 등의 HS2 가스
- Sourwater Stripper(SWS) 가스의 오프 가스
- Corpisol에서 가스 배출
- 알킬화 유닛의 사용후 산
- 클로스 공정 꼬리 가스
- 무거운 잔류물 또는 펫코크 연소식 보일러 오프 가스
- SNOX 연도 가스 탈황 다양한 공정에서 발생하는 보일러 연도 가스
- 금속공정가스
- 황산생산
프로세스
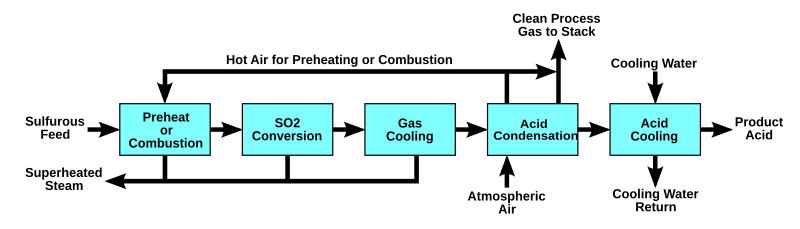
- WSA 프로세스의 주요 반응
- 연소: 2 HS2 + 3 O2 ⇌ 2 HO2 + 2 SO2 (-1036 kJ/mol)
- 산화: 2 SO2 + O2 ⇌ 2 SO3(-198 kJ/mol) [바나듐(V) 산화 촉매가 있는 경우]
- 수화: SO3 + HO2 ⇌ HSO24 (g) (-101 kJ/mol)
- 응축 : HSO24 (g) ⇌ HSO24 (l) (-90 kJ/mol)
위에 언급한 반응에 의해 방출되는 에너지는 대부분 상대적으로 약한 이중 결합을 가진2 O에서 유래한 것으로 증기 생산에 사용된다.[2] 산 1톤당 약 2~3톤의 고압증기가 생성된다.
산업용 응용 프로그램
WSA 프로세스 플랜트가 설치된 산업:
- 정유·석유화학공업
- 금속공업
- 석탄 기반 산업(코킹 및 가스화)
- 전력 산업
- 비스코스 공업
- 황산공업
WSA for gasifiers
가스 공급기 뒤에 설치된 정류소, 셀렉솔, 아민 가스 처리 또는 이와 유사한 장치에서 나오는 산성 가스는 CO 이외에2 HS2, COS 및 탄화수소를 포함한다. 이 가스들은 이전에 종종 폭발하여 대기 중으로 배출되었지만, 지금은 산성 가스가 SO2 배출로 환경에 영향을 주지 않기 위해 정화가 필요하다. WSA 프로세스는 SO2 제거의 요구를 충족할 수 있을 뿐만 아니라, 광범위한 공급 가스 구성도 수용할 수 있다.
WSA 공장은 높은 황 회수율을 제공하며 상당한 증기 생산을 위해 열을 회수한다. 열 회수율이 높고 냉각수 소비량이 적어 이 공정의 원가 성능이 우수하다.[citation needed]
가스화를 위한 WSA 프로세스의 예
예 1:
- 공급 가스 흐름: 14,000Nm3/h
- 구성 [vol %]: HS2 5.8%, COS 1.2%, HC 9.7%, CO2 77.4%
- SOx 농도 [vol %]: 1.58%
- HSO24 생산: 106 MTPD
- 증기발생량: 53톤/h
- 냉각수 소비량: 8 m3/ton산(델타 T = 10 °C)
- 연료 소비량: 1,000Nm3/h(LHV = 2,821kcal/Nm3)
예 2: 중국의 황공장은 암모니아 공장과 연계하여 건설될 것이며, 비료 생산을 위해 연간 500킬로톤/년 암모니아를 생산하게 될 것이다.
사용후산 재생 및 황산 생성
WSA 공정은 또한 황 연소로부터 황산을 생산하거나 알킬화 식물과 같은 사용후산을 재생하는데 사용될 수 있다. 습식 카탈루션 공정은 공급 가스가 촉매와 접촉할 때 과도한 수분을 함유한다는 점에서 다른 접촉 황산 공정과 다르다. 이산화황의 촉매 산화에 의해 형성된 삼산화황은 수분과 즉시 반응하여 온도에 의해 결정되는 범위까지 증기 단계에서 황산을 생성한다. 액체산은 이후에 황산 증기의 응축에 의해 형성되며, 건조한 가스에 기초한 접촉 과정의 경우와 마찬가지로 농축 황산에 삼산화황의 흡수에 의해서 형성되지 않는다.
제품 산의 농도는 촉매변환 기체의 HO2/SO3 비율과 응축 온도에 따라 달라진다.[4][5]
연소 가스는 약 420–440 °C의 컨버터 입구 온도로 냉각된다. 일반적인 냉간 가스 접촉 공정(DCDA) 공장에서 이러한 습식 가스를 처리하려면 모든 습기를 제거하기 위해 가스를 냉각하고 건조시켜야 한다. 그러므로, WSA 과정은 많은 경우에 황산을 더 비용 효율적으로 생산하는 방법이다.
전 세계 황 생산량의 약 80%~85%가 황산 제조에 사용된다. 유엔산업개발기구(UNIDO)와 국제비료개발센터가 공동 발간한 비료매뉴얼에 따르면 세계 황산 생산량의 50%가 비료 생산에 사용되고 있으며, 주로 인산염을 수용성 형태로 전환하는 데 사용된다. [6]
참조
- ^ Gary, J.H. & Handwerk, G.E. (1984). Petroleum Refining Technology and Economics (2nd ed.). Marcel Dekker, Inc. ISBN 0-8247-7150-8.
- ^ 슈미트-로르, K. (2015). J. Chem, "왜2 가연성은 항상 발열성이며 O. 몰 당 약 418 kJ의 수율을 보이는가?" 교육 92: 2094-2099 http://dx.doi.org/10.1021/acs.jchemed.5b00333
- ^ [1]; 세계 연료
- ^ 황 회복; (2007) WSA 프로세스에 의한 황 회수 프로세스 원칙). 덴마크: Jens Kristen Laursen, Haldor Topsoe A/S. 2007년 8월 탄화수소공학부 재인쇄
- ^ U.H.F Sander; H. Fischer; U. Rothe; R. Kola (1984). Sulphur, Sulphur Dioxide and Sulphuric Acid (1st ed.). The British Sulphur Corporation Limited. ISBN 0-902777-64-5.
- ^ [2]; (2008년 7월) IFDC는 비료와 식량안보에 초점을 맞춘 제4호, 제4호, 세계적인 황산부족으로 2009년 1월 6일 웨이백머신에 보관된 비료비용 상승에 기여한다.