정지 흐름
Stopped-flowStopped-flow는 Briton[1][2] Chance가 도입하고 Quentin[3] Gibson이 확장한 1ms의 반시간 화학 반응을 연구하기 위한 실험 기술입니다(온도 점프 [4]방법 등 다른 기술은 훨씬 빠른 공정에서 사용할 수 있습니다).
방법에 대한 설명
요약
정지 흐름 분광법은 용액에서 빠른 반응(밀리초의 절반으로)의 화학 동역학을 연구할 수 있게 한다.그것은 처음에 효소 촉매 반응에 특히 사용되었습니다.그리고 나서 거의 모든 생화학, 생물물리학, 화학 실험실에서 밀리초 단위의 화학 반응을 따라갈 필요가 있는 그 흐름이 빠르게 자리를 잡았습니다.가장 단순한 형태에서 정지된 흐름은 두 가지 솔루션을 혼합합니다.소량의 용액이 고효율 믹서에 빠르고 지속적으로 주입됩니다.이 혼합 과정은 매우 빠른 반응을 일으킨다.새롭게 혼합된 용액은 관찰 셀로 이동하여 셀의 내용물(이전 실험 또는 필요한 세척 단계에서 남은 용액)을 밀어낸다.이 용액이 혼합점에서 관측점까지 통과하는 데 걸리는 시간을 데드타임이라고 합니다.최소 주입 부피는 혼합 셀의 부피에 따라 달라집니다.이전 용액을 완전히 제거하기에 충분한 용액을 주입한 후에는 기기가 정지 상태에 도달하여 흐름을 중지할 수 있습니다.시린지 구동 기술에 따라 흐름 정지는 하드 스톱이라고 하는 스톱 밸브를 사용하거나 스톱 시린지를 사용하여 이루어집니다.또한 stopped-flow는 트리거라는 '시작 신호'를 디텍터로 전송하여 반응을 관찰할 수 있습니다.일반적으로 트리거 타이밍은 사용자가 정지 상태에 도달하기 몇 밀리초 전에 플로우가 정지하는 동시에 트리거할 수 있도록 소프트웨어 제어됩니다.
이것은 매우 경제적인 기술입니다.
반응제 주사기
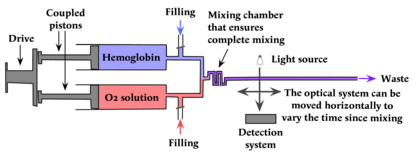
두 개의 주사기는 혼합될 때까지 화학 반응을 일으키지 않는 용액으로 채워져 있습니다.이러한 피스톤은 단일 구동 피스톤 또는 독립 스테핑 모터에 의해 구동되므로 서로 결합되고 내용물이 혼합 장치로 동시에 압출됩니다.
혼합실
주사기에서 두 용액을 밀어낸 후, 두 용액이 층류보다는 난류 흐름과 완전한 혼합을 보장하는 배플이 있는 혼합 시스템으로 들어갑니다. 그러면 두 용액이 불완전한 혼합으로 나란히 흐를 수 있습니다.
데드타임
데드타임은 용액이 혼합점에서 관측점으로 이동하는 시간으로, 관측할 수 없는 역학의 일부입니다.따라서 데드 타임이 낮을수록 사용자는 더 많은 정보를 얻을 수 있습니다.구형 기기에서는 1ms 정도일 수 있지만 개선으로 인해 약 0.3ms의 [5]데드 타임이 허용됩니다.
관찰 셀
혼합 반응물은 자외선 분광법, 형광 분광법, 원형 이색성 또는 빛 산란을 통해 분광 광도학적으로 반응을 따라갈 수 있는 관찰 세포를 통과하며, 현재는 이 [6]중 몇 가지를 결합하는 것이 일반적이다.자기 흡수 효과를 줄이기 위한 형광 측정에는 일반적으로 짧은 광로(0.75 - 1.5mm)의 관측 큐벳이 선호된다.흡광도 측정에는 더 긴 광로(0.5cm - 1cm)의 관측 큐벳이 선호된다.현대의 정지 흐름은 다른 셀 모델을 수용할 수 있으며 두 실험 사이에 큐벳을 변경할 수 있다.정지 흐름 X선 측정의 경우 석영 흡수를 최소화하기 위해 얇은 벽이 있는 석영 모세관을 사용합니다.동일한 모세혈관 내에서 동시에 X선과 흡광도를 측정할 수 있습니다.
정지중
혼합물이 관찰 셀을 통과하면 흐름으로 구동되는 피스톤이 들어 있는 세 번째 주사기로 들어가 흐름을 멈추고 관찰을 활성화하는 스위치를 작동시킵니다.
연속 흐름
정지유동법은 헤모글로빈에 대한 O의2 결합을 연구하기 위해 해밀턴 하트리지와 프란시스 로튼이[7] 사용한 연속유동법의 개발이다.정지 시스템이 없는 경우 반응 혼합물은 관측 시스템을 지나 긴 튜브로 전달되어 폐기됩니다(1923년 단순한 색계).컬러미터를 튜브를 따라 이동하고 유량을 파악함으로써 Hartridge와 Rougton은 알려진 시간이 지난 후 과정을 측정할 수 있었습니다.
그 당시에는, 이것은 분명히 다루기 어려운 문제(측정마다 초가 걸리는 장비로 밀리초가 걸리는 프로세스를 연구하는 것)를 단순한 장비로 해결할 수 있다는 것을 보여주는 혁명적인 발전이었습니다.그러나 실제로는 많은 양의 반응물로 제한되었다. 단백질의 경우 헤모글로빈의 반응으로 효과적으로 제한되었다.실용적 목적상 이 접근법은 구식이다.
급랭 흐름
정지 흐름 방법은 반응 추이에 사용할 수 있는 스펙트럼 분석 성질의 존재에 따라 달라집니다.그렇지 않은 경우 급랭 흐름은 분석을 [8]위해 기존의 화학적 방법을 사용하는 대안을 제공합니다.기계적 정지 시스템 대신 즉시 반응을 정지하는 수신자에게 제품을 전달하고, 즉 즉 즉석에서 동결하거나 화학 변성제로 효소를 변성시키거나 시료를 변성 광원에 노출시킴으로써 반응을 정지시킨다.연속유동법과 마찬가지로 튜브의 길이를 변화시킴으로써 혼합과 담금질 사이의 시간을 변화시킬 수 있다.
Alan Fersht와 Ross[9] Jakes가 도입한 펄스 급랭식 흐름법은 긴 튜브의 필요성을 극복합니다.이 반응은 정지된 흐름 실험에서와 똑같이 시작되지만, 시작 후 확실하고 사전 설정된 시간을 발생시키는 세 번째 주사기가 있습니다.
급랭된 흐름은 정지된 흐름과 관련하여 장점과 단점을 모두 가지고 있습니다.한편, 화학 분석을 통해 어떤 과정이 측정되는지 알 수 있지만, 분광 신호가 어떤 과정을 나타내는지 항상 알 수 있는 것은 아닙니다.반면, 급랭된 흐름은 시간 코스의 각 지점을 개별적으로 결정해야 하므로 훨씬 더 힘이 듭니다.Klebsiella pneumniae의[10] 질소화효소에 의한 촉매작용을 위해 왼쪽에 있는 이미지는 이 두 점을 모두 보여준다. 절반의 합의는 420 nm에서의 흡광도가 P의i 방출을 측정했음을 나타내지만 급랭 흐름 실험에는 11개의 데이터 포인트가 필요했다.
레퍼런스
- ^ Chance, Britton (1951). "Rapid and Sensitive Spectrophotometry. I. The Accelerated and Stopped‐Flow Methods for the Measurement of the Reaction Kinetics and Spectra of Unstable Compounds in the Visible Region of the Spectrum". Review of Scientific Instruments. 22 (8): 619–627. doi:10.1063/1.1746019.
- ^ Chance, Britton; Legallais, Victor (1951). "Rapid and Sensitive Spectrophotometry. II. A Stopped‐Flow Attachment for a Stabilized Quartz Spectrophotometer". Review of Scientific Instruments. 22 (8): 627–634. doi:10.1063/1.1746020.
- ^ Gibson, Q. H. (1954). "Stopped-flow apparatus for the study of rapid reactions". Discussions of the Faraday Society. 17: 137. doi:10.1039/df9541700137.
- ^ Eigen, M. (1954). "Methods for investigation of ionic reactions in aqueous solutions with half-times as short as 10–9sec. Application to neutralization and hydrolysis reactions". Discuss. Faraday Soc. 17: 194–205. doi:10.1039/df9541700194.
- ^ Clark, Charles R. (1997). "A Stopped-Flow Kinetics Experiment for Advanced Undergraduate Laboratories: Formation of Iron(III) Thiocyanate". Journal of Chemical Education. 74 (10): 1214. Bibcode:1997JChEd..74.1214C. doi:10.1021/ed074p1214.
- ^ Guillerm, Jessica; Frère, Jean-Marie; Meersman, Filip; Matagne, André (2021). "The right-handed parallel β-helix topology of Erwinia chrysanthemi pectin methylesterase is intimately associated with both sequential folding and resistance to high pressure". Biomolecules. 11: 1083. doi:10.3390/biom11081083. PMC 8392785. PMID 34439750.
- ^ Hartridge, H.; Roughton, F. J. W. (1923). "A method for measuring the velocity of very rapid chemical reactions". Proceedings of the Royal Society A. 104 (726): 376–394. Bibcode:1923RSPSA.104..376H. doi:10.1098/rspa.1923.0116.
- ^ Pinsent, B R W (1954). "A quenching method for studying rapid reactions". Discussions of the Faraday Society. 17: 140–141. doi:10.1039/df9541700140.
- ^ Fersht, A R; Jakes, R (1975). "Demonstration of two reaction pathways for aminoacylation of transfer-RNA: application of pulsed quenched flow technique". Biochemistry. 14 (15): 3350–3356. doi:10.1021/bi00686a010.
- ^ Thorneley, R N F; Cornish-Bowden, A (1977). "Kinetics of nitrogenase of Klebsiella-pneumoniae: heterotropic interactions between magnesium-adenosine 5'-diphosphate and magnesium-adenosine 5'-triphosphate". Biochem. J. 165 (2): 255–262. doi:10.1042/bj1650255. PMC 1164896.
추가 정보
- Alan Fersht (1998). Structure and Mechanism in Protein Science: Guide to Enzyme Catalysis and Protein Folding. New York: W. H. Freeman. pp. 132–168. ISBN 9780716732686.
- Athel Cornish-Bowden (2012). Fundamentals of Enzyme Kinetics (4th ed.). Weinheim: Wiley-Blackwell. pp. 391–396. ISBN 978-3527330744.