마름모꼴 입술
Rhombic lip마름모꼴 입술은 척추동물 배아 내에서 일시적으로 인식될 수 있는 발달 중인 메트뇌의 후부이다.그것은 제4심실 지붕에서 [1]배면의 신경상피세포까지 후방으로 뻗어있다.마름모꼴 립은 후두뇌 [2]발달 초기 단계에서 인식할 수 있는 마름모세포 1~8(r1-r8)에 기초하여 8개의 구조 단위로 나눌 수 있다.과립 세포와 5개의 뇌간 핵을 생성하는 마름모꼴 입술은 복잡한 소뇌 신경계를 [3]발달시키는데 중요한 역할을 합니다.
역사
1890년대 후반에 수행된 인간 배아의 연구를 통해, 스위스 해부학자 빌헬름 히스는 형태학에서 후뇌 신경 상피질의 나머지 부분과 구별되는 부분을 확인했고, 배아 발생의 후기로의 지속적인 염색체 분열, 그리고 후뇌 p를 통한 뉴런의 흐름의 배치를 확인하였습니다.에러웨어그는 이 구역을 "라우텐리페" 또는 마름모꼴 입술이라고 이름 붙였습니다. 왜냐하면 그것이 입 모양과 매우 흡사한 제 4뇌실의 마름모꼴 개구부에서 나온 것 같았기 때문입니다.그는 마름모꼴 입술이 배쪽으로 이동하여 관골핵과 감람핵을 채우는 전뇌전구(前ce前ce)를 가지고 있다고 제안했지만, 그 당시 이용 가능한 방법론은 그가 수집할 수 있는 증거의 양을 제한했다.전뇌신경세포가 등쪽에서 유래했다는 최초의 진짜 증거는 1990년대에 메추리 후뇌신경상피질의 일부를 오보에서 병아리 배아에 이식하는 기술인 병아리 메추리 키메라(chick-mail chimera)를 사용하여 얻어졌다.메추리 딸세포의 복부 이동을 추적한 결과 히스의 [4]이론이 확인됐다.
발전
| 메트뇌론 | |
|---|---|
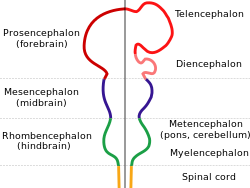 | |
 | |
| 식별자 | |
| NeuroLex ID | birnlex_965 |
| 신경해부술의 해부학적 용어 | |
소뇌영역의 기원
마름모꼴 립의 세포 기여
- 소뇌의 신경 사양은 제4심실의 [7]대칭 팽대부에서 시작된다.태아기 9일에서 11일 무렵, 세포는 두 가지 부위에서 발생한다: 마름모꼴 입술과 심실 영역.마름모꼴 입술은 글루탐산 과립 뉴런(r1에서 진화)과 5개의 뇌간핵(r6-r8에서 진화한 것으로 생각됨)을 생성한다.하등 감람핵인 뇌간 누셀레우스(nuceleus)는 피르키네 세포에 기어오르는 섬유를 투사한다.다른 네 개의 핵(외측 쐐기핵, 외측 망막핵, 폰틴핵, 시상망막핵)은 내부 과립 뉴런에 [2][4][7]이끼성 섬유를 투사한다.한편, 심실 영역의 세포는 GABAergic Purkinje 세포(소뇌 뉴런의 또 다른 유형)와 깊은 소뇌 [8]핵으로 진화한다.
마름모꼴 입술 발달
- 제4심실과 지붕판 사이에 위치한 마름모꼴 입술은 r1에서 r8까지 확장되며 나중에 [2][7]발달하는 동안 뇌간이 구부러질 때 위쪽 또는 소뇌, 아래쪽 또는 후뇌 부분으로 나눌 수 있습니다.기본 나선-루프-나선 구조를 가진 전사 인자 Math1의 발현은 마름모꼴 립의 배아 상피를 지배하며, 배아 9.5일(E9.5)[7][9]부터 중뇌 및 후뇌 영역에서 발현된다.수학 1-늘 마우스는 소뇌의 과립 뉴런과 전뇌계의 [7]폰틴 핵을 포함한 여러 마름모꼴 입술 유도체가 없는 것으로 나타났다.마름모꼴 입술은 발아층(E12.5 이전)에서 먼저 이주하는 Math1 발현 전구체가 심층핵 뉴런이 되고, 후발(E13)이 과립 [8]세포가 되는 시간 운명 지도에 따라 구성된다.병아리 메추리 키메라 실험은 r1이 과립 세포 전구체의 가장 가능성이 높은 공급원이라는 것을 보여주었다.마름모꼴 입술 안에서 과립 세포 전구체는 단극 형태학을 분열시키고 발전시키며,[7] 목적지를 향해 돌출하는 단일 과정을 가지고 있다.
- 개발이 계속됨에 따라 RL에서 생성된 과립 전구 세포는 외부 과립층(EGL)을 생성한다.이 움직임은 E15와 P15 사이에 발생합니다(산전 15와 산후 15).EGL은 소뇌 전체를 [8]감싸고 있는 2차 발아 상피이다.이 시기는 소뇌의 중요한 발달 단계이다.EGL 전구 세포의 확장은 성인 소뇌 [6]피질에서 250:1의 푸르키네 세포보다 많은 많은 뉴런 집단을 생성한다.EGL의 과립 뉴런은 세포 증식에 특이하고 중요한 역할을 하는 유전자를 발현합니다.이 유전자들은 Math1, RU49/Zipro1, [7]Zic1이라고 불립니다.앞서 언급했듯이, Math1은 RL의 개발 초기에 표현된다.RU49/Zipro1과 관련된 녹아웃 실험은 뇌 구조에 거의 변화를 일으키지 않지만, 이러한 유전자의 과잉 발현은 과립 세포의 양과 외부 EGL의 [7]증식을 극적으로 증가시킨다.이 결과는 RU49/Zipro1 유전자가 세포 증식에 충분한 역할을 한다는 것을 시사한다.
- EGL이 완전히 형성되면 과립 세포 전구체는 내부 과립층이라고 불리는 층을 형성하면서 안쪽으로 이동합니다.이동 직전에 세포들은 일련의 전기생리학적 변화를 겪는다.NMDA 수용체는 세포가 [7]더 이동할 수 있도록 준비하기 위해 활성화되는 것으로 여겨진다.이러한 NMDA 수용체의 활성화는 세포의 탈분극을 일으킨다.이 탈분극의 균형을 맞추기 위해 채널 GIRK2가 활성화된다.NMDA 수용체가 세포를 [7]탈분극시킨 후 세포 과분극에 관여한다.이러한 변화가 일어나는 동안, 세포들은 또한 방사상 신경교세포에 의해 이 새로운 층으로 유도된다.IGL에 들어가면 분열을 멈추고 Math1 유전자를 발현하지 않게 됩니다.
레퍼런스
- ^ Gilthorpe JD, Papantoniou EK, Chédotal A, Lumsden A, Wingate RJ (October 2002). "The migration of cerebellar rhombic lip derivatives". Development. 129 (20): 4719–28. PMID 12361964.
- ^ a b c Dun XP (August 2012). "Origin of climbing fiber neurons and the definition of rhombic lip". International Journal of Developmental Neuroscience. 30 (5): 391–5. doi:10.1016/j.ijdevneu.2012.02.002. PMID 22406199.
- ^ Wingate RJ (February 2001). "The rhombic lip and early cerebellar development". Current Opinion in Neurobiology. 11 (1): 82–8. doi:10.1016/S0959-4388(00)00177-X. PMID 11179876.
- ^ a b Ray RS, Dymecki SM (December 2009). "Rautenlippe Redux -- toward a unified view of the precerebellar rhombic lip". Current Opinion in Cell Biology. 21 (6): 741–7. doi:10.1016/j.ceb.2009.10.003. PMC 3729404. PMID 19883998.
- ^ Rod, Seeley (2012). Seeley's Anatomy and Physiology. New York, NY: McGraw Hill. p. 1152. ISBN 978-0-07-352561-7.
- ^ a b Hatten ME, Heintz N (1995). "Mechanisms of neural patterning and specification in the developing cerebellum". Annual Review of Neuroscience. 18: 385–408. doi:10.1146/annurev.ne.18.030195.002125. PMID 7605067.
- ^ a b c d e f g h i j k l m Wang VY, Zoghbi HY (July 2001). "Genetic regulation of cerebellar development". Nature Reviews Neuroscience. 2 (7): 484–91. doi:10.1038/35081558. PMID 11433373.
- ^ a b c d e Carletti B, Rossi F (February 2008). "Neurogenesis in the cerebellum". The Neuroscientist. 14 (1): 91–100. doi:10.1177/1073858407304629. PMID 17911211.
- ^ Rowan, Alison (2005). "The mystery of Maths". Nature Reviews Neuroscience. 6 (12): 916. doi:10.1038/nrn1813.
추가 정보
- Rowan, Alison (2006). "Development: Mapping cerebellar development". Nature Reviews Neuroscience. 7 (8): 598. doi:10.1038/nrn1982.



