몰리브데이트
Molybdate화학에서 몰리브데이트는 가장 높은 산화상태인 6의 몰리브덴을 가진 옥소아니온을 함유한 화합물이다. 몰리브덴은 불연속 구조물이나 중합체 확장 구조물이 될 수 있는 매우 큰 범위의 옥소이온을 형성할 수 있지만, 후자는 고체 상태에서만 발견된다. 더 큰 옥소이온은 폴리옥소메탈산염이라고 불리는 화합물 그룹의 구성원이며, 그것들은 오직 하나의 금속 원자만을 포함하고 있기 때문에 종종 이소폴리메탈산염이라고 불린다.[1] 이산 몰리브덴 산소는 칼륨 몰리브데일에서 발견된 가장 단순한 MoO에서부터 예를2−
4 들어 154 Mo 원자를 포함하는 이소폴리-몰리브덴 블루스에서 발견된 매우 큰 구조까지 크기가 다양하다. 몰리브덴의 행동은 그룹 6의 다른 요소들과 다르다. 크롬은 사면체 크롬에 기반한 크롬, CRO2−
4, CRO
22−
7
32−
10, CRO
42−
13 이온만을 형성한다. 텅스텐은 몰리브덴과 유사하며 6개의 좌표 텅스텐을 포함하는 많은 텅스타이트를 형성한다.[2]
몰리브데이트 음이온의 예
몰리브데일 옥수수의 예는 다음과 같다.
- MoO2−
4, 예: NaMoO와24 미네랄 파월라이트 CaMoO4; - MoO
22−
7, 수성암모늄 다이몰리브데이트. MoO의
22−
7 무수 테트라부틸람모늄 소금도 알려져 있다.[3] - 에틸렌디아민 소금의 MoO
32−
10,[4] - 칼륨 소금의 MoO
42−
13,[5] - 음이리늄(CHNH
6
5+
3) 소금의 MoO
52−
16,[6] - 테트라메틸람모늄 소금의 MoO
62−
19([7]헥사 몰리브데이트) - MoO
76−
24 in 암모늄 몰리브데일, (NH4)6MoO724/4H2O;[8] - 트리메틸람모늄 소금의 MoO
84−
26.[1]
몰리브다이트의 명칭은 일반적으로 존재하는 Mo 원자의 수를 나타내는 접두사의 관례를 따른다. 예를 들어, 2개의 몰리브덴 원자에 대한 dimolybdate, 3개의 몰리브덴 원자에 대한 trimolybdate 등. 때때로 산화 상태는 펜타몰리브데일(VI)과 같이 접미사로 추가된다. 헵타몰리브데일 이온인 MoO는
76−
24 흔히 "paramolybdate"라고 불린다.
몰리브데이트 음이온의 구조
작은 음이온인 MoO와2−
4 MoO는
22−
7 사면중심이다. MoO에서2−
4 4개의 옥시겐은 황산염과 색산염과 동등하며, 결합 길이와 각도가 같다. MoO는
22−
7 하나의 모퉁이를 공유하는 두 개의 4면체, 즉 하나의 브리징 O 원자로 간주될 수 있다.[1] 더 큰 음이온 몰리브덴에서는 일반적으로 6개의6 좌표가 MoO 옥타헤드라의 가장자리 또는 정점이 공유되는 것은 아니다. 팔면체는 왜곡되며, 일반적인 M-O 결합 길이는 다음과 같다.
- 단자 비브리지 M–O 약 1.7 å
- M–O–M 유닛을 브리징할 때 약 1.9 å
MoO
84−
26 음이온은 팔면체와 사면체 몰리브덴을 모두 포함하고 있으며 알파와 베타라는 2개의 이항체 형태로 분리될 수 있다.[2]
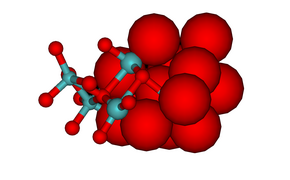
아래 16진법 이미지는 조정 다면체를 보여준다. 헵타몰리브데이트 이미지는 구조물에 있는 산소 원자의 밀접하게 포장된 성질을 보여준다. 산화 이온은 이온 반경이 1.40 å이고, 몰리브덴(VI)은 0.59 å 훨씬 작다.[1] 몰리브다이트의 구조와 몰리브덴 산화물(MoO3, MoO2 및 "결정전단" 산화물, MoO926, MoO1029) 사이에는 강한 유사성이 있다.[9]
수용액 속의 평형수
MoO3, 몰리브데넘 삼산화물이 알칼리 용액에 용해되면 간단한 MoO2−
4 음이온이 생성된다.
- MoO3 + 2 NaOH → NaMoO24 + HO2
pH를 낮추면 응축이 뒤따르며, 물의 손실과 Mo-O-Mo 연결의 형성이 이루어진다. 육각, 헵타, 옥타몰리브다이트로 이어지는 스토이치측정법은 다음과 같다.[1][10]
- 6 [MoO4]2- + 10 HCl → [MoO619]2- + 10 Cl− + 5 HO2:
- 7 MoO2−
4 + 8 H+ → MoO
76−
24 + 4 HO2 - MoO
76−
24 + 3 H+ →mo MoO
84−
26 + 2 HO2
과산화합체
많은 과독성 독소가 알려져 있다. 그들은 과산화수소를 이용한 몰리브데일염의 치료로 형성되는 경향이 있다. 주목할 만한 것은 모노머-다이머 평형[MoO23(O2)(2HO2)]22− 【MoO23(O2)(4HO2)】22−이다. 또한 알려져 있지만 불안정한 것은 [Mo(O2)]42−이다(Tetraperoxoxromate(V) 칼륨 참조). 일부 관련 화합물은 유기합성에서 산화제로 사용된다.[11]
테트라티오몰리브데이트
몰리브데일 용액을 황화수소 처리했을 때 적색 테트라티오몰리브데일 음이온 결과:
- [NH4]2[MoO4] + 4 H2S → [NH4]2[MoS4] + 4 H2O
몰리브데이트 자체와 마찬가지로 MoS는2−
4 산이 있는 곳에서 응축을 겪지만 이러한 응축은 리독스 공정을 동반한다.
산업용
카탈루션
몰리브다이트는 촉매에 널리 사용된다. 규모 면에서 몰리브데일의 가장 큰 소비자는 유황이 석유에서 제거되는 과정인 수황화 촉매를 위한 선행물질이다. 비스무트 몰리브다이트는 명목상 BiPMoO91252 성분으로 프로필렌의 아크릴로니트릴에 대한 암산화 촉매를 촉진한다. 페릭 몰리브다이트는 산업적으로 메탄올과 포름알데히드의 산화를 촉진하기 위해 사용된다.[12]
부식억제제
나트륨 몰리브데일은 부식 억제제로 공업용수 처리에서 사용되어 왔다. 처음에는 독성을 위해 색산이 금지되었을 때, 색산을 대체하는 것이 좋다고 생각되었다. 단, 몰리브데이는 단독으로 사용할 경우 고농도를 필요로 하므로 일반적으로 보완적 부식 억제제가 첨가되며,[13] 주로 고온 폐쇄 루프 냉각 회로에 사용된다.[14] 실험연구에 따르면, 몰리브데이트는 미생물학적으로 유발된 부식(MIC)에 대한 효율적인 바이오시드(biocide)[15]로 보고되었으며, 이때 몰리브데일/일 1.5mM를 더하면 부식률이 50% 감소하였다.
슈퍼커패시터
몰리브다테스(특히 FeMoO4, Fe2(MoO4),3 NiMoO4, CoMoO4, MnMoO4)는 수용성 콘덴서에서 양극 또는 음극 물질로 사용되어 왔다.[16][17][18][19] 유사 용량성 전하 저장으로 인해 최대 1500 F g의−1 특정 정전 용량이 관찰되었다.[17]
약
몰리브데넘-99는 핵의학 영상촬영을 위한 테크네튬-99m 발전기에서 모체 동위원소로 사용된다.[20]
기타
질소 고정에는 콩, 아카시아 등 콩류에서 몰리브도엔자임(molybdoenzymes)이 필요하다. 이런 이유로 비료는 종종 소량의 몰리브데일 염분을 함유하고 있다. 커버리지는 일반적으로 1에이커당 1킬로그램 미만이다.[12]
몰리브데일 크롬 색소는 특별하지만 시중에서 구할 수 있는 색소다.[12] 몰리브데일(보통 칼륨 몰리브데일의 형태로)은 몰리브덴 청색법이라 불리는 용액 내 실리카 농도에 대한 분석 색도 시험에도 사용된다.[21] 또한, 염료 말라카이트 그린과 관련하여 인산염 수량의 색도 측정에 사용된다.
수집 가능한 몰리브데이트
마다와스카 광산에서 나온 세계 최고의 크리스탈 몰리브데이트 샘플을 가지고 보석 애호가들이 수집한 몰리브데일 크리스탈.[22]
참조
- ^ a b c d e Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ a b c d Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999), Advanced Inorganic Chemistry (6th ed.), New York: Wiley-Interscience, ISBN 0-471-19957-5
- ^ V. W. Day; M. F. Fredrich; W. G. Klemperer; W. Shum (1977). "Synthesis and characterization of the dimolybdate ion, Mo
2O2−
7". Journal of the American Chemical Society. 99 (18): 6146. doi:10.1021/ja00460a074. - ^ Guillou N.; Ferey G. (August 1997). "Hydrothermal Synthesis and Crystal Structure of Anhydrous Ethylenediamine Trimolybdate (C
2H
10N
2)[Mo
3O
10]". Journal of Solid State Chemistry. 132 (1): 224–227(4). Bibcode:1997JSSCh.132..224G. doi:10.1006/jssc.1997.7502. - ^ B. M. Gatehouse; P. Leverett (1971). "Crystal structure of potassium tetramolybdate, K
2Mo
4O
13, and its relationship to the structures of other univalent metal polymolybdates". J. Chem. Soc. A: 2107–2112. doi:10.1039/J19710002107. - ^ W. Lasocha; H. Schenk (1997). "Crystal Structure of Anilinium Pentamolybdate from Powder Diffraction Data. The Solution of the Crystal Structure by Direct Methods Package POWSIM". J. Appl. Cryst. 30 (6): 909–913. doi:10.1107/S0021889897003105.
- ^ S. Ghammami (2003). "The crystal and molecular structure of bis(tetramethylammonium) hexamolybdate(VI)". Crystal Research and Technology. 38 (913): 913–917. doi:10.1002/crat.200310112.
- ^ Howard T. Evans jr.; Bryan M. Gatehouse; Peter Leverett (1975). "Crystal structure of the heptamolybdate(VI)(paramolybdate) ion, [Mo7O24]6−, in the ammonium and potassium tetrahydrate salts". J. Chem. Soc., Dalton Trans. (6): 505–514. doi:10.1039/DT9750000505.
- ^ "산화물: 고체 화학" W.H. 맥캐롤, 무기 화학 에드 백과사전 R. Bruce King, John Wiley and Sons(1994) ISBN 0-471-93620-0
- ^ Klemperer, W. G. (1990). "Tetrabutylammonium Isopolyoxometalates". Inorganic Syntheses. Inorganic Syntheses. 27. pp. 74–85. doi:10.1002/9780470132586.ch15. ISBN 9780470132586.
- ^ Dickman, Michael H.; Pope, Michael T. (1994). "Peroxo and Superoxo Complexes of Chromium, Molybdenum, and Tungsten". Chem. Rev. 94 (3): 569–584. doi:10.1021/cr00027a002.
- ^ a b c 로저 F. 세베닉 외 2005년 울만 화학 기술 백과사전 "몰리브덴과 몰리브덴 화합물"; 웨인하임 와일리-VCH doi:10.1002/14356007.a16_655
- ^ "Open Recirculating Cooling Systems - GE Water". gewater.com.
- ^ "Closed Recirculating Cooling Systems - GE Water". gewater.com.
- ^ "Microbiologically Influenced Corrosion in the Upstream Oil and Gas Industry".
- ^ Purushothaman, K. K.; Cuba, M.; Muralidharan, G. (2012-11-01). "Supercapacitor behavior of α-MnMoO4 nanorods on different electrolytes". Materials Research Bulletin. 47 (11): 3348–3351. doi:10.1016/j.materresbull.2012.07.027.
- ^ a b Senthilkumar, Baskar; Sankar, Kalimuthu Vijaya; Selvan, Ramakrishnan Kalai; Danielle, Meyrick; Manickam, Minakshi (2012-12-05). "Nano α-NiMoO4as a new electrode for electrochemical supercapacitors". RSC Adv. 3 (2): 352–357. doi:10.1039/c2ra22743f. ISSN 2046-2069.
- ^ Cai, Daoping; Wang, Dandan; Liu, Bin; Wang, Yanrong; Liu, Yuan; Wang, Lingling; Li, Han; Huang, Hui; Li, Qiuhong (2013-12-26). "Comparison of the Electrochemical Performance of NiMoO4 Nanorods and Hierarchical Nanospheres for Supercapacitor Applications". ACS Applied Materials & Interfaces. 5 (24): 12905–12910. doi:10.1021/am403444v. ISSN 1944-8244. PMID 24274769.
- ^ Xia, Xifeng; Lei, Wu; Hao, Qingli; Wang, Wenjuan; Wang, Xin (2013-06-01). "One-step synthesis of CoMoO4/graphene composites with enhanced electrochemical properties for supercapacitors". Electrochimica Acta. 99: 253–261. doi:10.1016/j.electacta.2013.03.131.
- ^ National Research Council (US) Committee on Medical Isotope Production Without Highly Enriched Uranium. (2009). "Molybdenum-99/Technetium-99m Production and Use". Medical Isotope Production without Highly Enriched Uranium. Washington DC: National Academies Press.
- ^ "ASTM D7126 - 15 Standard Test Method for On-Line Colorimetric Measurement of Silica". astm.org.
- ^ McDougall, Raymond (2019-09-03). "Mineral Highlights from the Bancroft Area, Ontario, Canada". Rocks & Minerals. 94 (5): 408–419. doi:10.1080/00357529.2019.1619134. ISSN 0035-7529.