고급 산화 과정
Advanced oxidation process선진 산화 공정(AOPs)은 넓은 의미에서 수산화기(·OH)와의 반응을 통해 산화함으로써 물과 폐수의 유기(그리고 때로는 무기물) 물질을 제거하도록 설계된 일련의 화학 처리 절차다.[1] 그러나 폐수 처리의 실제 적용에서 이 용어는 일반적으로 오존(O3), 과산화수소(HO22) 및/또는 자외선을 이용하는 화학 공정의 하위 집합을 더 구체적으로 언급한다.[2] 그러한 유형의 공정 중 하나는 현장 화학적 산화라고 불린다.
설명
AOP는 고반응성 수산화기(·OH)의 현장 생산에 의존한다. 이 반응성 종들은 물에 응용될 수 있는 가장 강한 산화제로서 물 행렬에 존재하는 거의 모든 화합물을 종종 확산 제어 반응 속도로 산화시킬 수 있다. 결과적으로, ·OH는 일단 형성되면 눈에 띄지 않게 반응하고 오염물질은 빠르고 효율적으로 분해되어 작은 무기 분자로 변환될 것이다. 히드록실산기는 하나 이상의 일차 산화제(예: 오존, 과산화수소, 산소) 및/또는 에너지 소스(예: 자외선) 또는 촉매(예: 이산화티타늄)의 도움을 받아 생성된다. 최대 •OH 수율을 얻기 위해 이러한 시약의 정밀하고 사전 프로그래밍된 용량, 시퀀스 및 조합이 적용된다. 일반적으로 적절히 튜닝된 조건에서 AOP를 적용하면 오염물질의 농도를 수백 ppm에서 5 ppb 미만으로 낮출 수 있어 COD와 TOC가 크게 낮아져 '21세기 물 처리 과정'[3]의 공로를 인정받게 된다.
AOP 절차는 특히 아로마틱스, 농약,[4] 석유 성분 및 폐수의 휘발성 유기 화합물과 같은 생물학적으로 독성이 있거나 분해되지 않는 물질을 청소하는 데 유용하다.[5] 또한, AOP는 2차 처리된 폐수의 유출물을 치료하는데 사용될 수 있으며, 이를 3차 처리라고 한다.[6] 오염 물질은 주로 물, 이산화탄소, 소금과 같은 안정적인 무기 화합물로 전환된다. 즉, 그들은 광물화를 겪는다. AOP 절차를 통한 폐수 정화의 목표는 화학적 오염물질과[7] 독성을 감소시킴으로써 깨끗한 폐수를 수신 하천이나 최소한 재래식 하수 처리로 재도입할 수 있다.
비록 산화 과정 ·OH과 관련된 사용에 늦게 19세기(그것은 분석 시약으로 그 시간에 사용됐어 펜톤 시약, 같은)부터 존재해 왔다, 물 치료에 그러한 산화적 종의 이용 글레이즈(알까지 적절한 관심을 받지 않았다.[1]" 충분한 수량에·OH의 가능한 세대를 제안했다. 수질 정화에는 영향을 미치며 1987년 처음으로 "고급 산화 과정"이라는 용어를 정의했다. AOP는 비교적 높은 관련 비용 때문에 오늘날까지 대규모로 (특히 개발도상국에서는) 상업적으로 사용되지 않고 있다. 그럼에도 불구하고 높은 산화능력과 효율성으로 인해 AOPs는 가장 완고하게 저항하는 유기·무기 오염물질을 제거해야 하는 3차 치료에서 인기 있는 기법이 되고 있다. 물 재이용에 대한 관심이 높아지고 수질오염과 관련한 보다 엄격한 규제가 현재 AOP의 본격 시행을 가속화하고 있다. 현재 전 세계적으로 주로 유럽과 미국에서 상용화된 AOP 설비가 약 500개 있다. 중국과 같은 다른 나라들은 AOPs에 대한 관심이 증가하고 있다.[citation needed]
화학 원리
일반적으로, AOPs에서의 화학은 기본적으로 세 부분으로 나눌 수 있다.[8]
- ·OH의 형성;
- ·OH에 의한 표적 분자에 대한 초기 공격 및 단편화
- 궁극적인 광물화까지 ·OH에 의한 후속 공격.
·OH 생산(Part 1)의 메커니즘은 사용되는 AOP 기법의 종류에 따라 크게 달라진다. 예를 들어, ozonation, UV/HO22, 광촉매 산화 및 Fenton의 산화는 ·OH 생성의 다른 메커니즘에 의존한다.
- HO22 + UV → 2·OH (HO의22 O-O 본드 균열은 2·OH 활성산소의 형성으로 이어진다)
- HARL + UV → ·OH + Cl.
- 오존 기반 AOP:[12]
- O3 + HO− → HO2− + O2 (O와3 히드록실 이온 사이의 반작용은 HO22 (충전된 형태) 형성을 유도한다.
- O3 + HO2− → HO2 · + O3−· (두 번째 O3 분자가 HO와2− 반응하여 오조나이드 급진성을 생성함)
- O3−··+H+ → HO3·(이 급진은 양성 시 ·OH에 부여)
- HO3· → ·OH + O2
- 여기에 제시된 반응 단계는 반응 시퀀스의 일부일 뿐이며 자세한 내용은 참조를 참조하십시오.
- 펜턴 기반 AOP:[13]
Fe2+ + HO22 → Fe3++ HO·+OH− (펜톤 시약 개시)
Fe3+ + HO22 → Fe2++HO·+H+ (Fe2+ 촉매 재생)
HO22 → HO · + HO · + HO2 (HO의22 자가 청소 및 분해)
여기에 제시된 반응 단계는 반응 시퀀스의 일부일 뿐이며 자세한 내용은 참조를 참조하십시오.
- TiO를2 사용한 광촉매 산화:[12]
- TiO2 + UV → e− + h+ (광촉매 표면의 방사선은 흥분된 전자(e−)와 전자 갭(h+)으로 이어진다)
- Ti(IV) + HO2 ⇌ Ti(IV)-HO2(수분이 촉매 표면에 흡착됨)
- Ti(IV)-HO2 + h h+ Ti(IV)-·OH + H+ 반응성이 높은 전자 갭은 물과 반응한다.
- 여기에 제시된 반응 단계는 반응 시퀀스의 일부일 뿐이며 자세한 내용은 참조를 참조하십시오.
현재 파트 3의 세부적인 메커니즘에 대한 합의는 없지만, 연구자들은 파트 2의 초기 공격 과정에 대해 조명하고 있다. 본질적으로 ·OH는 급진적인 종이며 매우 반응성이 높은 전기영역처럼 행동해야 한다. 따라서 초기 공격의 두 가지 유형은 수소 추상화와 추가가 되어야 한다. 기술 핸드북에서 채택하여 나중에 정제된 다음 계획은 ·OH에 의한 벤젠 산화의 가능한 메커니즘을 설명한다.[14]
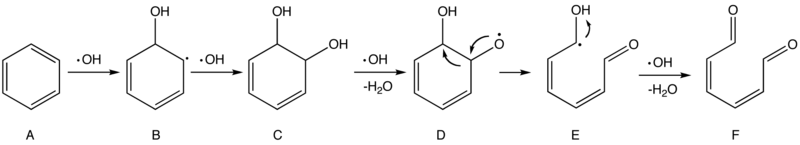
Scheme 1. 히드록실산기에 의한 벤젠 산화의 메커니즘
첫 번째와 두 번째 단계는 벤젠(A)에서 방향족 고리를 깨고 중간 C에서 두 개의 히드록실 그룹(–OH)을 형성하는 전기영양 첨가다. 나중에 a ·OH는 수산화기군 중 하나에 수소 원자를 잡고, 보다 안정적인 급진(E)을 형성하기 위해 재배열을 거치기 쉬운 급진종(D)을 생산한다. 반면 E는 ·OH의 공격을 쉽게 받아 결국 2,4헥사디엔-1,6디오네(F)를 형성한다. 충분한 ·OH 활성산소가 있는 한, 그 이후의 화합물 F에 대한 공격은 결국 파편들이 모두 HO나2 CO와2 같은 작고 안정적인 분자로 변환될 때까지 계속될 것이지만, 그러한 과정들은 여전히 무수히 많은 가능성과 부분적으로는 알 수 없는 메커니즘의 대상이 될 수도 있다.
이점
AOPs는 수처리 분야에서 다음과 같은 몇 가지 장점을 가지고 있다.
- 그들은 오염물질을 다른 단계로 모으거나 옮기기 보다는 수성 단계에서 유기 화합물을 효과적으로 제거할 수 있다.
- ·OH의 반응성 때문에 많은 수용성 오염물질과 차별 없이 반응한다. 따라서 AOP는 많은 유기 오염물질을 동시에 제거해야 하는 많은 시나리오에서 적용 가능하다.
- 일부 중금속은 침전된 M(OH)의 형태로도 제거될 수 있다.x
- 일부 AOPs 설계에서는 소독도 달성할 수 있으며, 따라서 이러한 AOP는 일부 수질 문제에 대한 통합 해결책이 된다.
- ·OH의 완전감소제품은 HO이므로2 AOPs는 이론적으로 새로운 유해물질을 물속에 전혀 도입하지 않는다.
현재의 단점
AOP는 완벽하지 않고 여러 가지 단점이 있다.[15]
- 가장 중요한 것은 대부분의 AOP 시스템의 작동을 유지하기 위해 값비싼 화학 시약을 지속적으로 투입해야 하기 때문에 AOP의 비용이 상당히 높다는 것이다. AOP는 바로 그 성질의 결과, 제거할 오염물질의 양에 비례하는 히드록실산기 및 기타 시약을 필요로 한다.
- 일부 기법은 신뢰할 수 있는 성능을 보장하기 위해 폐수의 사전 처리가 필요하며, 이는 잠재적으로 비용이 많이 들고 기술적으로 요구될 수 있다. 예를 들어, 중탄산염 이온(HCO3−)의 존재는 HO와2 훨씬 덜 반응적인 종인 ·CO를3− 산출하는 청소 공정으로 인해 ·OH의 농도를 눈에 띄게 낮출 수 있다.[3] 따라서 시스템에서 중탄산염을 제거해야 하며 그렇지 않으면 AOP가 손상된다.
- 대량의 폐수를 처리하기 위해 AOP만을 사용하는 것은 비용 효율적이지 않다. 대신 1차 및 2차 처리로 많은 양의 오염물질을 성공적으로 제거한 후 최종 단계에서 AOP를 배치해야 한다. 또한 AOPs를 생물학적 처리와 결합하여 비용을 낮추기 위한 연구가 진행 중이다.[16]
미래
1987년에 AOPs가 처음 정의된 이후, 그 분야는 이론과 적용 모두에서 급속한 발전을 목격했다. 지금까지, TiO2/UV 시스템, HO22/UV 시스템, 펜톤 시스템, 포토 펜톤 및 전자 펜톤 시스템은 광범위한 조사를 받았다. 그러나, 이러한 기존 AOP에 대한 연구 요구는 여전히 많다.[clarification needed]
최근 트렌드는 효율적이고 경제적인 새로운 수정된 AOP의 개발이다. 사실 건설적인 해결책을 제시하는 연구도 있었다. 예를 들어 비금속 원소를 사용한 도핑 TiO는2 광촉매 활동을 향상시킬 수 있으며 초음파 처리의 구현은 히드록실산기의 생산을 촉진할 수 있다.[17][18] Fluidized-Bed Fenton과 같은 수정된 AOPs는 성능 저하와 경제 측면에서도 큰 잠재력을 보였다.[19]
참고 항목
참조
- ^ a b Glaze, William; Kang, Joon-Wun; Chapin, Douglas H. (1987). "The Chemistry of Water Treatment Processes Involving Ozone, Hydrogen Peroxide and Ultraviolet Radiation". Ozone: Science & Engineering. 9 (4): 335–352. doi:10.1080/01919518708552148.
- ^ National Water Research Institute (2000). Treatment Technologies for Removal of Methyl Tertiary Butyl Ether (MTBE) from Drinking Water: Chapter III Advanced Oxidation Processes.
- ^ a b Munter, Rein (2001). "Advanced Oxidation Processes–Current Status and Prospects". Proceedings of the Estonian Academy of Sciences. Chemistry. 50 (2): 59–80. doi:10.3176/chem.2001.2.01. S2CID 239610363.
- ^ Misra, N.N. (2015). "The contribution of non-thermal and advanced oxidation technologies towards dissipation of pesticide residues". Trends in Food Science & Technology. 45 (2): 229–244. doi:10.1016/j.tifs.2015.06.005.
- ^ Enric Brillasa; Eva Mur; Roser Sauleda; Laura Sànchez; José Peral; Xavier Domènech; Juan Casado (March 1998). "Aniline mineralization by AOP's: anodic oxidation, photocatalysis, electro-Fenton and photoelectro-Fenton processes". Applied Catalysis B: Environmental. 16 (1): 31–42. doi:10.1016/S0926-3373(97)00059-3.
- ^ a b W.T.M. Audenaert; Y. Vermeersch; S.W.H. Van Hulle; P. Dejans; A. Dumouilin; I. Nopens (2011). "Application of a mechanistic UV/hydrogen peroxide model at full-scale: Sensitivity analysis, calibration and performance evaluation". Chemical Engineering Journal. 171 (1): 113–126. doi:10.1016/j.cej.2011.03.071. hdl:1854/LU-1260447.
- ^ Naddeo, Vincenzo; Zarra, Tiziano; Xia, Dongsheng; Cai, Yingjie; Telegin, Felix Y.; Pervez, Md Nahid (2019). "Efficient Degradation of Mordant Blue 9 Using the Fenton-Activated Persulfate System". Water. 11 (12): 2532. doi:10.3390/w11122532. ISSN 2073-4441.
- ^ Mazille, Félicien. "Advanced Oxidation Processes SSWM. Sustainable Sanitation and Water Management". Archived from the original on May 28, 2012. Retrieved June 13, 2012.
- ^ Lee, Brandon Chuan Yee; Lim, Fang Yee; Loh, Wei Hao; Ong, Say Leong; Hu, Jiangyong (January 2021). "Emerging Contaminants: An Overview of Recent Trends for Their Treatment and Management Using Light-Driven Processes". Water. 13 (17): 2340. doi:10.3390/w13172340.
- ^ a b "Light-Based Removal of Emerging Contaminants". encyclopedia.pub. Retrieved November 14, 2021.
- ^ El Mountassir EL MOUCHTARI, Carol ABDEL NOUR, Anne PIRAM, Stéphanie ROSSIGNOL and Pascal WONG-WAH-CHUNG (April 2019). "First results on the purification performance of LaVie system" (PDF). LaVie.CS1 maint: 여러 이름: 작성자 목록(링크)
- ^ a b Beltrán, Fernando J. (2004). Ozone Reaction Kinetics for Water and Wastewater Systems. CRC Press, Florida. ISBN 978-1-56670-629-2.
- ^ Cai, Q. Q.; Jothinathan, L.; Deng, S. H.; Ong, S. L.; Ng, H. Y.; Hu, J. Y. (January 1, 2021), Shah, Maulin P. (ed.), "11 - Fenton- and ozone-based AOP processes for industrial effluent treatment", Advanced Oxidation Processes for Effluent Treatment Plants, Elsevier, pp. 199–254, doi:10.1016/b978-0-12-821011-6.00011-6, ISBN 978-0-12-821011-6, S2CID 224976088, retrieved April 8, 2021
- ^ Solarchem Environmental System (1994). The UV/Oxidation Handbook.
- ^ "Advanced Oxidation Processes". Neopure Technologies. Archived from the original on August 18, 2018. Retrieved March 27, 2016.
- ^ Cai, Q. Q.; Wu, M. Y.; Li, R.; Deng, S. H.; Lee, B. C. Y.; Ong, S. L.; Hu, J. Y. (June 1, 2020). "Potential of combined advanced oxidation – Biological process for cost-effective organic matters removal in reverse osmosis concentrate produced from industrial wastewater reclamation: Screening of AOP pre-treatment technologies". Chemical Engineering Journal. 389: 123419. doi:10.1016/j.cej.2019.123419. ISSN 1385-8947. S2CID 209723537.
- ^ Thompson, Tracy L; Yates, John T (2006). "Surface science studies of the photoactivation of TiO2–new photochemical processes". Chemical Reviews. 106 (10): 4428–4453. doi:10.1021/cr050172k. PMID 17031993.
- ^ Berberidou, C; Poulios I.; Xekoukoulotakis, N. P.; Mantzavinos, D. (2007). "Sonolytic, photocatalytic and sonophotocatalytic degradation of malachite green in aqueous solutions". Applied Catalysis B: Environmental. 74 (1–2): 63–72. doi:10.1016/j.apcatb.2007.01.013.
- ^ Cai, Q. Q.; Lee, B. C. Y.; Ong, S. L.; Hu, J. Y. (February 15, 2021). "Fluidized-bed Fenton technologies for recalcitrant industrial wastewater treatment–Recent advances, challenges and perspective". Water Research. 190: 116692. doi:10.1016/j.watres.2020.116692. ISSN 0043-1354. PMID 33279748. S2CID 227523802.
추가 읽기
- Michael OD Roth: 화학 산화: 90년대를 위한 기술, VI권: 90년대를 위한 기술: 6 (화학 산화) W. Wesley의 코너 필드와 John A. Roth, Technomic Publishing CO, Lancaster 등이 그것이다. 1997, ISBN 1-56676-597-8 (엔젤)
- Oppenländer, Thomas (2003). Advanced Oxidation Processes (AOPs): Principles, Reaction Mechanisms, Reactor Concepts. Wiley VCH, Weinheim. ISBN 978-3-527-30563-6.