S상
S phaseS상(합성상)은 DNA가 복제되는2 세포주기의 상으로 G상과 G상 [1]사이에 발생한다1.게놈의 정확한 복제가 성공적인 세포 분열을 위해 매우 중요하기 때문에, S상 동안 일어나는 과정은 엄격히 조절되고 광범위하게 보존된다.
규정
S상으로의 진입은 G1 제한점(R)에 의해 제어되며, G1 제한점은 적절한 영양소와 성장 [2]신호가 있는 경우 세포 사이클의 나머지 부분에 세포를 커밋한다.이 전환은 본질적으로 되돌릴 수 없다; 제한점을 통과한 후, 환경 조건이 [2]나빠지더라도 세포는 S상을 거치게 된다.
따라서 S상으로의 진입은 세포상태의 단방향 이동을 촉진하는 분자경로에 의해 제어된다.예를 들어 효모에서 세포 성장은 Cln3 사이클린의 축적을 유도하며, 이는 사이클린의존성 키나제 CDK2와 [3]복합된다.Cln3-CDK2 복합체는 전사억제제 Whi5를 [3]비활성화함으로써 S상 유전자의 전사를 촉진한다.S상 유전자의 상향 조절은 Whi5를 더욱 억제하기 때문에, 이 경로는 세포를 S상 유전자 [3]발현에 완전히 커밋하는 양성 피드백 루프를 생성한다.
포유류의 [3]세포에는 놀라울 정도로 유사한 조절 방식이 존재한다.G1상 전체에서 수신된 승모판원 신호는 CDK4/[3]6과 복합하는 사이클린 D의 점진적 축적을 일으킨다.활성 사이클린 D-CDK4/6 복합체는 E2F 전사 인자의 방출을 유도하고, 이는 다시 S상 [3]유전자의 발현을 개시한다.몇몇 E2F 표적 유전자는 [3]E2F의 추가 방출을 촉진하여 효모에서 발견되는 것과 유사한 양의 피드백 루프를 생성한다.
DNA복제
M상 및 G1상 전체에서 세포는 [4]게놈 전체에 분포된 복제 기원에 대해 비활성 사전 복제 복합체(Pre-RC)를 결합한다.S 단계 동안 세포는 사전 RC를 활성 복제 포크로 변환하여 DNA [4]복제를 시작합니다.이 과정은 Cdc7과 다양한 S상 CDK의 키나아제 활성에 의존하며, 둘 다 S상 진입 [4]시 상향 조절된다.
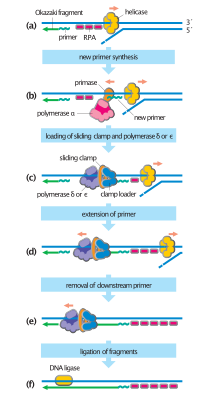
사전 RC의 활성화는 엄격히 규제되고 매우 순차적인 과정이다.Cdc7 및 S상 CDK가 각각의 기질을 인산화한 후, 두 번째 세트의 복제 인자가 [4]RC 이전과 관련된다.안정적인 연관성은 MCM 헬리케이스가 부모의 DNA를 2가닥의 ssDNA로 풀어주도록 장려하고, 이는 다시 ssDNA [4]결합 단백질인 복제 단백질 A(RPA)를 모집한다.RPA 채용은 복제 DNA 중합효소 및 PCNA 슬라이딩 [4]클램프를 장착하기 위한 복제 포크를 준비합니다.이러한 인자의 로딩은 활성 복제 포크를 완료하고 새로운 DNA 합성을 시작합니다.
완전한 레플리케이션 포크 어셈블리와 활성화는 레플리케이션 원본의 작은 서브셋에서만 발생합니다.모든 진핵생물은 DNA [5]복제의 한 주기 동안 엄격하게 필요한 것보다 더 많은 복제 기원을 가지고 있다.중복 기원은 DNA 복제의 유연성을 증가시켜 세포가 DNA 합성 속도를 조절하고 복제 [5]스트레스에 반응할 수 있게 한다.
히스톤 합성
새로운 DNA가 제대로 기능하기 위해서는 뉴클레오솜에 포장되어야 하기 때문에, 정준 히스톤 단백질의 합성은 DNA 복제와 함께 일어난다.초기 S상 동안 사이클린 E-Cdk2 복합체는 히스톤 [6]전사의 핵공활성제인 NPAT를 인산화한다.NPAT는 인산화에 의해 활성화되며, 히스톤 [6]유전자의 촉진자에게 Tip60 염색질 리모델링 복합체를 모집한다.Tip60 활성은 억제성 크로마틴 구조를 제거하고 전사율을 3~[1][6]10배 증가시킨다.
히스톤 유전자의 전사가 증가할 뿐만 아니라, S상 진입은 또한 RNA 수준에서 히스톤 생성을 조절한다.폴리아데닐화된 꼬리 대신, 표준 히스톤 전사체는 보존된 3' 스템 루프 모티브를 가지며, 스템 루프 결합 단백질(SLBP)[7]에 선택적으로 결합한다.SLBP 결합은 히스톤 mRNA의 효율적인 처리, 수출 및 번역을 위해 필요하며, 매우 민감한 생화학적 "스위치"[7]로 기능할 수 있다.S상에서는 NPAT와 함께 SLBP 축적이 작용하여 히스톤 [7]생산 효율을 획기적으로 높인다.그러나 S상이 종료되면 SLBP와 결합 RNA가 모두 빠르게 [8]분해됩니다.이는 히스톤 생산을 즉시 중단시키고 유리 히스톤의 [9]독성 축적을 방지합니다.
뉴클레오솜 복제
S상 동안 세포에 의해 생성된 유리히스톤은 새로운 뉴클레오솜에 빠르게 결합된다.이 프로세스는 레플리케이션의 포크와 밀접하게 관련되어 있어 레플리케이션의 「전면」과 「후면」에서 곧바로 발생합니다.선행 가닥을 따라 MCM 헬리케이스의 전위는 부모 뉴클레오솜 옥타머를 교란시켜 H3-H4 및 H2A-H2B 서브유닛의 [10]방출을 초래한다.복제 포크 뒤에 있는 뉴클레오좀의 재조립은 복제 [4][11]단백질과 느슨하게 관련된 염색질 조립 인자(CAF)에 의해 매개된다.완전히 이해되지는 않았지만 재구성은 DNA [11]복제에서 볼 수 있는 반보수적 방식을 사용하지 않는 것으로 보입니다.라벨링 실험은 뉴클레오솜 복제가 주로 [11][10]보수적이라는 것을 보여준다.부성 H3-H4 핵심 뉴클레오솜은 새로 합성된 H3-H4로부터 완전히 분리된 상태로 유지되며, 결과적으로 독점적으로 오래된 H3-H4 또는 [10][11]독점적으로 새로운 H3-H4를 포함하는 뉴클레오솜을 형성한다. "구" 및 "신" 히스톤은 각 딸 가닥에 반랜덤으로 할당되어 조절의 [10]결과를 초래한다.
염색질 도메인 재정립
분열 직후, 각 딸 염색체들은 부성 [10]염색체 내에 존재하는 후생유전학적 변형의 절반만을 가지고 있다.세포는 유사분열을 시작하기 전에 이 부분적인 명령 세트를 사용하여 기능적인 크로마틴 도메인을 재정립해야 합니다.
큰 게놈 영역의 경우, 오래된 H3-H4 뉴클레오솜의 유전은 염색질 도메인의 [10]정확한 재정립에 충분하다.폴리콤 억제 복합체 2(PRC2) 및 다른 여러 히스톤 변형 복합체는 오래된 히스톤에 존재하는 수정을 새로운 [10]히스톤에 "복사"할 수 있다.이 과정은 후생유전학적 표시를 증폭시키고 뉴클레오솜 [10]복제의 희석 효과를 상쇄한다.
그러나 개별 유전자의 크기에 근접하는 작은 도메인의 경우, 오래된 뉴클레오솜은 히스톤 [10]변형의 정확한 전파를 위해 너무 얇게 퍼져있다.이러한 영역에서 염색질 구조는 아마도 뉴클레오솜 재조립 [10]중에 히스톤 변이체의 통합에 의해 제어될 것이다.H3.3/H2A.Z와 문자 변환 활성 영역 사이에 나타나는 밀접한 상관관계가 이 제안된 [10]메커니즘을 뒷받침합니다.불행히도 인과관계는 아직 [10]증명되지 않았다.
DNA 손상 검사점
S상 동안 세포는 자신의 게놈에 이상이 없는지 지속적으로 검사한다.DNA 손상 검출은 추가적인 세포 [12]주기 진행을 지연 또는 정지시키는 세 가지 표준 S 단계 "체크포인트 경로"의 활성화를 유도한다.
- 복제 체크포인트는 RPA, ATR Interacting Protein(ATRIP) 및 [12]RAD17로부터의 신호를 통합하여 정지된 복제 포크를 검출합니다.활성화 시 복제 체크포인트는 뉴클레오티드 생합성을 상향 조절하고 만료되지 않은 [12]원본으로부터의 복제 시작을 차단합니다.이 두 프로세스 모두 dNTP의 [12]가용성을 높임으로써 정지된 포크를 복구하는 데 도움이 됩니다.
- S-M 체크포인트는 전체 게놈이 성공적으로 [12]복제될 때까지 유사분열을 차단합니다.이 경로는 세포 주기 전체에 걸쳐 점진적으로 축적되어 유사분열 [12]진입을 촉진하는 사이클린-B-CDK1 복합체를 억제함으로써 정지를 유도한다.
- 인트라 S 페이즈체크포인트는 ATR [12]키나아제 및 ATM 키나제를 활성화하여 Double Strand Breaks(DSB; 더블 스트랜드 브레이크)를 검출합니다.활성 ATR 및 ATM은 DNA 수복을 용이하게 할 뿐만 아니라 CDK에서 [12]억제성 인산염 잔류물을 제거하는 포스파타아제인 CDC25A의 분해를 촉진함으로써 세포 순환의 진행을 방해한다.DNA 이중사슬 절단을 복구하는 정확한 과정인 상동재조합은 S상에서는 가장 활발하고 G2/M상에서는 [13]감소하며 G1상에서는 거의 존재하지 않는다.
이러한 표준 체크포인트 외에도, 최근의 증거는 히스톤 공급과 뉴클레오솜 조립의 이상이 S상 [14]진행을 바꿀 수 있다는 것을 암시한다.드로소필라 세포의 유리 히스톤의 고갈은 S상을 극적으로 연장시키고 G2상에서 영구 [14]정지를 일으킨다.이 독특한 체포 표현형은 표준 DNA 손상 경로의 활성화와 관련이 없으며, 뉴클레오솜 조립체와 히스톤 공급이 새로운 S상 체크포인트에 [14]의해 면밀히 조사될 수 있음을 나타낸다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b David M (2007). The cell cycle : principles of control. Oxford University Press. ISBN 978-0199206100. OCLC 813540567.
- ^ a b Pardee AB, Blagosklonny MV (2013). The Restriction Point of the Cell Cycle. Landes Bioscience.
- ^ a b c d e f g Bertoli C, Skotheim JM, de Bruin RA (August 2013). "Control of cell cycle transcription during G1 and S phases". Nature Reviews. Molecular Cell Biology. 14 (8): 518–28. doi:10.1038/nrm3629. PMC 4569015. PMID 23877564.
- ^ a b c d e f g Takeda DY, Dutta A (April 2005). "DNA replication and progression through S phase". Oncogene. 24 (17): 2827–43. doi:10.1038/sj.onc.1208616. PMID 15838518.
- ^ a b Leonard AC, Méchali M (October 2013). "DNA replication origins". Cold Spring Harbor Perspectives in Biology. 5 (10): a010116. doi:10.1101/cshperspect.a010116. PMC 3783049. PMID 23838439.
- ^ a b c DeRan M, Pulvino M, Greene E, Su C, Zhao J (January 2008). "Transcriptional activation of histone genes requires NPAT-dependent recruitment of TRRAP-Tip60 complex to histone promoters during the G1/S phase transition". Molecular and Cellular Biology. 28 (1): 435–47. doi:10.1128/MCB.00607-07. PMC 2223310. PMID 17967892.
- ^ a b c Marzluff WF, Koreski KP (October 2017). "Birth and Death of Histone mRNAs". Trends in Genetics. 33 (10): 745–759. doi:10.1016/j.tig.2017.07.014. PMC 5645032. PMID 28867047.
- ^ Whitfield ML, Zheng LX, Baldwin A, Ohta T, Hurt MM, Marzluff WF (June 2000). "Stem-loop binding protein, the protein that binds the 3' end of histone mRNA, is cell cycle regulated by both translational and posttranslational mechanisms". Molecular and Cellular Biology. 20 (12): 4188–98. doi:10.1128/MCB.20.12.4188-4198.2000. PMC 85788. PMID 10825184.
- ^ Ma Y, Kanakousaki K, Buttitta L (2015). "How the cell cycle impacts chromatin architecture and influences cell fate". Frontiers in Genetics. 6: 19. doi:10.3389/fgene.2015.00019. PMC 4315090. PMID 25691891.
- ^ a b c d e f g h i j k l Ramachandran S, Henikoff S (August 2015). "Replicating Nucleosomes". Science Advances. 1 (7): e1500587. Bibcode:2015SciA....1E0587R. doi:10.1126/sciadv.1500587. PMC 4530793. PMID 26269799.
- ^ a b c d Annunziato AT (April 2005). "Split decision: what happens to nucleosomes during DNA replication?". The Journal of Biological Chemistry. 280 (13): 12065–8. doi:10.1074/jbc.R400039200. PMID 15664979.
- ^ a b c d e f g h Bartek J, Lukas C, Lukas J (October 2004). "Checking on DNA damage in S phase". Nature Reviews. Molecular Cell Biology. 5 (10): 792–804. doi:10.1038/nrm1493. PMID 15459660. S2CID 33560392.
- ^ Mao Z, Bozzella M, Seluanov A, Gorbunova V (September 2008). "DNA repair by nonhomologous end joining and homologous recombination during cell cycle in human cells". Cell Cycle. 7 (18): 2902–6. doi:10.4161/cc.7.18.6679. PMC 2754209. PMID 18769152.
- ^ a b c Günesdogan U, Jäckle H, Herzig A (September 2014). "Histone supply regulates S phase timing and cell cycle progression". eLife. 3: e02443. doi:10.7554/eLife.02443. PMC 4157229. PMID 25205668.