뫼비우스 향기
Möbius aromaticity유기화학에서 뫼비우스 방향성은 다수의 유기 분자에 존재하는 것으로 여겨지는 특별한 형태의 방향성이다.[1][2] 분자 궤도 이론의 관점에서 이 화합물들은 위상 밖으로의 홀수 수가 겹치는 단일 반복적인 분자 궤도 배열을 가지고 있는데, 이는 후켈 계통에 대한 방향족과 비교되는 반대 패턴이다. 리본으로 보는 궤도상의 노달면은 원통형이라기보다는 뫼비우스의 띠라고 해서 붙여진 이름이다. 궤도 에너지의 패턴은 회전된 프로스트 원(정점 대신 폴리곤의 가장자리가 아래에 있음)에 의해 주어지기 때문에 4n 전자가 있는 시스템은 방향성이 있는 반면, 4n + 2 전자가 있는 시스템은 반자동/비자동이다. 비록 4 전자 뫼비우스 방향족 체계의 궤도의 증분 비틀림 특성 때문에, 4 전자 뫼비우스 방향족 전이 상태는 순환성 반응을 위한 데워-짐머만 프레임워크의 맥락에서 잘 알려져 있지만, 안정적인 뫼비우스 방향족 분자는 적어도 8개의 전자를 포함해야 한다. 뫼비우스 분자 체계는 1964년 에드가 헤이클브론너에 의해 후켈법을 적용하여 고려되었으나,[3] 레이너 허지스 그룹에 의해 2003년까지 그러한 최초의 고립성 화합물이 합성되지 않았다.[4] 그러나, 우측에 표시된 덧없는 Trans-CH99+ cation은 계산 및 실험 증거를 바탕으로 1998년에 Möbius 방향족 반응 중간으로 제안되었다.
후켈-뫼비우스 방향성
헤르게스 화합물(아래 이미지에서 6개)은 시클로옥타트라엔의 대체물로 테트라데하이드로디안스라센 1과 라다인 싱트리시클로옥타디엔 2의 여러 광화학 사이클로어드 반응에서 합성되었다.[5]
중간 5는 2개의 이소머와 최종 6개의 이소머가 서로 다른 cis와 트랜스 구성을 가진 5개의 이소머를 혼합한 것이었다. 그 중 하나는 뫼비우스 방향족에 해당하는 C2 분자 대칭성을 가진 것으로 밝혀졌고, 또 다른 후켈 이소머는 Cs 대칭성을 가진 것이 발견되었다. 헤일브론너의 예측은 파이 계통에 16개의 전자가 있음에도 불구하고 (4n의 반자율 화합물로 만들어짐) 뫼비우스 화합물이 방향성을 갖는 것으로 밝혀졌기 때문에 이루어졌다. X선 결정학에서 추론한 결합 길이의 경우, HOMA 값은 0.50(폴리엔 부분만)과 0.35(합성물 전체만)로 얻었으며, 이 값은 적당한 향으로 적합했다.
Henry Rzepa는 중간 5에서 6으로의 전환은 헉켈이나 뫼비우스 전환 상태에 의해 진행될 수 있다고 지적했다.[6]
그 차이는 사이클로데카헥사에 대한 가상의 순환 순환 고리 개방 반응에서 입증되었다. 후켈 TS(왼쪽)는 6개의 전자(화살이 빨간색으로 밀림)를 포함하며, Cs 분자 대칭은 반응 전체에 걸쳐 보존된다. 링 개구부는 탈회 및 초선형이며 본드 길이 교대 및 NICS 값은 모두 6개의 멤브레인 링이 방향성이 있음을 나타낸다. 반면에 8개의 전자를 가진 뫼비우스 TS는 계산된 활성화 에너지가 낮으며, C2 대칭, 콘로터 및 난타성 고리 개방, 8-membed 링 방향성이 특징이다.
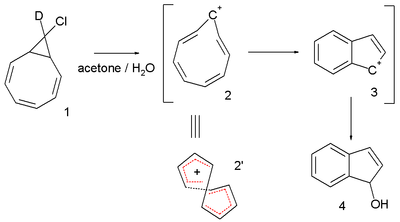
또 다른 흥미로운 시스템은 Paul v. R. Schleyer 등이 30년 넘게 탐험한 사이클로나테트라에닐 양이온이다. 이 반응성 중간은 자전거로 염화 9-데우테로-9'-클로로비시클로[6.1.0]-Nonatriene 1의 인덴 디하이드로인덴놀 4에 대한 용융분해에 내포되어 있다.[7][8] 시작 염화물은 한 위치에서만 체외가 제거되지만 최종 제품에서는 가능한 모든 위치에 체외가 분배된다. 이 관찰은 NICS 값이 -13.4 (보다 뛰어난 벤젠)로 계산되는 비틀린 8전자를 호출하여 설명한다.[9]
2005년에 이 같은 P.vRSchleyer[10]:그와 한나라당이 결합 길이 교대의 큰 영향을 받-0.02의 HOMA 값 -3.4 ppm의 또한 방향성과(또한 컴퓨터 모델에서 유추되)ster을 향해 지적하지 않은 계산된 NICS값을 야기하였다 결론을 내렸다 같은 결정 학적인 자료를 분석했다 2003년 Herges 주장에 의문을 제기했다.ic s기차는 효과적인 파이-파이의 중복을 막을 것이다.
후켈-뫼비우스 방향족 스위치(2007)는 28개의 전자 포르피린 시스템에 기초하여 설명되었다.[11][12]
이 분자의 페닐렌 링은 뫼비우스의 반반으로 된 것과 대략 동일한 에너지의 헉켈 이중 반반(그림 8 구성)으로 이루어진 것 등 일련의 컨포머를 형성하여 자유롭게 회전할 수 있다.
2014년 주와 샤아(슐레이어의 도움으로)는 오스뮴 원자와 연결된 두 개의 펜틴 고리로 구성된 평면 뫼비우스 시스템을 합성했다.[13] 그들은 오스뮴이 16, 18개의 전자를 갖는 파생상품을 만들어내고 크레이그-뫼비우스 방향성이 금속의 전자수보다 분자의 안정화를 위해 더 중요하다고 판단했다.
전환 상태
뫼비우스 방향족 상태 분자 체계의 희귀성과는 대조적으로 뫼비우스 방향족성을 나타내는 순환 전환 상태의 예는 많다. 뫼비우스 또는 후켈 위상 중 하나로 순환 전환 상태를 분류하면 전환 상태를 방향 또는 반자동으로 만들기 위해 4N 또는 4N + 2 전자가 필요한지 여부를 결정하므로 각각 허용 또는 금지된다. 후켈 MO 이론에서 도출된 에너지 수준 다이어그램을 바탕으로 (4N + 2) 전자 후켈과 (4N) 전자 뫼비우스 전환 상태는 방향성이 있고 허용되며, (4N + 2) 전자 뫼비우스와 (4N) 후켈 전환 상태는 반자율적이며 금지된다. 이것이 뫼비우스-후켈 개념의 기본 전제다.[14][15]
뫼비우스 위상에 대한 후켈 MO 이론 에너지 수준의 도출
위의 그림에서 두 연속 AO는 }에 의해 궤도 사이의 증분 비틀림에 의해 감쇠됨을 알 수 있다 여기서 = / 은 연속된 궤도 사이의 비틀림각이다. 일반적인 후켈 시스템과 비교했을 때 이러한 이유로 공진 적분 {\은(는) 다음과 같이 주어진다.
- = (/ )
여기서 은(는) 표준 Hukel 공명 적분 값(완전히 평행한 궤도 포함)이다. 그럼에도 불구하고 끝까지 돌고 나니 nth와 1차 궤도는 거의 완전히 위상을 벗어났다. ( 의 궤도 이후에도 비틀림이 계속된다면(+ ) ) st 궤도 는 1차 궤도와 비교했을 때 정확히 위상역전일 것이다. 이러한 이유로 후켈 매트릭스에서 탄소 과( N {\ 사이의 공진 적분은 - -}이다
일반 탄소 뫼비우스 시스템의 경우 해밀턴 H 는) 다음과 같다.
- H);0&, \cdots;\cdots &-\beta '\\\beta '&, \alpha&\beta '& &, 0\\0&\alpha&\cdots &, 0\\\vd{\displaystyle \mathbf{H}={\begin{pmatrix}\alpha&\beta '&\beta '&(α β ′ 0⋯ − β ′ β ′ α β ′ ⋯ 00β′ α ⋯ 0⋮ ⋮ ⋮ ⋱ ⋮ − β ′ 00⋯ α).Ots&\vdots, \vdots &, \ddots & &, \vdots \\-\bet. &\
이 행렬에 대한 고유값은 이제 뫼비우스 계통의 에너지 수준에 해당하는 것을 찾을 수 있다. 은(는) N N이므로 N 고유값 k E_{및 MOs. 변수 정의
- = - E
다음이 있음:
- ()k10⋯)k1⋯ 001)k⋯ 0⋮ ⋮ ⋮ ⋱ ⋮ − 100⋯)k11−)⋅(c1(k)c2(k)c3(k)⋮ c N(k))=0{\displaystyle{\begin{pmatrix}x_{k}&, 1&, 0&, \cdots &, -1\\1&, x_{k}&, 1&, \cdots &a.융점, 0\\0&, 1&, x_{k}&, \cdots &, 0\.
이 방정식에 대한 비경쟁적 해결책을 찾기 위해, 우리는 이 행렬의 결정 인자를 0으로 설정하여 얻는다.
- =- ( + 1)
따라서, 우리는 뫼비우스의 위상이 있는 순환계통의 에너지 수준을 발견한다.
- .
이와는 대조적으로, Hukel 위상이 있는 순환 시스템의 에너지 레벨을 회수한다.
- .
참고 항목
참조
- ^ Rzepa, Henry S. (2005). "Möbius Aromaticity and Delocalization". Chem. Rev. 105 (10): 3697–3715. doi:10.1021/cr030092l.
- ^ Seok Yoon, Zin; Osuka, Atsuhiro; Kim, Dongho (2009). "Möbius aromaticity and antiaromaticity in expanded porphyrins". Nature Chemistry. 1: 113–122. doi:10.1038/nchem.172.
- ^ Heilbronner, E. (1964). "Hückel molecular orbitals of Möbius-type conformations of annulenes". Tetrahedron Letters. 5 (29): 1923–1928. doi:10.1016/S0040-4039(01)89474-0.
- ^ Ajami, D.; Oeckler, O.; Simon, A.; Herges, R. (December 2003). "Synthesis of a Möbius aromatic hydrocarbon". Nature. 426: 819–821. doi:10.1038/nature02224. PMID 14685233.
- ^ 뫼비우스 링은 1과 COT 사이의 공식적인 올레핀 메타텍스 반응으로 형성된다는 점에 유의하십시오.
- ^ 주기적 반응의 방향성 변화 상태 Henry S. Rzepa J. 화학. 교육. 2007, 84, 1535. 추상적
- ^ Paul; Schleyer, R. (1971). "Thermal bicyclo[6.1.0]nonatrienyl chloride-dihydroindenyl chloride rearrangement". Journal of the American Chemical Society. 93: 279–281. doi:10.1021/ja00730a063.
- ^ Herges, Rainer (2006). "Topology in Chemistry: Designing Möbius Molecules †". Chemical Reviews. 106: 4820–4842. doi:10.1021/cr0505425.
- ^ 모노시클릭 (CH)9+ - 헤이얼브론너 뫼비우스 방향제 공개 안젤완테 뫼비우스 국제판 37권, 17호, 날짜: 1998년 9월 18일, 페이지: 2395-2397 마이클 모우크슈, 발렌틴 고게나, 하이준 자오, 폴 폰 라게르
- ^ Castro, Claire (2005). "Investigation of a Putative Möbius Aromatic Hydrocarbon. The Effect of Benzannelation on Möbius [4 n ]Annulene Aromaticity". Journal of the American Chemical Society. 127: 2425–2432. doi:10.1021/ja0458165.
- ^ Stępień, Marcin (2007). "Expanded Porphyrin with a Split Personality: A Hückel–Möbius Aromaticity Switch". Angewandte Chemie International Edition. 46: 7869–7873. doi:10.1002/anie.200700555.
- ^ 시약: 피롤, 벤츠알데히드, 붕소 3불화화, DDQ를 사용한 후속 산화, Ph = 페닐 메스 = mbainel
- ^ Zhu, Congqing; Ming Luo; Qin Zhu; Jun Zhu; Paul v. R. Schleyer; Judy I-Chia Wu; Xin Lu; Haiping Xia (25 February 2014). "Planar Möbius aromatic pentalenes incorporating 16 and 18 valence electron osmiums". Nature Communications. 5: 3265. Bibcode:2014NatCo...5E3265Z. doi:10.1038/ncomms4265. PMID 24567039.
- ^ Zimmerman, H. E (1966). "On Molecular Orbital Correlation Diagrams, the Occurrence of Möbius Systems in Cyclization Reactions, and Factors Controlling Ground and Excited State Reactions. I". J. Am. Chem. Soc. 88: 1564–1565. doi:10.1021/ja00959a052.
- ^ Zimmerman, H. E (1966). "On Molecular Orbital Correlation Diagrams, Möbius Systems, and Factors Controlling Ground and Excited State Reactions. II". J. Am. Chem. Soc. 88: 1566–1567. doi:10.1021/ja00959a053.








 연속된 궤도 사이의 비틀림각이다. 일반적인 후켈 시스템과 비교했을 때 이러한 이유로 공진 적분
연속된 궤도 사이의 비틀림각이다. 일반적인 후켈 시스템과 비교했을 때 이러한 이유로 공진 적분  (는) 다음과 같이 주어진다.
(는) 다음과 같이 주어진다. 
 (는) 표준 Hukel 공명 적분 값(완전히 평행한 궤도 포함)이다. 그럼에도 불구하고 끝까지 돌고 나니 nth와 1차 궤도는 거의 완전히 위상을 벗어났다. (
(는) 표준 Hukel 공명 적분 값(완전히 평행한 궤도 포함)이다. 그럼에도 불구하고 끝까지 돌고 나니 nth와 1차 궤도는 거의 완전히 위상을 벗어났다. ( 궤도 이후에도 비틀림이 계속된다면
궤도 이후에도 비틀림이 계속된다면
 (
(


 N
N 










