황반변성
Macular degeneration| 황반변성 | |
|---|---|
| 기타 이름 | 노화에 따른 황반변성 |
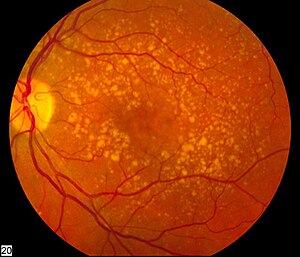 | |
| 노화로 인한 중간 황반변성을 나타내는 안구 뒷면 사진 | |
| 전문 | 안과, 검안 |
| 증상 | 시야[1] 중앙에 흐릿하거나 시야가 없는 경우 |
| 합병증 | 환각[1] |
| 통상적인 개시 | 고령자[1] |
| 종류들 | 얼리, 중급, 레이트[1] |
| 원인들 | 망막[1] 황반 손상 |
| 위험요소 | 유전학, 흡연[1] |
| 진단 방법 | 시력 검사[1] |
| 예방 | 운동, 식사, 금연[1] |
| 치료 | 항VEGF제 눈 주입, 레이저 응고, 광역학적[1] 치료 |
| 빈도수. | 2020년[2] 전 세계 8.7%의 보급률 |
황반변성은 노화 관련 황반변성(AMD 또는 ARMD)으로도 알려져 있으며 시야 [1]중앙에서 시야가 흐릿해지거나 보이지 않을 수 있는 의학적 질환이다.초기에는 증상이 [1]없는 경우가 많습니다.그러나 시간이 지나면서 일부 사람들은 한쪽 [1]눈이나 양쪽 눈에 영향을 미칠 수 있는 시력이 점차적으로 나빠지는 것을 경험한다.시력이 완전히 실명하는 것은 아니지만, 중심 시력의 상실은 얼굴을 인식하거나 운전을 하거나 읽거나 [1]일상생활의 다른 활동을 수행하는 것을 어렵게 만들 수 있다.시각 환각도 일어날 수 있지만 정신질환을 [1]나타내는 것은 아니다.
황반변성은 일반적으로 [1]노인에게서 발생한다.유전적 요인이나 흡연도 [1]한몫한다.망막 [1]황반 손상 때문입니다.진단은 시력 검사를 [1]통해 이루어집니다.중대도는 얼리,[1] 중간 및 레이트타입으로 나뉩니다.후기형은 추가로 "건조"와 "습식"으로 나뉘며 건식 형태는 [1][3]케이스의 90%를 차지한다.
두 형태의 차이는 황반변화이다.마른 형태의 AMD를 가진 사람들은 황반 안에 점차적으로 빛에 민감한 세포를 손상시키고 시력 감퇴를 초래하는 드루젠 세포 부스러기를 가지고 있다.습한 형태의 AMD에서 혈관은 황반 아래에서 자라며, 혈액과 액체가 [4]망막으로 새어나오게 한다.
예방에는 운동, 식사, 금연 등이 포함됩니다.[1]이미 잃어버린 [1]시력을 회복하는 치료법이나 치료법은 없다.습식 상태에서는 눈에 주입되거나 레이저 응고 또는 광역학적 치료가 더디게 [1]악화될 수 있습니다.항산화 비타민과 미네랄은 [5]예방에 도움이 되지 않는 것으로 보인다.하지만, 영양 보조 식품은 이미 그 [6]병에 걸린 사람들의 진행을 늦출 수 있다.
노화로 인한 황반변성은 전 [7]세계 근로 연령 인구의 중심 실명의 주요 원인이다.2020년 현재 전 세계 1억 9천만 명 이상이 영향을 받고 있으며 인구 [2]중 노인 비율이 증가함에 따라 2040년에는 2억 8백만 명으로 증가할 것으로 예상된다.그것은 남성과 여성 모두에게 똑같이 나타나고 유럽이나 북미의 [2]조상들에게서 더 흔하다.2013년에는 백내장,[8] 조산, 녹내장에 이어 네 번째로 흔한 실명 원인이었다.그것은 50세 이상의 사람들에게서 가장 흔하게 발생하며 미국에서는 이 연령대에서 [1][3]시력 감퇴의 가장 흔한 원인이다.50세에서 60세 사이의 사람들 중 약 0.4%가 이 병을 앓고 있는 반면, 60세에서 70세 사이의 사람들 중 0.7%, 70세에서 80세 [3]사이의 사람들 중 2.3%, 그리고 거의 12%가 이 병을 앓고 있다.
징후 및 증상

초기 또는 중간 AMD는 증상이 없거나 한쪽 또는 양쪽 눈에 흐릿하거나 시력이 저하될 수 있습니다.이는 처음에는 읽기 또는 주행에 어려움을 겪을 수 있습니다(특히 조명이 약한 영역).[2]AMD의 다른 증상으로는 시야의 왜곡이나 사각지대(특히 중앙 시야 [2]주변)가 있습니다.
황반 변성의 다른 징후와 증상은 다음과 같습니다.
- 직선의 그리드가 물결처럼 보이고 그리드의 일부가 공백으로 보이는 변형증 형태의 왜곡된 시력: 환자들은 종종 자신의 집에 있는 미니블라인드나 운전 중 전신주 같은 것을 볼 때 이것을 처음 알아차립니다.또한 중심 기미, 그림자 또는 시야 누락 영역이 있을 수 있습니다.
- 밝은 빛에 노출된 후 시각 기능의 회복이 느리다(사진스트레스 테스트)
- 시력이 급격히 저하된다(2단계 이상). 예: 20/20 ~ 20/80
- 흐릿한 시야:비삼출성 황반 변성이 있는 사람은 증상이 없거나 중심 시력의 점진적인 상실을 볼 수 있는 반면, 삼출성 황반 변성이 있는 사람은 종종 시력 상실의 빠른 시작을 볼 수 있다(흔히 비정상적인 혈관의 누출과 출혈로 인해 발생).
- 색상, 특히 어두운 색에서는 어두운 색, 밝은 색에서는 밝은 색을 구별하는 데 어려움이 있습니다.
- 콘트라스트 감도의 손실
- 형성된 시각적 환각과 섬광은 습윤 AMD에 의한 심각한 시각적 손실과도 관련되어 있습니다.
황반변성 자체는 완전한 실명으로 이어지지 않는다.그런 점에서 시각장애인은 극소수에 불과하다.거의 모든 경우에, 일부 시력은 남아있고, 주로 말초적인 것이다.다른 복잡한 조건은 이러한 급성 상태(심각한 뇌졸중 또는 외상, 치료되지 않은 녹내장 등)를 초래할 수 있지만, 황반변성 환자는 거의 시력을 완전히 [11]상실하지 않는다.
황반 부위는 망막의 약 2.1%만 구성되며 나머지 97.9%(말초 영역)는 이 질환의 영향을 받지 않는다.비록 황반이 시야의 작은 부분을 제공하지만, 시각 피질의 거의 절반은 황반 [12]정보를 처리하는 데 할애된다.
또한 건조한 황반변성 환자는 증상이 없지만 한쪽 눈이나 양쪽 [13][14]눈에서 서서히 흐릿한 시력이 나타날 수 있다.습식 황반 변성이 있는 사람들은 시각 [13][14]증상의 급성 시작을 경험할 수 있다.
위험요소
주요 위험 요소는 나이, 흡연,[15] 가족력이다.고령화는 AMD의 가장 강력한 예측 변수이며,[16] 특히 50세 이상입니다.
환경과 라이프스타일
- 흡연:담배를 피우는 것은 담배를 피우지 않은 사람에 비해 AMD의 위험을 2~3배 증가시키며, AMD의 예방에 가장 중요한 수정 가능한 요소일 수 있습니다.이전 연구들을 검토한 결과, "현재 흡연과 AMD 사이의 강한 연관성"이 발견되었습니다.담배를 피우면 [17]망막에 독성이 생길 수 있다고 말했다.
- 고혈압(고혈압):ALIENOR 연구 2013에서 초기 및 후기 AMD는 수축기 또는 확장기 혈압(BP), 고혈압 또는 항고혈압 약물의 사용과 유의하게 관련되지 않았지만, 상승된 맥박[PP) 수축기 BP - 확장기 BP]은 [18]후기 AMD의 위험 증가와 유의하게 관련되었다.
- 아테롬성 동맥경화증[19]
- 높은 콜레스테롤:높은 콜레스테롤은 AMD의 위험을[20][21] 증가시킬 수 있습니다.
- 비만: 복부 비만은 특히 남성들 사이에서[22] 위험 요소이다.
- 지방 섭취:포화 지방, 트랜스 지방, 그리고 오메가 6 지방산을 포함한 많은 양의 특정 지방을 섭취하는 것은 AMD에 기여할 가능성이 있는 반면, 단일 불포화 지방은 잠재적으로 [23]보호됩니다.특히, 오메가3 지방산은 [24]AMD의 위험을 낮출 수 있습니다.
- 햇빛의 자외선에 노출되는 것은 다른 [14][25]원인들보다 증거가 약하지만 AMD에 걸릴 위험이 증가하는 것과 관련이 있을 수 있습니다.
- 디지털 화면은 사람의 눈에 해로운 에너지를 방출하지 않지만, 정지하지 않고 장시간 화면을 응시하는 것은 눈의 피로를 증가시킨다.디지털 화면 노출이 황반 [25][14][26]변성의 위험에 기여한다는 주장을 뒷받침하는 증거는 없다.
유전학
AMD는 매우 유전적인 상태입니다.[15]영향을 받은 개인의 형제자매에 대한 재발 비율은 일반 [27]모집단보다 3배에서 6배 높다.유전자 연계 분석은 다른 염색체(1, 6 및 10)의 3개 위치에서 [28]최소 50%의 위험을 설명하는 5개 유전자 변형을 확인했다.이 유전자들은 면역 반응, 염증 과정, 망막의 항상성을 조절하는 역할을 한다.이러한 유전자의 변이들은 이러한 과정에서 다른 종류의 기능 장애를 일으킨다.시간이 지남에 따라, 이것은 세포내 및 세포외 대사 부스러기의 축적을 초래한다.이것은 망막의 흉터나 혈관 형성 장애를 일으킬 수 있다.
AMD와 관련된 유전자 변이의 목록은 보체 인자, 아폴리포단백질 E, 섬유아세포 성장 인자 2, DNA 절제 복구 단백질 및 노화 관련 황반증 감수성 단백질 [29]2를 포함한다.
비록 유전자 검사가 AMD에 걸리기 쉬운 유전자 변이의 식별으로 이어질 수 있지만, 이 질환의 복잡한 병인은 이러한 테스트를 [15]일상적으로 사용하는 것을 방해한다.그럼에도 불구하고 임상시험을 위한 환자를 선택하고 [15]치료에 대한 반응을 분석하는 데 유용할 수 있다.확인된 유전자 변형이 발견되는 세 가지 위치는 다음과 같다.
- 1q31.3의[30] 1번 염색체 상보인자 H(CFH)
- 10q26[28] 위치에서 10번 염색체의 HTRA 세린펩티다아제 1/나이 관련 황반증 감수성 2(HTRA1/ARMS2)
- 6p21.3의 6번 염색체 상보인자 B/보완성성분 2(CFB/CC2)
특정 유전자
- 보체 시스템 단백질에 대한 유전자의 다형성:상보계 단백질 인자 H(CFH), 인자 B(CFB) 및 인자 3(C3)에 대한 유전자 변화는 특히 [15]사람의 AMD 발병 위험과 강하게 관련되어 있으며 CFH는 염증 [15]반응을 억제하는 데 관여한다.CFH(Y402H)의 돌연변이는 단백질이 망막과 같은 조직을 국소화하고 보완적 [15]과잉활성으로부터 보호하는 능력을 감소시킨다.보체인자 H 관련 유전자 R3 및 R1의 부재는 [31][32]AMD에 대한 보호를 한다.2007년 두 개의 독립적인 연구에서 보체계의 중심 단백질인 C3 유전자의 특정 공통 돌연변이 Arg80Gly가 [33][34]AMD의 발생과 강하게 관련되어 있는 것으로 나타났다.두 논문의 저자는 이들의 연구가 이 질병의 병인에 대한 보완 경로의 영향을 강조하는 것으로 간주한다.
- 2006년의 두 연구에서, HTRA1이라고 불리는 질병에 관련된 또 다른 유전자가 확인되었다.[35][36]
- 유전자 SERPING1(Serpin 펩티드가수분해효소 억제제, Clade G(C1 억제제), Member 1)의 6개의 돌연변이가 AMD와 관련되어 있으며, 이 유전자의 돌연변이도 유전성 혈관부종을 [37]일으킬 수 있다.
- Fibulin-5 돌연변이: 희귀한 형태의 질병은 상염색체 우성적인 방법으로 Fibulin-5의 유전적 결함으로 인해 발생한다.2004년 스톤 외 연구진은 402명의 AMD 환자를 대상으로 검사를 실시하여 피블린-5의 돌연변이와 발병률 사이에 통계적으로 유의한 상관관계가 있음을 밝혔다.
- MT-ND2 분자와 같은 미토콘드리아 관련 유전자 다형성은 습윤 AMD를 [38][39]예측한다.
병태생리학
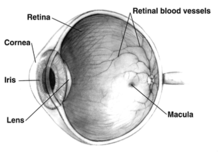
노화와 관련된 황반변성의 병인은 잘 알려져 있지 않지만 산화 스트레스, 미토콘드리아 기능 장애, 염증 과정을 포함한 몇몇 이론들이 제시되었다.
손상된 세포 성분의 생산과 분해 사이의 불균형은 예를 들어 세포 내 리포푸신 및 세포 외 드루젠과 같은 유해 산물의 축적을 초래한다.초기위축은 AMD 초기 지리적 위축에 선행하는 망막색소상피(RPE)의 얇음 또는 탈색 부위로 구분된다.AMD의 고도단계에서는 RPE(지리적 위축)의 위축 및/또는 광수용체와 중심시력의 죽음을 초래하는 새로운 혈관 발달(혈관화)이 일어난다.손실.
건조(불침습) 형태에서, 드루젠은 망막과 맥락막 사이에 축적되어 망막에 위축과 흉터를 일으킨다.더 심한 습식(삼출물) 형태에서는, 혈관이 망막 뒤에 있는 맥락막(신경혈관화)에서 자라나 삼출액과 액체가 누출될 수 있고 출혈도 일으킬 수 있다.
초기 연구는 드루젠에 [40]면역 매개자 가족이 많다는 것을 증명했다.보체인자 H(CFH)는 이 염증 캐스케이드의 중요한 억제제이며 CFH 유전자의 질병 관련 다형성은 [15][41][42][43][44][45]AMD와 강하게 관련된다.따라서 황반에서 만성적으로 낮은 등급의 보균 활성화와 염증의 AMD 병태생리학 모델이 [46][47]발전했다.이에 대한 신뢰성을 부여하는 것은 보체 성분 3(C3)[33]을 포함한 보체 캐스케이드의 다른 요소에서 질병과 관련된 유전자 다형성이 발견되었기 때문이다.
AMD의 강력한 예측 변수는 LOC 387715의 10q26 염색체에서 발견됩니다.이 부위의 삽입/삭제 다형성은 폴리아데닐화 [48]신호의 결실을 통해 ARM2 유전자의 mRNA의 불안정화를 통해 ARM2 유전자의 발현을 감소시킨다.ARM2 단백질은 미토콘드리아에 국소화되어 에너지 대사에 참여할 수 있지만, 그 기능에 대해서는 아직 많이 밝혀져야 한다.
진행위험의 다른 유전자 지표는 AMD [49]진행에서 세포외 매트릭스 대사의 역할을 시사하는 금속단백질분해효소3(TIMP3)의 조직 억제제를 포함한다.간리파아제, 콜레스테롤에스테르전달효소, 리포단백질리파아제 및 ATP결합 카세트 A1과 같은 콜레스테롤 대사 유전자의 변화는 질병 진행과 관련이 있다.질병의 초기 스티그마타인 드루젠은 콜레스테롤이 풍부하여 게놈 전체의 연관성 [50]연구 결과에 얼굴 유효성을 제공합니다.
스테이지
AMD에서는 망막 색소 상피와 기저 맥락막 사이의 황반(망막의 일부)에 드루젠이라고 불리는 특징적인 노란색 퇴적물이 점진적으로 축적됩니다.이 축적은 시간이 지남에 따라 망막을 손상시키는 것으로 여겨진다.알츠하이머병의 뇌에 축적되는 아밀로이드 베타는 AMD에 축적되는 단백질 중 하나이며, 이것이 AMD가 때때로 "눈의 알즈하이머"[51] 또는 "망막의 알즈하이머"로 불리는 이유이다.AMD는 드루젠의 [1]범위(크기 및 수)에 따라 얼리, 중급, 레이트의 3단계로 나눌 수 있습니다.
AMD와 유사한 병리학은 망막 색소 상피와 기저 맥락막 사이의 황반에서 작은 노란색 퇴적물(드루젠)에서 시작됩니다.이러한 초기 변화를 가진 대부분의 사람들은 여전히 좋은 시력을 가지고 있다.드루젠을 가진 사람들은 AMD에 걸릴 수도 있고 그렇지 않을 수도 있다. 사실, 60세 이상의 대부분의 사람들은 부작용 없이 드루젠을 앓고 있다.드루젠이 크고 수가 많고 황반 아래의 색소 세포층의 교란과 관련이 있을 때 증상이 발생할 위험이 더 높습니다.크고 부드러운 드루젠은 콜레스테롤 침전물의 증가와 관련이 있는 것으로 생각된다.
초기 AMD
초기 AMD는 보통 사람 머리카락의 너비 정도인 중간 크기 드루젠의 존재에 기초하여 진단됩니다.초기 AMD는 보통 [1]증상이 없습니다.
중급 AMD
중간 AMD는 큰 드루젠 및/또는 망막 색소 이상에 의해 진단된다.중간 AMD는 시력 감퇴를 일으킬 수 있지만 초기 AMD와 마찬가지로 대개 [1][52]증상이 없습니다.
최근 중간 AMD의 하위 그룹이 식별되었으며, 이러한 하위 그룹은 후기 AMD로 진행될 위험이 매우 높습니다.(정확한 정의에 따라) 이 하위 그룹을 초기 GA 및/또는 iRORA(불완전한 망막 색소 상피 및 외부 망막 위축)[53][54]라고 한다.중간 AMD의 이러한 '고위험' 하위 그룹은 환자에게 예후를 알리는 데 사용될 수 있습니다.또한 이것들은 임상시험에 엔드 포인트로 적용될 수 있다.
후기 AMD
후기 AMD에서는 충분한 망막 손상이 발생하여 드루젠 외에도 사람들은 증상적인 중심 시력 상실을 경험하기 시작합니다.그 손상은 위축의 진행이나 혈관신질환의 발병일 수 있다.후기 AMD는 손상의 유형에 따라 다음 두 가지 하위 유형으로 나뉩니다.지리적 위축과 습윤 AMD(Neovacular [52][1]AMD라고도 함).
드라이 AMD
드라이 AMD(비소재형 AMD라고도 함)는 혈관 외(습식 AMD) 모든 형태의 AMD를 포괄하는 광범위한 명칭입니다.여기에는 AMD의 초기 및 중간 형태와 지리적 위축으로 알려진 건조 AMD의 고급 형태가 포함됩니다.건조한 AMD 환자들은 초기 단계에서 최소한의 증상을 보이는 경향이 있다.; 그 상태가 지리적 위축으로 진행되면 시각 기능 상실이 더 자주 발생한다.건식 AMD는 케이스의 80~90%를 차지하며 진행이 더딘 경향이 있습니다.10~20%의 사람에게서 건조 AMD가 습식 상태로 진행됩니다.
지리적 위축
지리적 위축(위축성 AMD라고도 함)은 망막 세포의 점진적이고 돌이킬 수 없는 손실이 시각 기능의 상실로 이어지는 AMD의 발전된 형태입니다.망막을 구성하는 여러 층이 있고, 지리적 위축에는 위축을 겪는 세 가지 특정한 층이 있습니다: 맥락막, 망막 색소 상피, 그리고 위에 있는 광수용체입니다.
지리적으로 위축된 세 층은 모두 서로 인접해 있다.광수용체는 가장 표면적이고 외부로부터 오는 빛으로부터 에너지를 뇌로 보내는 전기 신호로 변환하는 역할을 하는 세포입니다.망막 색소 상피에는 몇 가지 기능이 있다.망막 색소 상피의 주요 기능 중 하나는 산화 스트레스를 최소화하는 것이다.그것은 빛을 흡수함으로써 빛을 밑층에 도달하는 것을 막음으로써 그렇게 한다.망막 색소 상피 밑에 있는 층들은 매우 혈관화되어 있어서 매우 높은 산소 장력을 가지고 있다.따라서 빛이 이러한 층에 도달하면 많은 활성산기가 형성되어 주변 조직에 손상을 입힐 수 있다.지리적으로 위축된 가장 깊은 층은 choriocapilaris라고 불린다.망막 색소 상피에 영양분을 공급하는 모세관 네트워크입니다.
지리적 위축의 병태생리학은 아직 불확실하다.일부 연구는 이것이 망막 색소 상피 결핍으로 인한 것이 아닌지 의문을 제기했고,[55] 이는 산화 스트레스 증가를 이끌었다.다른 연구들은 [56]손상의 염증적인 원인을 찾아냈다.아직까지는 의학계가 확실치 않다.최근의 연구들은 각 층을 개별적으로 보기 시작했다.그들은 Choriocapillaris의 혈류 감소가 망막 색소 상피와 그 위에 있는 광수용체의 [57]위축에 선행한다는 것을 발견했다.맥락막(choriocapillaris)은 혈관층이기 때문에, 이것은 왜 지리적 위축이 혈류 감소로 인한 질병일 수 있는지에 대한 논쟁으로 사용될 수 있다.
습식 AMD
이나 삼출성Neovascular AMD고급 AMD의" 젖은"형태, 브루흐의 막을 통하여 시력 손실 비정상적인 혈관 성장(맥락막의. 신혈관 형성)에 맥락막 모세 혈관층 때문에 원인이 됩니다.보통, 항상 그런 것은 아니지만 AMD의 건조한 형태에 의해 선행된다.망막에 이상 혈관의 확산 혈관 내피 성장 인자(VEGF)에 의해. 왜냐하면 이러한 혈관 이상, 이 또 궁극적으로 흑점 아래에 혈액과 단백질 누출로 이어진다 전형적인 혈관보다 허약한 자극이 된다.새 거고 이런 혈관들에서 흉터 출혈 결국 광수용체에 돌이킬 수 없는 피해와 빠른 시력 손실 치료하지 않고 내버려두면을 일으킨다.
산화응력
망막색소상피(RPE)의 리소좀 내에 저분자량 광독성 프로옥시던트 멜라닌 올리고머의 노화 관련 축적은 RPE – 자가흡입에 의한 광수용체 외측봉 세그먼트(POS)의 소화 속도를 감소시키는 데 부분적으로 책임이 있을 수 있다.POS의 소화 속도 감소는 [58][59]AMD와 관련된 전형적인 징후인 리포푸신 형성과 관련이 있는 것으로 나타났습니다.
황반에 염증이 더 생기게 함으로써 AMD의 원인에서 망막 산화 스트레스의 역할은 흡연자와 자외선 [17][60][61]조사에 노출된 사람들의 질병 비율의 증가에 의해 제시된다.
미토콘드리아 기능장애가 [62]한 역할을 할 수 있다.최근[63] 미토콘드리아 DNA에 대한 손상이 AMD 병인의 필수 요소일 수 있고 활성산소 종의 과잉생산이 이 과정에서 한 역할을 할 수 있다는 증거가 검토되었다.
진단.
노화와 관련된 황반변성의 진단은 반드시 [64]시력이 아니라 황반 내 징후에 따라 달라진다.AMD의 조기 진단은 추가적인 시력 저하를 방지하고 잠재적으로 [64]시력을 향상시킬 수 있습니다.
건조(또는 초기) AMD 진단에는 다음과 같은 임상 검사와 절차 및 테스트가 포함될 수 있습니다.
- 건조에서 습기로의 이행은 빠르게 일어날 수 있으며, 이를 방치할 경우 불과 6개월 안에 법적 실명으로 이어질 수 있습니다.이러한 현상이 발생하는 것을 방지하고 질병 프로세스 초기에 예방 전략을 시작하기 위해 암적응 테스트를 수행할 수 있습니다.암적응계는 임상적으로 [65]분명한 것보다 최소 3년 일찍 잠재의식 AMD를 검출할 수 있다.
- 콘트라스트 감도가 저하되어 윤곽선, 그림자 및 색각이 선명하지 않습니다.조영 감도의 손실은 집에서 또는 안과 전문의에 의해 수행되는 Pelli Robson과 같은 조영 감도 테스트를 통해 빠르고 쉽게 측정할 수 있습니다.
- Amsler 그리드를 표시할 때 일부 직선은 물결 모양으로 표시되고 일부 패치는 공백으로 표시됩니다.
- Snellen 관리도를 볼 때 두 줄 이상의 줄이 감소합니다.
- AMD 사례의 85-90%에서 발생하는 건성 황반 변성의 경우 안저 촬영에서 드루젠 반점을 볼 수 있습니다.
- 전자망막도 검사로 정상 눈에 비해 황반에서 반응이 약하거나 없는 점이 발견될 수 있습니다
- Farnsworth-Munsell 100 색상 테스트 및 색채 민감도 평가를 위한 최대 색상 대비 민감도 테스트(MCCS)
- 광학적 일관성 단층촬영은 현재 대부분의 안과 의사들이 항혈관신생 약물에 대한 치료에 대한 반응의 진단과 후속 평가에 사용합니다.
습식(또는 후기) AMD 진단에는 위의 테스트 외에 다음 사항이 포함될 수 있습니다.
- 우선적인 과민성 주변측정법 변화(습식 AMD의 경우).우선적인 과민성 주변측정법은 시력의 급격한 변화를 감지하는 테스트로, 왜곡된 점 패턴으로 황반을 자극하고 이것이 [66]시야에서 발생하는 위치를 식별하는 것을 포함합니다.
- 습식 황반 변성의 경우 혈관조영술은 황반 뒤쪽의 혈류 누출을 시각화할 수 있습니다.플루오레세인 혈관조영술은 비정상적인 혈관과정을 식별하고 국소화할 수 있도록 합니다.
조직학
- 망막의 색소 변화 – 홍채의 색소 세포 외에도 망막 아래에 색소 세포가 있습니다.이 세포들이 분해되고 색소를 방출할 때, 방출된 색소의 어두운 덩어리와 나중에, 덜 색소화된 부분이 나타날 수 있습니다.
- 삼출액 변화: 눈 출혈, 경질 삼출액, 망막하/하 RPE/배설액
- 드루젠, 망막에 쌓이는 세포외 물질의 작은 축적입니다.드루젠은 시력 감퇴의 원인으로 지목되는 경향이 있지만, 드루젠 퇴적물은 시력 감퇴 없이 망막에 존재할 수 있습니다.드루젠의 침전물이 많은 일부 환자들은 정상적인 시력을 가지고 있다.높은 농도의 드루젠이 존재할 때 망막에서 정상적인 망막 수신과 영상 전송이 가능할 경우, 드루젠이 시각 기능의 상실에 관련될 수 있더라도 시력 상실의 원인을 설명하는 다른 요인이 적어도 하나 있어야 합니다.
예방
2017년 코크란 리뷰에서는 비타민과 미네랄 보충제를 단독으로 또는 조합하여 사용하는 것이 AMD의 [5]시작 여부에 영향을 미치지 않는 것으로 나타났다.
흡연 예방, 식단에 생선 포함, 건강한 체중 유지 또한 AMD를 예방할[67] 수 있습니다.
관리
AMD의 치료는 진단 시점의 질병 범주에 따라 다릅니다.일반적으로 치료는 [68]AMD의 진행을 늦추는 것을 목적으로 하고 있으며,[68] 2018년 현재 AMD의 효과를 되돌릴 수 있는 치료법은 없다.조기 및 중기 AMD는 금연, 고혈압, 아테롬성 동맥경화 등의 알려진 위험인자를 수정하고 식이요법을 [2][68]수정하여 관리하고 있다.중간 단계 AMD의 경우, 관리에는 항산화제와 미네랄 [68][69]보충도 포함됩니다.어드밴스드 스테이지의 AMD는 건식 AMD(CNV 없음) 또는 습식 AMD(CNV 있음)[68]의 맥락막 신생 혈관계(CNV) 유무에 따라 관리됩니다.건식 [68]AMD에 대한 효과적인 치료법이 없습니다.습윤 AMD에 존재하는 CNV는 혈관내피성장인자([68][70][69]VEGF) 억제제로 관리된다.Amsler 그리드 또는 기타 가정용 시각 모니터링 도구를 사용하여 질병 [2]진행의 징후일 수 있는 왜곡된 시력의 발달을 모니터링할 수 있습니다.
비타민 및 미네랄 보충
연령에 관련된 눈병 연구 1과 2는 한쪽 눈에 AMD 또는 중간 AMD 또는 다른 쪽 눈에 AMD가 있고 다른 쪽 눈에 AMD가 발달한 사람들은 특정한 비타민과 미네랄 [2]보충으로부터 혜택을 받을 수 있다는 것을 보여주었다.AREDS-1의 특정 비타민과 미네랄은 비타민 C(500mg), 아연(80mg), 비타민 E(400IU), 구리(2mg), 베타카로틴(15mg)이다.AREDS-2 제제에서는 베타카로틴을 [2]복용하는 흡연자의 폐암 위험으로 인해 루테인(10mg)과 제아산틴(2mg)이 베타카로틴을 대체하였다.이러한 특정 미량 영양소 보충제는 [2]5년에 더 심각한 형태의 AMD로 진행될 위험이 낮고 시력이 더 높은 것과 관련이 있었다.미량 영양소 보충제가 중증 질환자의 AMD 진행을 막거나 [2]AMD가 없는 사람의 질병 발병을 막았다는 증거는 없다.
드라이 AMD
건식 AMD에는 치료법이 없습니다.건성 AMD에 대한 몇 가지 임상시험이 진행 중인 가운데 안구 염증을 치료하기 위한 보체억제제 개발에 대한 학계 및 의학적 관심이 높아지고 있지만, AMD(항인자 D제, 람팔리주맙)에서 제3상 시험을 완료한 첫 번째 약물은 질병 [15]진행률을 크게 개선하지 못했다.그럼에도 불구하고, 보완 시스템의 다른 측면을 겨냥한 전략은 계속 [15]진행 중이다.
습식 AMD
Ranibizumab, aflibercept, brolucizumab 및 faricimab은 습한 [70][71]AMD에서 CNV 치료를 위해 승인된 VEGF 억제제입니다.세 가지 약물은 모두 체내 주입을 통해 투여되며, 이는 눈에 직접 주입되는 것을 의미합니다.베바시주맙은 이전 두 가지 약물과 유사한 효능과 안전성을 가진 것으로 밝혀진 또 다른 VEGF 억제제이지만 AMD는 현재 [69]AMD의 경우 레이저 응고 [72]치료로 치료될 수 있습니다.
무작위 대조군 시험 결과, 베바시주맙과 라니비주맙은 유사한 유효성을 가지며, 베바시주맙에 [73]대한 부작용의 유의미한 증가는 보고되지 않았다.2014년 코크란 리뷰에 따르면 비시주맙과 라니비주맙의 전신 안전성은 위장 장애를 [74]제외하고 혈관신생 AMD를 치료하기 위해 사용되었을 때 유사하다.그러나 베바시주맵은 황반변성 치료에 대해 FDA 승인을 받지 않았다.영국에서의 논란은 승인되었지만 비싼 라니비주맙에 [75]대해 더 저렴한 베바시주맙을 비공식적으로 사용하는 것과 관련이 있다.라니비주맙은 눈 주사를 [76]위해 특별히 고안된 모체 베바시주맙 분자의 작은 조각인 팹 조각입니다.신혈관 AMD의 치료를 위해 승인된 다른 항혈관신생제로는 페갑타닙과[77] [78]아프리버셉트가 있다.
이러한 항VEGF제는 매월 또는 적응적으로 투여할 수 있습니다.적응형 안티 VEGF 치료의 경우 일반적으로 두 가지 접근법이 적용된다.프로레나타(Prore nata)의 경우 환자가 일정한 간격으로 오지만, 활성이 감지된 경우(즉, 유체의 존재)에만 치료가 투여됩니다.치료-연장의 경우 환자는 항상 치료를 받지만 [79]병변이 비활성화된 경우 다음 방문까지의 간격이 길어집니다.최근, 연구원들은 미래의 [80][81][82]치료 필요성을 예측하기 위해 인공지능 알고리즘을 적용하기 시작했다.그러나 이러한 접근법은 현재 임상 용도로 검증되지 않았습니다.
미국 안과학회 실무 지침에서는 황반 퇴화를 위한 레이저 응고 요법을 권장하지 않지만, 약물 [83][84]치료에 반응하지 않는 안구 바깥쪽 맥락막에 새로운 혈관이 있는 사람들에게 유용할 수 있다고 명시하고 있습니다.레이저 응고가 드루젠의 소실을 초래하지만 맥락막 신생혈관에 영향을 [85]미치지 않는다는 강력한 증거가 있다.2007년 Cochrane 리뷰에 따르면, 에 대한 레이저 광응고된 새로운 혈관은 공막 바깥쪽 맥락막에서 효과적이고 경제적인 방법이지만, 공막 [86]옆 또는 아래에 있는 혈관에 대해서는 이점이 제한적이라는 것이 밝혀졌다.
광역학적 치료법도 습한 AMD를 [87]치료하기 위해 사용되어 왔다.verteforfin 약물을 정맥에 투여하고, 그 후 특정 파장의 빛을 비정상적인 혈관에 가한다.이것은 혈관을 파괴하는 verteporfin을 활성화시킨다.
백내장 수술은 AMD의 진행을 증가시키는 수술에 대한 우려가 있었지만 AMD를 가진 사람들의 시력을 향상시킬 수 있다. 무작위 대조 실험 결과 즉시 백내장 수술을 받은 사람들은 지연을 겪은 사람들보다 시력이 향상되고 삶의 질이 더 좋은 것으로 나타났다.ed 백내장 수술(6개월).[88]
습식 AMD에 대한 치료법으로 방사선 치료가 제안되었지만, 항VEGF와 결합된 현대 입체 방사선 치료의 사용을 뒷받침하는 증거는 현재 불확실하며 진행 중인 [89]연구 결과를 기다리고 있다.
항HIV 치료에 사용되는 것과 같은 뉴클레오시드 역전사 억제제는 위축성 황반변성 발병 위험 감소와 관련이 있었다.이는 알루 원소가 세포질에서 L1(단백질) 매개 역전사를 거치면서 DNA 합성을 일으키기 때문이다.첫 번째 임상시험은 2021년 [90]1월 현재 준비 중이다.
적응형 장치
말초 시력은 영향을 받지 않기 때문에, 황반 변성이 있는 사람들은 그들의 남은 시력을 부분적인 [91]보상을 위해 사용하는 것을 배울 수 있다.많은 나라에서 원조와 자원을 이용할 수 있고 미국의 [92]모든 주에서 "독립 생활"을 위한 클래스가 제공되며, 일부 기술은 주 재활 부서에서 얻을 수 있습니다.
적응형 장치는 사람들이 읽도록 도울 수 있다.여기에는 돋보기, 특수 안경 렌즈, 컴퓨터 스크린 리더, 전자 안경, 독서 자료를 확대하는 TV 시스템이 포함됩니다.
JAWS 또는 Thunder와 같은 컴퓨터 화면 리더는 표준 Windows 컴퓨터에서 작동합니다.또한 Apple 기기는 다양한 기능(보이스오버, 화면 리더, 점자 등)을 제공합니다.
비디오 카메라는 표준 또는 특수 목적의 컴퓨터 모니터에 삽입할 수 있으며, 이미지를 확대 및 확대할 수 있습니다.이러한 시스템에는 종종 쓰여진 자료를 이동하기 위한 이동식 테이블이 포함되어 있습니다.
인쇄 서적, 추적을 용이하게 하는 패턴, 오디오북, 텍스트와 오디오를 모두 갖춘 DAISY 서적용 큰 글꼴을 제공합니다.
역학
노화와 관련된 황반변성의 유병률은 아시아인과 [94]아프리카인보다 유럽인에게 더 높다.아시아인과 아프리카인의 [94]유병률에는 차이가 없다.노화 관련 황반변성과 그 관련 특징의 발병률은 연령에 따라 증가하며 55세 [95]미만에서 낮다.흡연은 수정할 수 있는 가장 강력한 위험 [96]요소이다.2008년 현재,[97] 미국 백인 인구에서 노화 관련 황반변성은 전체 시력 손실의 54% 이상을 차지한다.약 8백만 명의 미국인들이 조기 연령 관련 황반 변성의 영향을 받고 있으며, 이 중 100만 명 이상이 향후 5년 이내에 노령 관련 황반 변성의 영향을 받게 될 것이다.영국에서는 65~74세의 실명자의 42%가 노화와 관련된 황반변성이 실명의 원인이고, 75~84세의 거의 3분의 2가 실명자이며,[97] 85세 이상의 거의 4분의 3이 실명의 원인이다.
조사 방향
연구에 따르면 AMD와 관련된 드루젠은 아밀로이드 베타(Aβ) 플라크와 분자 구성이 유사하며 알츠하이머병과 아테롬성 동맥경화증과 같은 다른 노화 관련 질환의 침전물도 유사합니다.이는 AMD 및 기타 연령 관련 [98]질병의 병인에도 유사한 경로가 관련될 수 있음을 시사한다.AMD는 또한 [15]눈과 유사한 구조를 가진 신장과 몇 가지 유전적, 환경적 위험 요소를 공유합니다.
유전자 검사
유전자 검사는 AMD 환자가 발병 위험이 더 큰지 여부를 식별하는데 도움을 줄 수 있고 질병의 [15]진행을 알려줄 수 있다.또한 유전자 검사를 통해 환자가 항 VEGF 약물이나 보완 억제제와 [15][99]같은 치료에 반응할 가능성이 높은지 여부를 확인할 수 있다.그러나 임상 실무에서 유전적 변이를 통합하는 예측 도구를 사용하는 데는 몇 가지 과제가 남아 있다.다양한 유전적 변종과 환경적 요인이 상호작용하여 AMD의 위험에 영향을 미치는 방법에 대한 우리의 제한된 이해와 더불어, 집단에서 공통적으로 나타나는 단일 뉴클레오티드 다형성은 AMD의 [15]개별 환자에게 작은 영향을 미칩니다.따라서, 종종 [15]더 뚜렷한 영향을 미치는 희귀 돌연변이의 기능적 결과를 이해하는 데 관심이 증가하고 있다.임상 관리를 안내하는 유전자 검사는 현재 [15]권장되지 않습니다.
줄기세포 이식
골수줄기세포를 이용한 세포기반 치료와 망막색소상피이식술이 연구되고 있다.[100]많은 실험들이 인간에게 일어났고 고무적인 [101]결과를 가져왔다.
게놈 편집
CRISPR-Cas9 게놈 편집은 VEGFA에 의한 습윤한 노화 관련 황반 변성을 치료하기 위해 사용될 수 있다.과학자들은 의도하지 않은 표적외 편집을 유발하지 않고 맥락막 신생 혈관의 영역을 63% 줄일 수 있는 인공 렌티바이러스를 영향을 받는 해부학적 영역에 주입하는 접근방식을 설명했다.또는 항Cas9 면역 [102][103]반응입니다.
기타 타입
비슷한 증상을 보이지만 병인학상 습기 또는 건조 노화와 관련된 황반 변성과는 무관한 황반 변성(희귀한)이 몇 가지 있습니다.그것들은 모두 어린 시절이나 중년에 발생할 수 있는 유전 질환이다.
- 비텔형 황반 디스트로피
- Sorsby 안저 디스트로피는 상염색체 우성 망막 질환으로 치료 불가능한 혈관하 신혈관화로 인한 갑작스러운 급성 상실이 특징입니다.
- 스타가르트병(청소년 황반변성, STGD)은 상염색체 열성 망막 장애로 청소년 황반변성, 말초 망막의 변화, 리포푸신 유사 물질의 망막하 퇴적 등이 특징이다.
매우 다른 병인과 다른 치료법을 가진 유사한 증상은 상피막이나 황반주름 또는 중심 장액망막증과 같은 황반에 영향을 미치는 다른 질환에 의해 야기될 수 있다.
주목할 만한 경우
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab "Facts About Age-Related Macular Degeneration". National Eye Institute. June 2015. Archived from the original on 22 December 2015. Retrieved 21 December 2015.
- ^ a b c d e f g h i j k Apte, Rajendra S. (5 August 2021). "Age-Related Macular Degeneration". New England Journal of Medicine. 385 (6): 539–547. doi:10.1056/NEJMcp2102061. PMID 34347954. S2CID 236926930.
- ^ a b c Mehta S (September 2015). "Age-Related Macular Degeneration". Primary Care. 42 (3): 377–91. doi:10.1016/j.pop.2015.05.009. PMID 26319344.
- ^ "Age-Related Macular Degeneration". WebMD. Retrieved 2022-03-15.
- ^ a b Evans JR, Lawrenson JG (July 2017). "Antioxidant vitamin and mineral supplements for preventing age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2017 (7): CD000253. doi:10.1002/14651858.CD000253.pub4. PMC 6483250. PMID 28756617.
- ^ Evans JR, Lawrenson JG (July 2017). "Antioxidant vitamin and mineral supplements for slowing the progression of age-related macular degeneration". The Cochrane Database of Systematic Reviews. 7 (9): CD000254. doi:10.1002/14651858.CD000254.pub4. PMC 6483465. PMID 28756618.
- ^ Ramin, Shahrokh; Soheilian, Masoud; Habibi, Gholamreza; Ghazavi, Roghayeh; Gharebaghi, Reza; Heidary, Fatemeh (2015). "Age-Related Macular Degeneration: A Scientometric Analysis". Medical Hypothesis, Discovery & Innovation in Ophthalmology. 4 (2): 39–49. ISSN 2322-4436. PMC 4458325. PMID 26060829.
- ^ Vos, Theo; Barber, Ryan M.; Bell, Brad; Bertozzi-Villa, Amelia; Biryukov, Stan; Bolliger, Ian; Charlson, Fiona; Davis, Adrian; Degenhardt, Louisa; Dicker, Daniel; Duan, Leilei; Erskine, Holly; Feigin, Valery L.; Ferrari, Alize J.; Fitzmaurice, Christina; Fleming, Thomas; Graetz, Nicholas; Guinovart, Caterina; Haagsma, Juanita; Hansen, Gillian M.; Hanson, Sarah Wulf; Heuton, Kyle R.; Higashi, Hideki; Kassebaum, Nicholas; Kyu, Hmwe; Laurie, Evan; Liang, Xiofeng; Lofgren, Katherine; Lozano, Rafael; et al. (August 2015). "Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013". The Lancet. 386 (9995): 743–800. doi:10.1016/s0140-6736(15)60692-4. PMC 4561509. PMID 26063472.
- ^ "Age-related Macular Degeneration". 22 October 2013. Archived from the original on 2013-10-22. Retrieved 5 November 2018.
- ^ "Age-Related Macular Degeneration PPP – Updated 2015". American Academy of Ophthalmology. 2015-01-29. Archived from the original on 2018-11-13. Retrieved 2018-11-13.
- ^ Roberts, DL (September 2006). "The First Year – Age Related Macular Degeneration". Marlowe & Company: 100.
- ^ Roberts, DL (September 2006). "The First Year – Age Related Macular Degeneration". Marlowe & Company: 20.
- ^ a b Cunningham J (March 2017). "Recognizing age-related macular degeneration in primary care". JAAPA. 30 (3): 18–22. doi:10.1097/01.jaa.0000512227.85313.05. PMID 28151737. S2CID 205396269.
- ^ a b c d Lim LS, Mitchell P, Seddon JM, Holz FG, Wong TY (May 2012). "Age-related macular degeneration". The Lancet. 379 (9827): 1728–38. doi:10.1016/S0140-6736(12)60282-7. PMID 22559899. S2CID 25049931.
- ^ a b c d e f g h i j k l m n o p Tzoumas, Nikolaos; Hallam, Dean; Harris, Claire L.; Lako, Majlinda; Kavanagh, David; Steel, David H.W. (November 2020). "Revisiting the role of factor H in age-related macular degeneration: Insights from complement-mediated renal disease and rare genetic variants". Survey of Ophthalmology. 66 (2): 378–401. doi:10.1016/j.survophthal.2020.10.008. ISSN 0039-6257. PMID 33157112. S2CID 226274874.
- ^ Deangelis MM, Silveira AC, Carr EA, Kim IK (May 2011). "Genetics of age-related macular degeneration: current concepts, future directions". Seminars in Ophthalmology. 26 (3): 77–93. doi:10.3109/08820538.2011.577129. PMC 4242505. PMID 21609220.
- ^ a b Thornton J, Edwards R, Mitchell P, Harrison RA, Buchan I, Kelly SP (September 2005). "Smoking and age-related macular degeneration: a review of association". Eye. 19 (9): 935–44. doi:10.1038/sj.eye.6701978. PMID 16151432.
- ^ Cougnard-Grégoire A, Delyfer MN, Korobelnik JF, Rougier MB, Malet F, Le Goff M, et al. (March 2013). "Long-term blood pressure and age-related macular degeneration: the ALIENOR study". Investigative Ophthalmology & Visual Science. 54 (3): 1905–12. doi:10.1167/iovs.12-10192. PMID 23404120.
- ^ García-Layana A, Cabrera-López F, García-Arumí J, Arias-Barquet L, Ruiz-Moreno JM (October 2017). "Early and intermediate age-related macular degeneration: update and clinical review". Clinical Interventions in Aging. 12: 1579–87. doi:10.2147/cia.s142685. PMC 5633280. PMID 29042759.
- ^ Dasari B, Prasanthi JR, Marwarha G, Singh BB, Ghribi O (August 2011). "Cholesterol-enriched diet causes age-related macular degeneration-like pathology in rabbit retina". BMC Ophthalmology. 11: 22. doi:10.1186/1471-2415-11-22. PMC 3170645. PMID 21851605.
- ^ Burgess, Stephen; Davey Smith, George (August 2017). "Mendelian Randomization Implicates High-Density Lipoprotein Cholesterol–Associated Mechanisms in Etiology of Age-Related Macular Degeneration". Ophthalmology. 124 (8): 1165–1174. doi:10.1016/j.ophtha.2017.03.042. Retrieved 29 July 2022.
- ^ Adams MK, Simpson JA, Aung KZ, Makeyeva GA, Giles GG, English DR, Hopper J, Guymer RH, Baird PN, Robman LD (June 2011). "Abdominal obesity and age-related macular degeneration". American Journal of Epidemiology. 173 (11): 1246–55. doi:10.1093/aje/kwr005. PMID 21422060.
- ^ Parekh N, Voland RP, Moeller SM, Blodi BA, Ritenbaugh C, Chappell RJ, et al. (November 2009). "Association between dietary fat intake and age-related macular degeneration in the Carotenoids in Age-Related Eye Disease Study (CAREDS): an ancillary study of the Women's Health Initiative". Archives of Ophthalmology. 127 (11): 1483–93. doi:10.1001/archophthalmol.2009.130. PMC 3144752. PMID 19901214.
- ^ SanGiovanni JP, Chew EY, Clemons TE, Davis MD, Ferris FL, Gensler GR, et al. (May 2007). "The relationship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS Report No. 20". Archives of Ophthalmology. 125 (5): 671–79. doi:10.1001/archopht.125.5.671. PMID 17502507.
- ^ a b Arunkumar R, Calvo CM, Conrady CD, Bernstein PS (May 2018). "What do we know about the macular pigment in AMD: the past, the present, and the future". Eye. 32 (5): 992–1004. doi:10.1038/s41433-018-0044-0. PMC 5944649. PMID 29576617.
- ^ "Are Computer Glasses Worth It?". American Academy of Ophthalmology. 2017-04-27. Retrieved 2020-02-02.
- ^ Maller J, George S, Purcell S, Fagerness J, Altshuler D, Daly MJ, Seddon JM (September 2006). "Common variation in three genes, including a noncoding variant in CFH, strongly influences risk of age-related macular degeneration". Nature Genetics. 38 (9): 1055–59. doi:10.1038/ng1873. PMID 16936732. S2CID 15830119.
- ^ a b Schmitz-Valckenberg, Steffen; Fleckenstein, Monika; Zouache, Moussa A.; Pfau, Maximilian; Pappas, Christian; Hageman, Jill L.; Agrón, Elvira; Malley, Claire; Keenan, Tiarnan D. L.; Chew, Emily Y.; Hageman, Gregory S. (2022-02-03). "Progression of Age-Related Macular Degeneration and Homozygous Risk at Chromosome 1 or 10". JAMA Ophthalmology. 140 (3): 252–260. doi:10.1001/jamaophthalmol.2021.6072. PMC 8814975. PMID 35113155. Retrieved 2022-02-03.
- ^ Tong, Yao; Wang, Shusheng (2020). "Not All Stressors Are Equal: Mechanism of Stressors on RPE Cell Degeneration". Frontiers in Cell and Developmental Biology. 8: 591067. doi:10.3389/fcell.2020.591067. ISSN 2296-634X. PMC 7710875. PMID 33330470.
- ^ Edwards AO, Ritter R, Abel KJ, Manning A, Panhuysen C, Farrer LA (April 2005). "Complement factor H polymorphism and age-related macular degeneration". Science. 308 (5720): 421–24. Bibcode:2005Sci...308..421E. doi:10.1126/science.1110189. PMID 15761121. S2CID 31337096.
- ^ Hughes AE, Orr N, Esfandiary H, Diaz-Torres M, Goodship T, Chakravarthy U (October 2006). "A common CFH haplotype, with deletion of CFHR1 and CFHR3, is associated with lower risk of age-related macular degeneration". Nature Genetics. 38 (10): 1173–77. doi:10.1038/ng1890. PMID 16998489. S2CID 21178921.
- ^ Fritsche LG, Lauer N, Hartmann A, Stippa S, Keilhauer CN, Oppermann M, et al. (December 2010). "An imbalance of human complement regulatory proteins CFHR1, CFHR3 and factor H influences risk for age-related macular degeneration (AMD)". Human Molecular Genetics. 19 (23): 4694–704. doi:10.1093/hmg/ddq399. PMID 20843825.
- ^ a b Yates, John R.W.; Sepp, Tiina; Matharu, Baljinder K.; Khan, Jane C.; Thurlby, Deborah A.; Shahid, Humma; Clayton, David G.; Hayward, Caroline; Morgan, Joanne; Wright, Alan F.; Armbrecht, Ana Maria; Dhillon, Baljean; Deary, Ian J.; Redmond, Elizabeth; Bird, Alan C.; Moore, Anthony T.; Genetic Factors in AMD Study, Group. (9 August 2007). "Complement C3 Variant and the Risk of Age-Related Macular Degeneration". New England Journal of Medicine. 357 (6): 553–61. doi:10.1056/NEJMoa072618. PMID 17634448.
- ^ Maller JB, Fagerness JA, Reynolds RC, Neale BM, Daly MJ, Seddon JM (October 2007). "Variation in complement factor 3 is associated with risk of age-related macular degeneration". Nature Genetics. 39 (10): 1200–01. doi:10.1038/ng2131. PMID 17767156. S2CID 8595223.
- ^ Yang Z, Camp NJ, Sun H, Tong Z, Gibbs D, Cameron DJ, et al. (November 2006). "A variant of the HTRA1 gene increases susceptibility to age-related macular degeneration". Science. 314 (5801): 992–93. Bibcode:2006Sci...314..992Y. doi:10.1126/science.1133811. PMID 17053109. S2CID 19577378.
- ^ Dewan A, Liu M, Hartman S, Zhang SS, Liu DT, Zhao C, Tam PO, Chan WM, Lam DS, Snyder M, Barnstable C, Pang CP, Hoh J (November 2006). "HTRA1 promoter polymorphism in wet age-related macular degeneration". Science. 314 (5801): 989–92. Bibcode:2006Sci...314..989D. doi:10.1126/science.1133807. PMID 17053108. S2CID 85725181.
- ^ Hirschler, Ben (2008-10-07). "Gene discovery may help hunt for blindness cure". Reuters. Archived from the original on October 11, 2008. Retrieved 2008-10-07.
- ^ Udar N, Atilano SR, Memarzadeh M, Boyer DS, Chwa M, Lu S, Maguen B, Langberg J, Coskun P, Wallace DC, Nesburn AB, Khatibi N, Hertzog D, Le K, Hwang D, Kenney MC (June 2009). "Mitochondrial DNA haplogroups associated with age-related macular degeneration". Investigative Ophthalmology & Visual Science. 50 (6): 2966–74. doi:10.1167/iovs.08-2646. PMID 19151382.
- ^ Canter JA, Olson LM, Spencer K, Schnetz-Boutaud N, Anderson B, Hauser MA, Schmidt S, Postel EA, Agarwal A, Pericak-Vance MA, Sternberg P, Haines JL (May 2008). Nicholas Weedon M (ed.). "Mitochondrial DNA polymorphism A4917G is independently associated with age-related macular degeneration". PLOS ONE. 3 (5): e2091. Bibcode:2008PLoSO...3.2091C. doi:10.1371/journal.pone.0002091. PMC 2330085. PMID 18461138.

- ^ Mullins RF, Russell SR, Anderson DH, Hageman GS (May 2000). "Drusen associated with aging and age-related macular degeneration contain proteins common to extracellular deposits associated with atherosclerosis, elastosis, amyloidosis, and dense deposit disease". FASEB Journal. 14 (7): 835–46. doi:10.1096/fasebj.14.7.835. PMID 10783137. S2CID 24601453.
- ^ Hageman GS, Anderson DH, Johnson LV, Hancox LS, Taiber AJ, Hardisty LI, et al. (May 2005). "A common haplotype in the complement regulatory gene factor H (HF1/CFH) predisposes individuals to age-related macular degeneration". Proceedings of the National Academy of Sciences of the United States of America. 102 (20): 7227–32. doi:10.1073/pnas.0501536102. PMC 1088171. PMID 15870199.
- ^ Chen LJ, Liu DT, Tam PO, Chan WM, Liu K, Chong KK, Lam DS, Pang CP (December 2006). "Association of complement factor H polymorphisms with exudative age-related macular degeneration". Molecular Vision. 12: 1536–42. PMID 17167412.
- ^ Despriet DD, Klaver CC, Witteman JC, Bergen AA, Kardys I, de Maat MP, Boekhoorn SS, Vingerling JR, Hofman A, Oostra BA, Uitterlinden AG, Stijnen T, van Duijn CM, de Jong PT (July 2006). "Complement factor H polymorphism, complement activators, and risk of age-related macular degeneration". JAMA. 296 (3): 301–09. doi:10.1001/jama.296.3.301. PMID 16849663.
- ^ Li M, Atmaca-Sonmez P, Othman M, Branham KE, Khanna R, Wade MS, et al. (September 2006). "CFH haplotypes without the Y402H coding variant show strong association with susceptibility to age-related macular degeneration". Nature Genetics. 38 (9): 1049–54. doi:10.1038/ng1871. PMC 1941700. PMID 16936733.
- ^ Haines JL, Hauser MA, Schmidt S, Scott WK, Olson LM, Gallins P, Spencer KL, Kwan SY, Noureddine M, Gilbert JR, Schnetz-Boutaud N, Agarwal A, Postel EA, Pericak-Vance MA (April 2005). "Complement factor H variant increases the risk of age-related macular degeneration". Science. 308 (5720): 419–21. Bibcode:2005Sci...308..419H. doi:10.1126/science.1110359. PMID 15761120. S2CID 32716116.
- ^ Rohrer, Bärbel; Long, Qin; Coughlin, Beth; Renner, Brandon; Huang, Yuxiang; Kunchithapautham, Kannan; Ferreira, Viviana P.; Pangburn, Michael K.; Gilkeson, Gary S.; Thurman, Joshua M.; Tomlinson, Stephen; Holers, V. Michael (2010). "A Targeted Inhibitor of the Complement Alternative Pathway Reduces RPE Injury and Angiogenesis in Models of Age-Related Macular Degeneration". Inflammation and Retinal Disease: Complement Biology and Pathology. Advances in Experimental Medicine and Biology. Vol. 703. pp. 137–49. doi:10.1007/978-1-4419-5635-4_10. ISBN 978-1-4419-5634-7. PMID 20711712.
- ^ Kunchithapautham K, Rohrer B (July 2011). "Sublytic membrane-attack-complex (MAC) activation alters regulated rather than constitutive vascular endothelial growth factor (VEGF) secretion in retinal pigment epithelium monolayers". The Journal of Biological Chemistry. 286 (27): 23717–24. doi:10.1074/jbc.M110.214593. PMC 3129152. PMID 21566137.
- ^ Fritsche LG, Loenhardt T, Janssen A, Fisher SA, Rivera A, Keilhauer CN, Weber BH (July 2008). "Age-related macular degeneration is associated with an unstable ARMS2 (LOC387715) mRNA". Nature Genetics. 40 (7): 892–96. doi:10.1038/ng.170. PMID 18511946. S2CID 205344383.
- ^ Chen W, Stambolian D, Edwards AO, Branham KE, Othman M, Jakobsdottir J, et al. (April 2010). "Genetic variants near TIMP3 and high-density lipoprotein-associated loci influence susceptibility to age-related macular degeneration". Proceedings of the National Academy of Sciences of the United States of America. 107 (16): 7401–06. Bibcode:2010PNAS..107.7401C. doi:10.1073/pnas.0912702107. PMC 2867722. PMID 20385819.
- ^ Neale BM, Fagerness J, Reynolds R, Sobrin L, Parker M, Raychaudhuri S, Tan PL, Oh EC, Merriam JE, Souied E, Bernstein PS, Li B, Frederick JM, Zhang K, Brantley MA, Lee AY, Zack DJ, Campochiaro B, Campochiaro P, Ripke S, Smith RT, Barile GR, Katsanis N, Allikmets R, Daly MJ, Seddon JM (April 2010). "Genome-wide association study of advanced age-related macular degeneration identifies a role of the hepatic lipase gene (LIPC)". Proceedings of the National Academy of Sciences of the United States of America. 107 (16): 7395–400. Bibcode:2010PNAS..107.7395N. doi:10.1073/pnas.0912019107. PMC 2867697. PMID 20385826.
- ^ Ratnayaka JA, Serpell LC, Lotery AJ (August 2015). "Dementia of the eye: the role of amyloid beta in retinal degeneration". Eye. 29 (8): 1013–26. doi:10.1038/eye.2015.100. PMC 4541342. PMID 26088679.
- ^ a b Ferris FL, Wilkinson CP, Bird A, Chakravarthy U, Chew E, Csaky K, Sadda SR (April 2013). "Clinical classification of age-related macular degeneration". Ophthalmology. 120 (4): 844–51. doi:10.1016/j.ophtha.2012.10.036. PMID 23332590.
- ^ Wu Z, Luu CD, Hodgson LA, Caruso E, Tindill N, Aung KZ, McGuinness MB, Makeyeva G, Chen FK, Chakravarthy U, Arnold JJ, Heriot WJ, Durkin SR, Guymer RH (June 2020). "Prospective Longitudinal Evaluation of Nascent Geographic Atrophy in Age-Related Macular Degeneration". Ophthalmol Retina. 4 (6): 568–575. doi:10.1016/j.oret.2019.12.011. PMID 32088159. S2CID 211263484.
- ^ Wu Z, Pfau M, Blodi BA, Holz FG, Jaffe GJ, Liakopoulos S, Sadda SR, Staurenghi G, Bjelopera E, Brown T, Chang P, Choong J, Corradetti G, Corvi F, Domalpally A, Hurtenbach C, Nittala MG, Olson A, Pak JW, Pappe J, Saßmannshausen M, Skalak C, Thiele S, Guymer RH, Schmitz-Valckenberg S (March 2021). "OCT Signs of Early Atrophy in Age-Related Macular Degeneration: Interreader Agreement: Classification of Atrophy Meetings Report 6". Ophthalmol Retina. 6 (1): 4–14. doi:10.1016/j.oret.2021.03.008. ISSN 2468-6530. PMID 33766801.
- ^ X. Shaw, Peter; Stiles, Travis; Douglas, Christopher; Ho, Daisy; Fan, Wei; Du, Hongjun; Xiao, Xu (2016). "Oxidative stress, innate immunity, and age-related macular degeneration". AIMS Molecular Science. 3 (2): 196–221. doi:10.3934/molsci.2016.2.196. PMC 4882104. PMID 27239555.
- ^ Kauppinen, Anu; Paterno, Jussi J.; Blasiak, Janusz; Salminen, Antero; Kaarniranta, Kai (6 February 2016). "Inflammation and its role in age-related macular degeneration". Cellular and Molecular Life Sciences. 73 (9): 1765–86. doi:10.1007/s00018-016-2147-8. PMC 4819943. PMID 26852158.
- ^ Thulliez, Marie; Zhang, Qinqin; Shi, Yingying; Zhou, Hao; Chu, Zhongdi; de Sisternes, Luis; Durbin, Mary K.; Feuer, William; Gregori, Giovanni; Wang, Ruikang K.; Rosenfeld, Philip J. (June 2019). "Correlations between Choriocapillaris Flow Deficits around Geographic Atrophy and Enlargement Rates Based on Swept-Source OCT Imaging". Ophthalmology Retina. 3 (6): 478–88. doi:10.1016/j.oret.2019.01.024. PMID 31174669. S2CID 86851083.
- ^ Sarangarajan, Rangaprasad; Apte, Shireesh. P. (2005). "Melanin Aggregation and Polymerization: Possible Implications in Age-Related Macular Degeneration". Ophthalmic Research. 37 (3): 136–41. doi:10.1159/000085533. PMID 15867475. S2CID 27499198.
- ^ John Lacey, "Harvard Medical은 Merck와 황반변성의 잠재적 치료제 개발을 위한 계약을 체결했습니다." 2007-06-07년 Wayback Machine, 2006년 5월 23일
- ^ Tomany SC, Cruickshanks KJ, Klein R, Klein BE, Knudtson MD (May 2004). "Sunlight and the 10-year incidence of age-related maculopathy: the Beaver Dam Eye Study". Archives of Ophthalmology. 122 (5): 750–57. doi:10.1001/archopht.122.5.750. PMID 15136324.
- ^ Szaflik JP, Janik-Papis K, Synowiec E, Ksiazek D, Zaras M, Wozniak K, Szaflik J, Blasiak J (October 2009). "DNA damage and repair in age-related macular degeneration". Mutation Research. 669 (1–2): 169–76. doi:10.1016/j.mrfmmm.2009.06.008. PMID 19559717.
- ^ Barot M, Gokulgandhi MR, Mitra AK (December 2011). "Mitochondrial dysfunction in retinal diseases". Current Eye Research. 36 (12): 1069–77. doi:10.3109/02713683.2011.607536. PMC 4516173. PMID 21978133.
- ^ Karniranta K, Pawlowska E, Szzepanska J, Jablkawska A, Blasiak J. 연령 관련 황반변성의 ROS 매개 병인에 대한 미토콘드리아 DNA 손상의 역할(AMD); 2019년 5월 14일 (10일)PMID 31091656, PMCID: PMC6566654
- ^ a b National Guideline Alliance (UK) (2018). Age-related macular degeneration: diagnosis and management. National Institute for Health and Care Excellence: Clinical Guidelines. London: National Institute for Health and Care Excellence (UK). ISBN 978-1473127876. PMID 29400919.
- ^ Owsley C, McGwin G, Clark ME, Jackson GR, Callahan MA, Kline LB, Witherspoon CD, Curcio CA (February 2016). "Delayed Rod-Mediated Dark Adaptation Is a Functional Biomarker for Incident Early Age-Related Macular Degeneration". Ophthalmology. 123 (2): 344–51. doi:10.1016/j.ophtha.2015.09.041. PMC 4724453. PMID 26522707.
- ^ Faes L, Bodmer NS, Bachmann LM, Thiel MA, Schmid MK (July 2014). "Diagnostic accuracy of the Amsler grid and the preferential hyperacuity perimetry in the screening of patients with age-related macular degeneration: systematic review and meta-analysis". Eye. 28 (7): 788–96. doi:10.1038/eye.2014.104. PMC 4094801. PMID 24788016.
- ^ "Dry macular degeneration - Symptoms and causes". Mayo Clinic. Retrieved 2022-03-15.
- ^ a b c d e f g 주교 P.노화로 인한 황반변성.BMJ의 베스트 프랙티스2018.
- ^ a b c Lawrenson JG, Evans JR (April 2015). "Omega 3 fatty acids for preventing or slowing the progression of age-related macular degeneration" (PDF). The Cochrane Database of Systematic Reviews (4): CD010015. doi:10.1002/14651858.cd010015.pub3. PMC 7087473. PMID 25856365.
- ^ a b Sarwar S, Clearfield E, Soliman MK, Sadiq MA, Baldwin AJ, Hanout M, Agarwal A, Sepah YJ, Do DV, Nguyen QD (February 2016). "Aflibercept for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2016 (2): CD011346. doi:10.1002/14651858.cd011346.pub2. PMC 5030844. PMID 26857947.
- ^ Nguyen, Quan Dong (2020). "Brolucizumab: Evolution through Preclinical and Clinical Studies and the Implications for the Management of Neovascular Age-Related Macular Degeneration". Ophthalmology. 127 (7): 963–76. doi:10.1016/j.ophtha.2019.12.031. PMID 32107066.
- ^ Virgili G, Bini A (July 2007). "Laser photocoagulation for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews (3): CD004763. doi:10.1002/14651858.cd004763.pub2. PMID 17636773.
- ^ Chakravarthy U, Harding SP, Rogers CA, Downes SM, Lotery AJ, Culliford LA, Reeves BC (October 2013). "Alternative treatments to inhibit VEGF in age-related choroidal neovascularisation: 2-year findings of the IVAN randomised controlled trial". The Lancet. 382 (9900): 1258–67. doi:10.1016/S0140-6736(13)61501-9. PMID 23870813.
- ^ Moja L, Lucenteforte E, Kwag KH, Bertele V, Campomori A, Chakravarthy U, D'Amico R, Dickersin K, Kodjikian L, Lindsley K, Loke Y, Maguire M, Martin DF, Mugelli A, Mühlbauer B, Püntmann I, Reeves B, Rogers C, Schmucker C, Subramanian ML, Virgili G (September 2014). Moja L (ed.). "Systemic safety of bevacizumab versus ranibizumab for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews. 9 (9): CD011230. doi:10.1002/14651858.CD011230.pub2. hdl:2434/273140. PMC 4262120. PMID 25220133.
- ^ Copley, Caroline; Hirschler, Ben (April 24, 2012). "Novartis challenges UK Avastin use in eye disease". Reuters. Archived from the original on May 22, 2013.
- ^ Heidary, Fatemeh; Hitam, Wan Hazabbah Wan; Ngah, Nor Fariza; George, Tara Mary; Hashim, Hanizasurana; Shatriah, Ismail (2011). "Intravitreal Ranibizumab for Choroidal Neovascularization in Best's Vitelliform Macular Dystrophy in a 6-Year-Old Boy". Journal of Pediatric Ophthalmology & Strabismus. 48 (6): e19-22. doi:10.3928/01913913-20110308-02. ISSN 0191-3913. PMID 21417187.
- ^ "FDA Approves New Drug Treatment for Age-Related Macular Degeneration". FDA.gov. U.S. Food and Drug Administration. Archived from the original on 2015-11-20.
- ^ FDA, 2013-05-28 Wayback Machine에서 황반변성에 대한 Eylea 승인
- ^ Okada M, Kandasamy R, Chong EW, McGuiness M, Guymer RH (August 2018). "The Treat-and-Extend Injection Regimen Versus Alternate Dosing Strategies in Age-related Macular Degeneration: A Systematic Review and Meta-analysis". Am J Ophthalmol. 192: 184–197. doi:10.1016/j.ajo.2018.05.026. PMID 29885297. S2CID 47012435.
- ^ Pfau M, Sahu S, Rupnow RA, Romond K, Millet D, Holz FG, Schmitz-Valckenberg S, Fleckenstein M, Lim JI, de Sisternes L, Leng T, Rubin DL, Hallak JA (June 2021). "Probabilistic Forecasting of Anti-VEGF Treatment Frequency in Neovascular Age-Related Macular Degeneration". Transl Vis Sci Technol. 10 (7): 30. doi:10.1167/tvst.10.7.30. PMC 8254013. PMID 34185055.
- ^ Vogl WD, Waldstein SM, Gerendas BS, Schlegl T, Langs G, Schmidt-Erfurth U (August 2017). "Analyzing and Predicting Visual Acuity Outcomes of Anti-VEGF Therapy by a Longitudinal Mixed Effects Model of Imaging and Clinical Data". Invest Ophthalmol Vis Sci. 58 (10): 4173–4181. doi:10.1167/iovs.17-21878. PMID 28837729.
- ^ Gallardo M, Munk MR, Kurmann T, De Zanet S, Mosinska A, Karagoz IK, Zinkernagel MS, Wolf S, Sznitman R (July 2021). "Machine Learning Can Predict Anti-VEGF Treatment Demand in a Treat-and-Extend Regimen for Patients with Neovascular AMD, DME, and RVO Associated Macular Edema". Ophthalmol Retina. 5 (7): 604–624. doi:10.1016/j.oret.2021.05.002. PMID 33971352.
- ^ "Age-Related Macular Degeneration PPP – Updated 2015". American Academy of Ophthalmology Preferred Practice Pattern. 29 January 2015. Archived from the original on 21 October 2016. Retrieved 22 October 2016.
- ^ Lindsley K, Li T, Ssemanda E, Virgili G, Dickersin K (April 2016). "Interventions for Age-Related Macular Degeneration: Are Practice Guidelines Based on Systematic Reviews?". Ophthalmology. 123 (4): 884–97. doi:10.1016/j.ophtha.2015.12.004. PMC 4808456. PMID 26804762.
- ^ Virgili G, Michelessi M, Parodi MB, Bacherini D, Evans JR (October 2015). "Laser treatment of drusen to prevent progression to advanced age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2015 (10): CD006537. doi:10.1002/14651858.CD006537.pub3. PMC 4733883. PMID 26493180.
- ^ Virgili G, Bini A (July 2007). "Laser photocoagulation for neovascular age-related macular degeneration". The Cochrane Database of Systematic Reviews (3): CD004763. doi:10.1002/14651858.CD004763.pub2. PMID 17636773.
- ^ Meads C (2003). "Clinical effectiveness and cost–utility of photodynamic therapy for wet age-related macular degeneration: a systematic review and economic evaluation". Health Technology Assessment. 7 (9): v–vi, 1–98. doi:10.3310/hta7090. PMID 12709292.
- ^ Casparis H, Lindsley K, Kuo IC, Sikder S, Bressler NM (February 2017). "Surgery for cataracts in people with age-related macular degeneration". The Cochrane Database of Systematic Reviews. 2017 (2): CD006757. doi:10.1002/14651858.CD006757.pub4. PMC 3480178. PMID 28206671.
- ^ Evans, Jennifer R; Igwe, Chinedu; Jackson, Timothy L; Chong, Victor (2020-08-26). "Radiotherapy for neovascular age-related macular degeneration". Cochrane Database of Systematic Reviews. 2020 (8): CD004004. doi:10.1002/14651858.cd004004.pub4. ISSN 1465-1858. PMC 8812340. PMID 32844399. S2CID 221326233.
- ^ Fukuda, Shinichi; Varshney, Akhil; Fowler, Benjamin J.; Wang, Shao-bin; Narendran, Siddharth; Ambati, Kameshwari; Yasuma, Tetsuhiro; Magagnoli, Joseph; Leung, Hannah; Hirahara, Shuichiro; Nagasaka, Yosuke (2021-02-09). "Cytoplasmic synthesis of endogenous Alu complementary DNA via reverse transcription and implications in age-related macular degeneration". Proceedings of the National Academy of Sciences. 118 (6): e2022751118. doi:10.1073/pnas.2022751118. ISSN 0027-8424. PMC 8017980. PMID 33526699. S2CID 231761522.
- ^ "Low Vision Rehabilitation Delivery Model". Mdsupport.org. Archived from the original on 2010-11-07. Retrieved 2011-01-11.
- ^ "Agencies, Centers, Organizations, & Societies". Mdsupport.org. 2005-09-01. Archived from the original on 2011-06-11. Retrieved 2011-01-11.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. Archived from the original on 2009-11-11. Retrieved Nov 11, 2009.
- ^ a b Wong WL, Su X, Li X, Cheung CM, Klein R, Cheng CY, Wong TY (February 2014). "Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040: a systematic review and meta-analysis". The Lancet. Global Health. 2 (2): e106–16. doi:10.1016/S2214-109X(13)70145-1. PMID 25104651.
- ^ "Age-related macular degeneration - Symptoms, diagnosis and treatment". BMJ Best Practice. Retrieved 2018-11-13.
- ^ Velilla S, García-Medina JJ, García-Layana A, Dolz-Marco R, Pons-Vázquez S, Pinazo-Durán MD, Gómez-Ulla F, Arévalo JF, Díaz-Llopis M, Gallego-Pinazo R (2013). "Smoking and age-related macular degeneration: review and update". Journal of Ophthalmology. 2013: 895147. doi:10.1155/2013/895147. PMC 3866712. PMID 24368940.
- ^ a b Coleman, Hanna R; Chan, Chi-Chao; Ferris, Frederick L; Chew, Emily Y (November 2008). "Age-related macular degeneration". The Lancet. 372 (9652): 1835–45. doi:10.1016/S0140-6736(08)61759-6. ISSN 0140-6736. PMC 2603424. PMID 19027484.
- ^ Mullins RF, Russell SR, Anderson DH, Hageman GS, et al. (May 2000). "Drusen associated with aging and age-related macular degeneration contain proteins common to extracellular deposits associated with atherosclerosis, elastosis, amyloidosis, and dense deposit disease". FASEB Journal. 14 (7): 835–46. doi:10.1096/fasebj.14.7.835. PMID 10783137. S2CID 24601453.
- ^ "EYE-RISK - EYE-RISK". www.eyerisk.eu. Retrieved 2021-05-15.
- ^ John S, Natarajan S, Parikumar P, Shanmugam PM, Senthilkumar R, Green DW, Abraham SJ (2013). "Choice of Cell Source in Cell-Based Therapies for Retinal Damage due to Age-Related Macular Degeneration: A Review". Journal of Ophthalmology. 2013: 1–9. doi:10.1155/2013/465169. PMC 3654320. PMID 23710332.
- ^ Carr AJ, Smart MJ, Ramsden CM, Powner MB, da Cruz L, Coffey PJ (July 2013). "Development of human embryonic stem cell therapies for age-related macular degeneration". Trends in Neurosciences. 36 (7): 385–95. doi:10.1016/j.tins.2013.03.006. PMID 23601133. S2CID 1007033.
- ^ "Transient editing catches the eye" (Editorial). Nature Biomedical Engineering. 5 (2): 127. February 2021. doi:10.1038/s41551-021-00695-z. PMID 33580230.
- ^ Ling, Sikai; Yang, Shiqi; Hu, Xinde; Yin, Di; Dai, Yao; Qian, Xiaoqing; Wang, Dawei; Pan, Xiaoyong; Hong, Jiaxu; Sun, Xiaodong; Yang, Hui; Paludan, Soren Riis; Cai, Yujia (February 2021). "Lentiviral delivery of co-packaged Cas9 mRNA and a Vegfa -targeting guide RNA prevents wet age-related macular degeneration in mice". Nature Biomedical Engineering. 5 (2): 144–56. doi:10.1038/s41551-020-00656-y. ISSN 2157-846X. PMID 33398131. S2CID 230508724. Retrieved 7 March 2021.
- ^ "Judi Dench "시력 저하로 더 이상 읽을 수 없음" 웨이백 머신에 보관된 2016-10-19" 가디언, 2014년 2월 23일
- ^ "Joan은 기립박수를 보내며 2016-04-20 Wayback Machine에서 보관" 가디언, 2014년 5월 13일
- ^ "2013-02-08년 웨이백 머신에 보관된 황반협회의 초석", 황반협.(2012년까지 월리스와 그로밋에서 월리스의 목소리를 맡은 것으로 유명함)






