호르몬 보충 요법
Hormone replacement therapy폐경 호르몬 치료 또는 폐경 후 호르몬 치료로도 알려진 호르몬 대체 요법은 여성 [1][2]갱년기와 관련된 증상을 치료하기 위해 사용되는 호르몬 치료의 한 형태이다.이러한 증상들은 발열, 질 위축, 피부 노화 가속화, 질 건조, 근육량 감소, 성 기능 장애, 그리고 뼈 손실을 포함할 수 있습니다.그것들은 대부분 [1][2]폐경기 동안 발생하는 성호르몬의 감소와 관련이 있다.
폐경기 증상에 HRT에서 사용되는 주요 호르몬 약물은 에스트로겐과 프로게스테론이며, 그 중 프로게스테론은 자연발생적인 주요 여성 성호르몬이며, 또한 폐경기 [1]호르몬 치료에 사용되는 제조된 약물이다.비록 두 종류의 호르몬이 증상적인 이점을 가질 수 있지만, 프로게스토겐은 자궁내막암의 위험을 피하기 위해 자궁이 있을 때 에스트로겐 요법에 특별히 첨가된다.이것은 프로게스토겐이 이 [3][4]위험을 감소시키는 반면, 무저항 에스트로겐 요법은 자궁내막 비후화를 촉진하고 암의 위험을 증가시킬 수 있기 때문이다.테스토스테론 같은 안드로겐도 [5]가끔 사용된다.HRT는 다양한 경로를 [1][2]통해 사용할 수 있습니다.
대부분의 장기 시스템에 대한 HRT의 장기적인 영향은 호르몬에 대한 마지막 생리학적 노출 이후 나이와 시간에 따라 다르며, 개별 요법에는 큰 차이가 있을 수 있으며, 이는 효과 분석을 어렵게 [6]하는 요인이다.WHI(Women's Health Initiative)는 1991년에 시작된 27,000명 이상의 여성을 대상으로 한 지속적인 연구로, 가장 최근의 분석에서는 폐경 후 10년 이내에 HRT가 관상동맥 질환, 골다공증 및 치매의 모든 원인 사망률과 위험을 감소시킨다; 10년 후 사망률과 관상동맥 심장에 대한 유익한 영향비록 고관절과 척추골절의 위험이 감소하고 [7][8]경구 복용 시 정맥혈전 색전증의 위험이 증가하지만 질병은 더 이상 명백하지 않다.
"생물학적" 호르몬 대체는 21세기 발전된 것으로 [9]"인체 내에서 생성되는 호르몬과 정확히 동일한 화학 및 분자 구조를 가진 제조된 화합물을 사용한다.이것들은 주로 식물에서[10] 유래한 스테로이드제이며 등록된 의약품 또는 맞춤형 복합제제의 구성요소가 될 수 있다. 후자는 표준화 및 공식적인 [11]감독 부족으로 인해 규제 기관에 의해 일반적으로 권장되지 않는다.생체동일 호르몬 대체는 2017년 [12]현재 그 안전성과 효능을 판단하기에는 임상 연구가 불충분하다.
미국 식품의약국(FDA)의 현재 사용 지침에는 혈관 운동 핫플래시 또는 질 위축과 같은 갱년기 증상의 단기 치료와 골다공증 [13]예방이 포함된다.
의료 용도
미국에서 HRT의 승인된 사용에는 핫 플래시와 질 위축과 같은 갱년기 증상의 단기 치료와 골다공증 [13]예방이 포함된다.미국산부인과학회(ACOG)는 갱년기 [14]증상의 증상 완화를 위해 HRT를 승인하고 적절한 [15]시나리오에서 65세 이상의 사용을 옹호합니다.북미 갱년기 협회(NAMS) 2016 연차총회는 HRT가 [16]60세 이전의 여성들에게 위험성보다 더 많은 혜택을 줄 수 있다고 언급했다.
The Endocrine Society가 발표한 합의된 전문가 의견은 폐경기 주변 또는 폐경기 초기 몇 년 동안 복용했을 때 HRT는 이전에 발표된 것보다 위험을 덜 수반하고 대부분의 [17]시나리오에서 모든 원인 사망률을 감소시킨다고 말했다.미국임상내분비학회(AACE)도 적절한 [12]경우 HRT를 승인하는 입장문을 발표했다.
이 치료를 받는 여성은 대개 폐경 후, 근막 또는 외과적으로 폐경 후이다.폐경은 난포 활동의 상실로 인한 월경의 영구적인 중단으로, 마지막 자연 생리 주기로부터 12개월 후에 시작하는 것으로 정의된다.이 12개월의 시점은 갱년기를 '주경계면'과 '후경계면'[4]으로 알려진 조기 및 후기의 전환기로 나눈다.난소암이나 자궁암을 치료하기 위해 할 수 있는 것과 같이 난소를 수술로 제거하면 조기 폐경이 발생할 수 있다.
인구통계학적으로 볼 때, 이용 가능한 데이터의 대부분은 폐경 후 미국 여성으로, 동시에 존재하는 질환이 있고 평균 연령이 60세 [18]이상이다.
갱년기 증상
HRT는 [19]폐경기 기간 동안 갱년기 증상으로부터 단기적인 완화를 위해 종종 투여된다.잠재적 갱년기 증상은 다음과 같습니다.[1][2]
- 핫 플래시 - 혈관 운동 증상
- 외음부 질 위축 - 위축성 질염 및 건조증
- 질 위축과 윤활 부족으로 인한 고통스런 성관계
- 골감소 - 골감소증, 골다공증 및 관련 골절로 이어질 수 있는 골밀도의 감소
- 성욕의 감소
- 탈여성화 - 여성 지방 분포 감소 및 피부[20][21] 노화 가속화
- 수면장애와 관절통
이 중 가장 흔한 것은 성욕 상실과 [4][22]질 건조증이다.
심장병
폐경기에서의 HRT의 영향은 다양하며, 5년 이내에 시작할 때는 심장병 위험이 낮지만 10년 [23][24][25]후에는 영향이 없다.폐경 [26]후 20년 후 HRT를 투여하면 심장질환이 증가할 수 있다.이러한 변동성은 일부 리뷰를 통해 [27]이환율에 유의한 영향이 없음을 시사했다.중요한 것은 [6]연령에 관계없이 HRT와 장기 사망률에 차이가 없다는 것이다.
코크란 리뷰에 따르면 폐경 후 10년 이내에 HRT를 시작한 여성은 뇌졸중과 폐색전증의 [23]위험성에 강한 영향을 미치지 않고 사망률과 관상동맥 심장질환이 낮았다.폐경 후 10년 이상 경과한 후 치료를 시작한 사람들은 사망률과 관상동맥 심장병에는 거의 영향을 주지 않았지만 뇌졸중 위험은 증가하였다.두 치료법 모두 정맥 응괴와 [23]폐색전증과 관련이 있었다.
에스트로겐과 프로게스테론이 함유된 HRT는 또한 콜레스테롤 수치를 향상시킨다.폐경이 되면 HDL은 감소하고 LDL, 트리글리세리드, 리포단백은 증가하는데, 이는 에스트로겐과 역행하는 패턴이다.HRT는 심장 수축, 관상동맥 혈류, 당 대사를 개선하고 혈소판 응집 및 플라크 형성을 감소시킵니다.HRT는 콜레스테롤 ABC 수송체의 [28]유도를 통해 역콜레스테롤 수송을 촉진할 수 있다.HRT는 또한 혈전성 지단백 a의 [29]큰 감소를 초래한다.테스토스테론 요법을 사용한 심혈관 질환에 대한 연구는 혼합되었고, 일부는 효과가 없거나 가벼운 부정적인 영향을 시사했지만, 다른 것들은 콜레스테롤, 트리글리세리드, [30][31]체중과 같은 대리 표시의 개선을 보여주었다.테스토스테론은 혈관 내피 기능과 색조에 긍정적인 영향을 미치며, 관찰 연구 결과 테스토스테론이 낮은 여성은 심장병에 걸릴 위험이 더 높을 수 있습니다.사용 가능한 스터디는 작은 샘플 크기와 스터디 설계에 의해 제한됩니다.폐경과 함께 발생하는 저성호르몬 결합 글로불린은 체질량 지수 증가와 제2형 [32]당뇨병 위험과 관련이 있다.
핏덩어리지다
정맥 혈전 형성 및 폐색전증에 대한 호르몬 대체 요법의 영향은 에스트로겐 및 프로게스토겐 치료법, 용량 또는 [18]사용 방법에 따라 달라질 수 있습니다.투여 경로 간 비교 결과 에스트로겐을 피부나 질에 바르면 [18][33]혈전 위험이 낮아지는 반면 경구 투여 시 혈전 및 폐색전증의 위험이 [23]높아지는 것으로 나타났다.호르몬 치료의 피부와 질 경로는 첫 번째 통과 대사의 대상이 아니기 때문에 구강 치료가 비타민 K의존성 응고 인자의 간 합성에 미치는 동화 효과가 부족하여 구강 치료가 혈전 [34]형성을 증가시킬 수 있는 이유를 설명할 수 있습니다.
2018년 리뷰에서는 프로게스테론과 에스트로겐을 함께 복용하면 이러한 [33]위험을 줄일 수 있는 것으로 밝혀졌지만, 다른 리뷰에서는 에스트로겐과 프로게스토겐이 결합되었을 때, 특히 폐경 후 10년 이상 경과하고 여성이 60세 [18][23]이상 되었을 때 혈전과 폐색전증의 위험이 증가했다고 보고되었다.
정맥 혈전 색전증의 위험은 생물학적 동일성 제제로 감소될 수 있지만, 이에 대한 연구는 [35]초기 단계일 뿐이다.
| 유형 | 경로 | 약품 | 승산비(95%) |
|---|---|---|---|
| 갱년기 호르몬 요법 | 오랄 | 에스트라디올 단독 1일 1mg 이하 1일 1mg 이상 | 1.27 (1.16–1.39)* 1.22 (1.09–1.37)* 1.35 (1.18–1.55)* |
| 켤레 에스트로겐만 0.625mg/일 0.625mg/일 | 1.49 (1.39–1.60)* 1.40 (1.28–1.53)* 1.71 (1.51–1.93)* | ||
| 에스트라디올/메드록시프로게스테론아세테이트 | 1.44 (1.09–1.89)* | ||
| 에스트라디올/디드로게스테론 1일 1mg 이하 1일 1mg 이상 | 1.18 (0.98–1.42) 1.12 (0.90–1.40) 1.34 (0.94–1.90) | ||
| 에스트라디올/노레스티론 1일 1mg 이하 1일 1mg 이상 | 1.68 (1.57–1.80)* 1.38 (1.23–1.56)* 1.84 (1.69–2.00)* | ||
| 에스트라디올/노르게스트렐 또는 에스트라디올/드로스피레논 | 1.42 (1.00–2.03) | ||
| 복합 에스트로겐/메드록시프로게스테론 아세테이트 | 2.10 (1.92–2.31)* | ||
| 켤레 에스트로겐/노르게스트렐 0.625mg/일 0.625mg/일 | 1.73 (1.57–1.91)* 1.53 (1.36–1.72)* 2.38 (1.99–2.85)* | ||
| 티볼론만 | 1.02 (0.90–1.15) | ||
| 랄록시펜 단독 | 1.49 (1.24–1.79)* | ||
| 경피 | 에스트라디올 단독 하루 50μg 이하 하루 50μg 이상 | 0.96 (0.88–1.04) 0.94 (0.85–1.03) 1.05 (0.88–1.24) | |
| 에스트라디올/프로게스토겐 | 0.88 (0.73–1.01) | ||
| 질내 | 에스트라디올 단독 | 0.84 (0.73–0.97) | |
| 켤레 에스트로겐만 | 1.04 (0.76–1.43) | ||
| 복합 산아 제한 | 오랄 | 에티닐에스트라디올/노레스티론 | 2.56 (2.15–3.06)* |
| 에티닐에스트라디올/레보노르게스트렐 | 2.38 (2.18–2.59)* | ||
| 에티닐에스트라디올/노르게스티메이트 | 2.53 (2.17–2.96)* | ||
| 에티닐에스트라디올/데소게스트렐 | 4.28 (3.66–5.01)* | ||
| 에티닐에스트라디올/게스토덴 | 3.64 (3.00–4.43)* | ||
| 에티닐에스트라디올/드로스피레논 | 4.12 (3.43–4.96)* | ||
| 아세트산 에티닐에스트라디올/시프로테론 | 4.27 (3.57–5.11)* | ||
| 참고: (1) QResearch 및 임상 프랙티스 연구 데이터링크(CPRD) 데이터베이스의 데이터를 기반으로 한 사례-대조군 연구(2015, 2019). (2) 생물학적 프로게스테론은 포함되지 않았지만 에스트로겐에만 관련된 추가 위험은 없는 것으로 알려져 있다.각주: * = 통계적으로 유의합니다(p < 0.01).출처:"템플릿"을 참조해 주세요. | |||
스트로크
폐경 [36]후 5년 이내에 치료를 시작하면 HRT 관련 뇌졸중의 가능성이 없고, 비구강 [8]경로로 인해 관련성이 없거나 예방적이라는 여러 연구가 있다.WHI에 개입하는 동안 허혈성 뇌졸중 위험이 증가했으며, 치료 중단[26] 후 유의미한 영향이 없었고 장기적인 사후 [6]추적 조사에서는 사망률에 차이가 없었다.경구 합성 에스트로겐 또는 에스트로겐-프로게스토겐 복합 치료가 폐경으로부터 5년까지 지연될 때, 스웨덴 여성의 코호트 연구는 출혈과 허혈성 [36]뇌졸중과의 연관성을 시사했다.덴마크 여성의 또 다른 대규모 코호트는 경구 에스트로겐이 뇌졸중의 위험을 증가시켰지만 피부를 통한 흡수는 전혀 영향을 주지 않았고 질 에스트로겐은 실제로 위험을 [8]감소시켰다는 것을 발견하면서 투여의 구체적인 경로가 중요하다고 제안했다.
자궁내막암

폐경 후 여성의 경우 에스트로겐과 프로게스틴을 지속적으로 조합하면 자궁내막암 [37]발생률이 감소한다.프로게스토겐 치료 기간은 자궁내막 [38]질환을 예방하기 위해 사이클당 최소 14일이어야 한다.
자궁내막암은 호르몬 대체의 맥락에서 두 가지 형태로 분류되었다.타입 1은 가장 흔하고 에스트로겐 치료와 연관될 수 있으며 보통 낮은 등급입니다.타입 2는 에스트로겐 자극과 관련이 없으며 보통 더 높고 [39]예후가 좋지 않다.에스트로겐 치료로 자궁내막암으로 이어지는 자궁내막과형성은 프로게스토겐의 [39]병용 투여로 예방할 수 있다.1970년대에 산아제한을 위해 고용량 에스트로겐을 광범위하게 사용한 것은 제1형 자궁내막암의 [40]발생률을 크게 증가시킨 것으로 생각된다.
역설적으로, 프로게스토겐은 자궁 섬유질의 성장을 촉진하고, HRT를 시작하기 전에 골반 초음파를 시행하여 자궁이나 자궁내막의 기초적인 [39]병변이 없음을 확인할 수 있습니다.
안드로겐은 폐경 후 여성의 자궁내막 증식을 자극하지 않으며 에스트로겐에 의해 유발되는 증식을 어느 [41]정도 억제하는 것으로 보인다.
자궁내막암 [42]치료 후 호르몬 대체요법을 고려하는 여성에게 알릴 수 있는 양질의 증거가 불충분합니다.
유방암
유방암과 호르몬 대체의 연관성에 대한 연구는 일관성이 없고 폐경 이후 교체의 유형과 시기에 따라 다르다.리스크 증가를 시사하는 평가도 있지만,[43] 리스크가 감소하는 평가도 있습니다.이러한 효과의 불일치는 유방암 [27]위험에 대한 HRT의 의미 있는 영향의 부족을 암시하는 것으로 제시되었다.
합성 프로게스테론에 [6]의한 호르몬 대체 요법의 유방암 발생률이 통계적으로 유의하지 않다.생물학적 프로게스테론을 [44]사용하면 위험을 줄일 수 있지만, 대조군 내 유방암의 희귀성으로 인해 효과가 낮다고 시사하는 유일한 선행 연구는 있었다.2018년 [43]현재 무작위 대조 실험은 없습니다.유방암의 상대적 위험은 또한 폐경과 HRT 사이의 간격과 합성 프로게스틴 [45][46]투여 경로에 따라 달라집니다.
여성건강구상 참가자들의 가장 최근의 후속조사는 에스트로겐을 메드록시-프로게스테론과 [47]함께 복용하면 상대적 위험이 증가했지만, 자궁 절제 후 참가자들에게서 유방암 발병률이 낮다는 것을 보여주었다.에스트로겐은 질 출혈과 자궁암의 위험이 증가하기 때문에 자궁 절제술 환경에서만 단독으로 투여된다.[48][49]
HRT는 하체질량지수(BMI)를 가진 여성에게서 유방암 위험과 더 강하게 연관되어 왔다.체질량지수([50]BMI)가 25 이상인 유방암 관련성은 발견되지 않았다.이러한 연구 중 일부에서 유의한 효과가 없는 것은 보다 높은 베이스라인 에스트론을 가진 과체중 여성에 대한 선택적 처방 또는 경구 투여 후 매우 낮은 프로게스테론 혈청 수치로 인해 높은 종양 불활성화율이 [51]초래되는 것일 수 있다는 일부의 제안이 있었다.
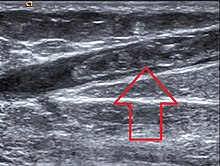
유방조영술을 사용하여 HRT에 대한 유방조직 밀도의 반응을 평가하는 것은 치료와 관련된 유방암 위험의 정도를 평가하는 데 도움이 되는 것으로 보인다. 치밀하거나 밀도가 혼합된 유방조직을 가진 여성은 저밀도 [52]조직을 가진 여성보다 유방암에 걸릴 위험이 더 높다.
미크론화된 프로게스테론은 5년 미만으로 사용했을 때 유방암 위험과 관련이 없는 것으로 보이며,[53] 장기간 사용했을 때 위험이 증가했음을 시사하는 제한된 데이터도 있다.
Richard Neapolitan의 회고적 Cox 비례 위험 분석은 결합 말 에스트로겐 사용만으로 유방암 위험 감소를 지지했지만, 또한 메드록시프로게스테론 아세테이트가 포함된 결합 말 에스트로겐이 유방암 위험 감소와 관련이 있으며 생체동일 호르몬 치료법이 유사하지 않음을 시사했다.통계적으로 유의한 [43]효과가 있는 테드.유방암에 [54]관한 두 가지 투여 경로를 비교하는 사전 무작위 임상시험은 없었다.
유방암에 걸린 적이 있는 여성의 경우, 우선 골다공증에 대한 비스포네이트나 선택적 에스트로겐 수용체 조절제(SERM), 심혈관 질환에 대한 콜레스테롤 강하제와 아스피린, 국소 증상에 대한 질 에스트로겐과 같은 갱년기 효과를 위한 다른 선택지를 고려할 것을 권고한다.유방암 후 전신 HRT에 대한 관찰 연구는 일반적으로 안심이 된다.유방암 후 HRT가 필요한 경우, 에스트로겐 전용 치료나 프로게스토겐을 사용한 에스트로겐 치료가 결합된 [55]전신 치료보다 더 안전할 수 있습니다.BRCA1 또는 BRCA2 돌연변이 보균자인 여성에서 HRT는 유방암 [56]위험에 영향을 미치지 않는 것으로 보인다.정기적인 검사 유방 촬영도 받는 HRT를 사용하는 여성의 상대적 수는 HRT를 사용하지 않는 여성보다 높다. HRT는 두 [57]그룹의 유방암 검출률이 다른 요인으로 제시되고 있다.
안드로겐 치료와 함께, 대부분의 역학 연구는 양성 [58]연관성을 시사하지만, 사전 임상 연구는 유방 조직에 대한 억제 효과를 제시했다.
| 테라피 | 5년 미만 | 5~14년 | 15년 이상 | |||
|---|---|---|---|---|---|---|
| 경우들 | RR (95% CI) | 경우들 | RR (95% CI) | 경우들 | RR (95% CI) | |
| 에스트로겐만 | 1259 | 1.18 (1.10–1.26) | 4869 | 1.33 (1.28–1.37) | 2183 | 1.58 (1.51–1.67) |
| 에스트로겐에 의해 | ||||||
| 켤레 에스트로겐 | 481 | 1.22 (1.09–1.35) | 1910 | 1.32 (1.25–1.39) | 1179 | 1.68 (1.57–1.80) |
| 에스트라디올 | 346 | 1.20 (1.05–1.36) | 1580 | 1.38 (1.30–1.46) | 435 | 1.78 (1.58–1.99) |
| 에스트로피네이트(에스트론 황산염) | 9 | 1.45 (0.67–3.15) | 50 | 1.09 (0.79–1.51) | 28 | 1.53 (1.01–2.33) |
| 에스트리올 | 15 | 1.21 (0.68–2.14) | 44 | 1.24 (0.89–1.73) | 9 | 1.41 (0.67–2.93) |
| 기타 에스트로겐 | 15 | 0.98 (0.46–2.09) | 21 | 0.98 (0.58–1.66) | 5 | 0.77 (0.27–2.21) |
| 노선별 | ||||||
| 구강 에스트로겐 | – | – | 3633 | 1.33 (1.27–1.38) | – | – |
| 경피 에스트로겐 | – | – | 919 | 1.35 (1.25–1.46) | – | – |
| 질에스트로겐류 | – | – | 437 | 1.09 (0.97–1.23) | – | – |
| 에스트로겐 및 프로게스토겐 | 2419 | 1.58 (1.51–1.67) | 8319 | 2.08 (2.02–2.15) | 1424 | 2.51 (2.34–2.68) |
| 프로게스토겐별 | ||||||
| (Levo)노르게스트렐 | 343 | 1.70 (1.49–1.94) | 1735 | 2.12 (1.99–2.25) | 219 | 2.69 (2.27–3.18) |
| 아세트산노레티스테론 | 650 | 1.61 (1.46–1.77) | 2642 | 2.20 (2.09–2.32) | 420 | 2.97 (2.60–3.39) |
| 아세트산메드록시프로게스테론 | 714 | 1.64 (1.50–1.79) | 2012 | 2.07 (1.96–2.19) | 411 | 2.71 (2.39–3.07) |
| 디드로게스테론 | 65 | 1.21 (0.90–1.61) | 162 | 1.41 (1.17–1.71) | 26 | 2.23 (1.32–3.76) |
| 프로게스테론 | 11 | 0.91 (0.47–1.78) | 38 | 2.05 (1.38–3.06) | 1 | – |
| 프로메게스톤 | 12 | 1.68 (0.85–3.31) | 19 | 2.06 (1.19–3.56) | 0 | – |
| 아세트산노메스트롤 | 8 | 1.60 (0.70–3.64) | 14 | 1.38 (0.75–2.53) | 0 | – |
| 기타 프로게스토겐 | 12 | 1.70 (0.86–3.38) | 19 | 1.79 (1.05–3.05) | 0 | – |
| 프로게스토겐 주파수별 | ||||||
| 계속되는 | – | – | 3948 | 2.30 (2.21–2.40) | – | – |
| 간헐적 | – | – | 3467 | 1.93 (1.84–2.01) | – | – |
| 프로게스토겐만 | 98 | 1.37 (1.08–1.74) | 107 | 1.39 (1.11–1.75) | 30 | 2.10 (1.35–3.27) |
| 프로게스토겐별 | ||||||
| 아세트산메드록시프로게스테론 | 28 | 1.68 (1.06–2.66) | 18 | 1.16 (0.68–1.98) | 7 | 3.42 (1.26–9.30) |
| 아세트산노레티스테론 | 13 | 1.58 (0.77–3.24) | 24 | 1.55 (0.88–2.74) | 6 | 3.33 (0.81–13.8) |
| 디드로게스테론 | 3 | 2.30 (0.49–10.9) | 11 | 3.31 (1.39–7.84) | 0 | – |
| 기타 프로게스토겐 | 8 | 2.83 (1.04–7.68) | 5 | 1.47 (0.47–4.56) | 1 | – |
| 여러가지 종류의 | ||||||
| 티볼론 | – | – | 680 | 1.57 (1.43–1.72) | – | – |
| 비고: 폐경호르몬 치료와 유방암 위험에 대한 전세계 역학 증거의 메타분석(CGHFBC)갱년기 호르몬 치료제의 현재 사용 여부와 사용 안 함에 대한 상대 위험도를 완전히 조정했습니다.출처:"템플릿"을 참조해 주세요. | ||||||
| 스터디 | 테라피 | 위험비(95%) |
|---|---|---|
| E3N-EPIC: Fournier 등(2005) | 에스트로겐만 | 1.1 (0.8–1.6) |
| 에스트로겐 플러스 프로게스테론 경피 에스트로겐 경구 에스트로겐 | 0.9 (0.7–1.2) 0.9 (0.7–1.2) 이벤트 없음 | |
| 에스트로겐 플러스 프로게스틴 경피 에스트로겐 경구 에스트로겐 | 1.4 (1.2–1.7) 1.4 (1.2–1.7) 1.5 (1.1–1.9) | |
| E3N-EPIC: Fournier 등(2008) | 경구 에스트로겐만 | 1.32 (0.76–2.29) |
| 경구 에스트로겐 플러스 프로게스토겐 프로게스테론 디드로게스테론 메드로게스톤 클로르마디논아세테이트 아세트산 시프로테론 프로메게스톤 아세트산노메스트롤 아세트산노레티스테론 아세트산메드록시프로게스테론 | 분석되지a 않음 0.77 (0.36–1.62) 2.74 (1.42–5.29) 2.02 (1.00–4.06) 2.57 (1.81–3.65) 1.62 (0.94–2.82) 1.10 (0.55–2.21) 2.11 (1.56–2.86) 1.48 (1.02–2.16) | |
| 경피 에스트로겐만 | 1.28 (0.98–1.69) | |
| 경피 에스트로겐 플러스 프로게스토겐 프로게스테론 디드로게스테론 메드로게스톤 클로르마디논아세테이트 아세트산 시프로테론 프로메게스톤 아세트산노메스트롤 아세트산노레티스테론 아세트산메드록시프로게스테론 | 1.08 (0.89–1.31) 1.18 (0.95–1.48) 2.03 (1.39–2.97) 1.48 (1.05–2.09) 분석되지a 않음 1.52 (1.19–1.96) 1.60 (1.28–2.01) 분석되지a 않음 분석되지a 않음 | |
| E3N-EPIC: Fournier 외 (2014) | 에스트로겐만 | 1.17 (0.99–1.38) |
| 에스트로겐 플러스 프로게스테론 또는 디드로게스테론 | 1.22 (1.11–1.35) | |
| 에스트로겐 플러스 프로게스틴 | 1.87 (1.71–2.04) | |
| CECILLE: Cordina-Duverger 외 (2013) | 에스트로겐만 | 1.19 (0.69–2.04) |
| 에스트로겐+프로게스토겐 프로게스테론 프로게스틴 프로게스테론 유도체 테스토스테론 유도체 | 1.33 (0.92–1.92) 0.80 (0.44–1.43) 1.72 (1.11–2.65) 1.57 (0.99–2.49) 3.35 (1.07–10.4) | |
| 각주: = 분석되지 않음, 5건 미만.출처:"템플릿"을 참조해 주세요. | ||
| 스터디 | 테라피 | 위험비(95%) |
|---|---|---|
| E3N-EPIC: Fournier 등(2005년)a | 경피 에스트로겐 플러스 프로게스테론 2년 미만 2 ~ 4년 years4년 | 0.9 (0.6–1.4) 0.7 (0.4–1.2) 1.2 (0.7–2.0) |
| 경피 에스트로겐 플러스 프로게스틴 2년 미만 2 ~ 4년 years4년 | 1.6 (1.3–2.0) 1.4 (1.0–1.8) 1.2 (0.8–1.7) | |
| 경구 에스트로겐 플러스 프로게스틴 2년 미만 2 ~ 4년 years4년 | 1.2 (0.9–1.8) 1.6 (1.1–2.3) 1.9 (1.2–3.2) | |
| E3N-EPIC: Fournier 등(2008) | 에스트로겐 플러스 프로게스테론 2년 미만 2 ~ 4년 4 ~ 6년 years6년 | 0.71 (0.44–1.14) 0.95 (0.67–1.36) 1.26 (0.87–1.82) 1.22 (0.89–1.67) |
| 에스트로겐+디드로게스테론 2년 미만 2 ~ 4년 4 ~ 6년 years6년 | 0.84 (0.51–1.38) 1.16 (0.79–1.71) 1.28 (0.83–1.99) 1.32 (0.93–1.86) | |
| 에스트로겐 및 기타 프로게스토겐 2년 미만 2 ~ 4년 4 ~ 6년 years6년 | 1.36 (1.07–1.72) 1.59 (1.30–1.94) 1.79 (1.44–2.23) 1.95 (1.62–2.35) | |
| E3N-EPIC: Fournier 외 (2014) | 에스트로겐 플러스 프로게스테론 또는 디드로게스테론 5년 미만 years5년 | 1.13 (0.99–1.29) 1.31 (1.15–1.48) |
| 에스트로겐 및 기타 프로게스토겐 5년 미만 years5년 | 1.70 (1.50–1.91) 2.02 (1.81–2.26) | |
| 각주 = 경구 에스트로겐 플러스 프로게스테론은 이 요법을 사용하는 여성의 수가 적기 때문에 분석되지 않았다.출처:"템플릿"을 참조해 주세요. | ||
난소암
HRT는 난소암 위험 증가와 관련이 있으며,[59] HRT를 사용하는 여성들은 사용자 1,000명당 약 1명의 난소암 환자가 추가로 발생한다.이 위험은 에스트로겐만 투여하는 것이 아니라 프로게스토겐 치료를 병행할 때 감소하며 HRT를 [60]중단한 후 시간이 지날수록 감소한다.특정 아형에 대해서는 장액암의 위험이 높을 수 있으나 명확한 세포, 자궁내막암,[60] 점액성 난소암과의 관련성은 없다.난소를 외과적으로 제거한 후 난소암 생존자에게 호르몬 치료를 하는 것은 일반적으로 생존율을 [61]높이는 것으로 여겨진다.
기타 악성종양
대장암
WHI에서 에스트로겐-프로게스테론 복합 치료를 받은 여성들은 대장암에 걸릴 위험이 낮았다.그러나 호르몬을 [62]섭취하지 않은 여성에게서 대장암보다 림프절이나 먼 곳에 암이 전이됐을 가능성이 높았다.대장암 생존자의 경우 HRT를 사용하면 재발 위험과 전체 [63]사망률이 낮아지는 것으로 생각됩니다.
자궁경부암
HRT로 치료된 폐경 후 여성의 자궁경부 스쿼모스 세포암 위험이 유의미하게 감소하고 선암은 약하게 증가하는 것으로 보인다.자궁경부암 [64]생존자에게 HRT를 사용할 때 재발 위험이 높아진다는 연구는 없다.
성기능
HRT는 폐경과 함께 발생할 수 있는 성욕 부족과 성기능 장애를 도울 수 있다.40세에서 69세 사이의 여성들에 대한 역학 조사에 따르면 여성의 75%가 [4]폐경 후에도 여전히 성적으로 활동적이다.수명이 늘어남에 따라, 오늘날 여성들은 건강한 성생활이 [65]삶의 질에 필수적인 기간인 폐경 후 상태에서 삶의 3분의 1 이상을 살고 있다.
성욕 감소와 성기능 장애는 폐경 후 여성들에게 흔한 문제이며, 이는 저활동성 성욕 장애로 언급되며, 그 징후와 증상 모두 HRT에 [5][66]의해 개선될 수 있다.이 기간 동안 에스트로겐의 감소와 모낭 자극 호르몬의 증가를 포함한 몇 가지 호르몬 변화가 일어난다.대부분의 여성들의 경우, 변화의 대부분은 폐경 후기와 폐경 [4]후기에 일어난다.성호르몬결합글로불린(SHBG)과 인히빈(A와 B)의 감소도 일어난다.테스토스테론은 남성보다 낮은 수준의 여성들에게 존재하며, 30세에 정점을 찍고 나이가 들면서 점차 감소한다; 에스트로겐과 프로게스테론에 [4]비해 갱년기 전환기에는 변화가 적다.
세계적인 합의된 입장 성명은 폐경 전 수준의 테스토스테론 대체가 HSDD에 효과적일 수 있다고 조언했다.그러나 테스토스테론 치료에 대한 안전 정보는 2년간의 지속적인 치료 이후로는 이용할 수 없으며 생리학적 수준 이상의 복용은 [31]권장되지 않는다.폐경 후 여성의 [67]성욕을 회복시키는 테스토스테론 패치가 발견되었다.대부분의 실험에서는 여성들이 동반 에스트로겐과 프로게스테론을 복용하고 테스토스테론 치료 자체는 비교적 기간이 짧은 가운데 테스토스테론 대체가 심장병인 유방암에 미치는 영향을 평가할 수 있는 자료가 충분하지 않다.이 제한된 데이터의 설정에서 테스토스테론 치료는 부작용과 [31]관련이 없다.
모든 여성들이 반응하는 것은 아니다. 특히 기존의 성적 [22]문제가 있는 여성들이 그렇다.에스트로겐 대체는 질 세포, pH 수치, 그리고 질로의 혈류를 회복시킬 수 있는데, 이 모든 것들은 폐경이 시작되면 악화되는 경향이 있다.섹스에 대한 고통이나 불편함은 [22]에스트로겐에 가장 반응하는 성분으로 보인다.그것은 또한 [22]요로에 긍정적인 영향을 미치는 것으로 나타났다.에스트로겐은 질 위축을 줄이고 성적 흥분, 빈도 및 오르가즘을 [22]증가시킬 수 있다.
호르몬 대체의 효과는 장기 복용 [22]후 일부 여성들에게서 떨어질 수 있다.에스트로겐/안드로겐 대체 요법의 복합적인 효과가 에스트로겐에 대해서만 [22]성욕과 각성을 증가시킬 수 있다는 것도 많은 연구에서 밝혀졌습니다.유럽에서 이용 가능한 에스트로겐, 안드로겐, 그리고 프로게스토제닉 특성을 가진 합성 스테로이드인 티볼론은 기분, 성욕, 그리고 신체 증상학을 개선할 수 있는 능력을 가지고 있습니다.다양한 위약 대조 연구에서 혈관 운동 증상, 감정 반응, 수면 장애, 신체적 증상 및 성욕의 개선이 관찰되었지만, 그것은 또한 기존의 [5]HRT와 유사한 위험 프로파일을 가지고 있다.
신경변성 장애
예방을 위해, WHI는 HRT가 65세 이후에 시작되면 치매의 위험을 증가시킬 수 있지만, 50세에서 55세 [26]사이의 사람들에 대해서는 중립적인 결과를 보이거나 신경 보호 효과가 있다고 제안했다.폐경기 주변에서의 다른 연구들은 HRT가 지속적으로 알츠하이머의 낮은 [68][69]위험과 관련이 있다는 것을 보여주었다.파킨슨병의 경우 대부분의 임상 및 역학 연구는 연관성이[70][71] 없거나 [68][72]결정적인 결과를 보여주지 못하고 있다.덴마크의 한 연구는 주기적 투여 [73]일정에서 HRT와 함께 파킨슨병에 걸릴 위험이 증가함을 시사했다.
치료와 관련하여, 무작위 임상시험에 따르면 HRT는 폐경 후 여성의 치매 맥락 밖에서 무증상 및 경도 인지장애 [74][75][76]양쪽에서 실행 및 주의 과정을 개선한다.에스트로겐 대체는 파킨슨병에 걸린 폐경 후 여성의 운동 증상과 일상 생활 활동을 개선하며 UPDRS 점수가 크게 [77]향상되는 것으로 보인다.또한 임상시험에서는 [78]폐경 후 여성의 언어학습과 기억력의 통계적으로 유의한 작은 개선과 관련된 테스토스테론 대체가 나타났다.DHEA는 [32]폐경기 이후 인지능력이 향상되는 것으로 발견되지 않았다.임상 전 연구에 따르면 내인성 에스트로겐과 테스토스테론은 신경 보호 작용을 하며 뇌 아밀로이드 [79][80]증착을 예방할 수 있다.
근육과 뼈
치료 중 고관절 골절 위험이 유의미하게 감소하여 HRT를 [26][81]중단한 후에도 덜 지속됩니다.그것은 또한 콜라겐 형성을 도와 추간판 및 [82]골력을 향상시킨다.
호르몬 대체 요법은 에스트로겐과 안드로겐의 형태로 [83]근육에 대한 노화의 영향을 되돌리는 데 효과적일 수 있다.테스토스테론이 낮을수록 골밀도가 낮아지고 유리테스토스테론이 높을수록 [32]고관절 골절률이 낮아진다.성기능 저하를 위해 사용될 수 있는 테스토스테론 치료는 또한 골밀도와 근육량을 [31]증가시킬 수 있다.
부작용
HRT의 부작용은 다양한 빈도로 발생하며 다음을 포함합니다.[84]
흔한
금지 사항
다음으로 [86]HRT에 대한 절대적 및 상대적인 금기를 나타냅니다.
절대 금기 사항
상대적 금기 사항
- 편두통
- 유방암의 역사
- 난소암 병력
- 정맥혈전증
- 자궁 섬유종의 역사
- 유방의 비정형 덕트 과형성
- 활동성 담낭질환(담낭염, 담낭염)
- 잘 분화되고 초기 자궁내막암 - 일단 악성종양 치료가 완료되면, 더 이상 절대 금기가 아니다.
역사와 연구
임신한 암말의 소변에서 CEE를 추출한 것이 1942년 도입된 [87][88]초기 형태의 에스트로겐 중 하나인 프레마린의 시판으로 이어졌다.그 때부터 1970년대 중반까지 에스트로겐은 보조 프로게스토겐 없이 투여되었다.1975년부터, 연구들은 프로게스토겐이 없다면, 프레마린에 의한 저항 없는 에스트로겐 치료는 자궁내막암의 위험을 8배 증가시켰고, 결국 프레마린의 판매가 [87]급감하게 만들었다는 것을 보여주기 시작했다.1980년대 초에 에스트로겐에 프로게스토겐을 첨가하면 자궁내막의 [87]위험을 줄일 수 있다는 것이 인식되었다.이는 에스트로겐-프로게스토겐 복합 치료법의 개발로 이어졌으며, 가장 일반적으로 켤레 말 에스트로겐(Premarin)과 메드록시프로게스테론(Provera)[87]의 조합으로 이루어졌다.
트라이얼
Women's Health Initiative 시험은 1991년과 2006년 사이에 실시되었으며, 건강한 [87]여성에 대한 최초의 대규모 이중맹검 위약 대조 임상 시험이었다.호르몬 치료 기간 동안 침습성 유방암, 뇌졸중, 폐결핵이 증가한다는 것을 암시하는 그들의 결과는 긍정적이기도 하고 부정적이기도 했다.다른 위험에는 자궁내막암, 담낭질환, 요실금의 증가가 포함되지만, 이점에는 고관절 골절 감소, 당뇨병 발병률 감소, 혈관운동 증상 개선이 포함됩니다.65세 이상의 여성에게서 HRT와 함께 치매에 걸릴 위험이 증가하지만, 젊은 나이에는 신경 보호 효과가 있는 것으로 보인다.HRT가 중단된 후에도 WHI는 참가자를 계속 관찰했고 유방암 위험의 일부 상승이 지속되었지만 [26]이러한 위험과 편익의 대부분이 소멸된 것을 발견했다.다른 연구들 또한 [60]난소암의 위험성을 증가시켰다고 시사했다.
에스트로겐과 프로게스틴의 병용 치료를 받고 있는 WHI의 부문은 2002년 건강 위험의 인식으로 인해 데이터 모니터링 위원회(DMC)에 의해 조기 폐쇄되었다. 그러나 이는 위험의 증가를 시사하는 데이터가 명백해진 후 1년 만에 발생했다.2004년에는 자궁 절제 후 환자가 단독으로 에스트로겐으로 치료를 받는 WHI의 팔도 DMC에 의해 폐쇄되었다. 임상 의료 관행은 HRT에 대한 두 개의 병행 여성 건강 이니셔티브(WHI) 연구에 기초하여 바뀌었다.이전의 연구는 더 적었고, 많은 여성들이 호르몬 치료를 선택적으로 받았다.병행 연구들 중 한 부분은 평균 5.2년 동안 16,000명 이상의 여성들을 추적했고, 그들 중 절반은 위약을 복용했고, 나머지 절반은 CEEs와 MPAs를 함께 복용했다.이 WHI 에스트로겐-플러스-프로게스틴 실험은 예비 결과가 CEE와 프로게스틴의 결합 위험이 그들의 이익을 초과한다는 것을 시사했기 때문에 2002년에 조기 중단되었다.중단된 WHI 에스트로겐-플러스-프로게스틴 연구에 대한 첫 보고서는 2002년 [89]7월에 나왔다.
2002년 WHI의 초기 데이터에 따르면 HRT가 50세에서 59세 사이에 시작되었을 때는 사망률이 낮았지만 60세 이후에 시작되었을 때는 사망률이 더 높았다.고령 환자에서는 대장암과 골절 발생률이 감소했지만 유방암, 심장마비, 정맥혈전증, 뇌졸중의 발생률이 명백하게 증가하였다.당시 WHI는 비수술적 폐경이 있는 여성들에게 관련 [89]위험을 최소화하기 위해 가능한 한 짧은 시간 동안 가장 낮은 양의 HRT를 복용할 것을 권고했다.WHI의 발견 중 일부는 백만 여성 연구로 알려진 영국에서 수행된 더 큰 규모의 국가 연구에서 다시 발견되었다.그 결과 HRT를 복용하는 여성의 수는 [90]급격히 감소했다.2012년, 미국 예방 태스크 포스(USPSTF)는 에스트로겐과 프로게스틴 요법의 폐해가 만성 질환 예방 [91][92]혜택을 초과할 가능성이 높다고 결론지었다.
폐경 후 여성의 HRT와 함께 첫 번째 WHI 추적 연구가 발표된 2002년에는 노년층 및 젊은 연령층 모두 유방암 발병률이 약간 높았고, 젊은 참가자는 아니지만 노년층 환자에서 심장마비와 뇌졸중이 모두 증가했다.유방암은 에스트로겐과 프로게스틴으로 치료받은 여성에게서 증가했지만 에스트로겐과 프로게스테론 또는 에스트로겐만으로는 증가하지 않았다.자궁이 자궁내막에 대한 증식 효과로 인해 자궁이 아직 존재하는 경우, 무저항 에스트로겐(즉 프로게스토겐 없이 에스트로겐 단독)에 의한 치료는 금지된다.WHI는 또한 에스트로겐과 프로게스토겐을 함께 사용했을 때 대장암 발생률이 감소했으며, 가장 중요한 것은 골절 발생률이 감소했다는 것을 발견했다.결국, 연구는 HRT가 50-59세 사이에 시작되었을 때 사망률이 낮았지만 60세 이후에 시작되었을 때 사망률이 더 높다는 것을 알게 되면서 HRT에 대한 이질적인 결과를 발견했다.이 연구의 저자들은 [89]비수술적 폐경이 있는 여성들은 위험을 최소화하기 위해 가장 짧은 시간 동안 가능한 최소량의 호르몬을 섭취할 것을 권고했다.
WHI에 의해 발표된 데이터는 보충 에스트로겐이 정맥 혈전 색전증과 유방암의 위험을 증가시켰지만 골다공증과 대장암에 대한 보호 효과가 있는 반면 심혈관 질환에 대한 영향은 [93]혼합되었다.이러한 결과는 나중에 영국에서 시행된 실험에서는 입증되었지만 프랑스와 중국에서 시행된 보다 최근의 연구에서는 입증되지 않았다.유전자 다형은 [94][95]폐경 후 여성의 HRT에 대한 대사 반응의 개인 간 변동과 관련이 있는 것으로 보인다.
| 임상 결과 | 가설화 리스크에 대한 영향 | 에스트로겐 및 프로게스토겐 (CEs0.625mg/일 + 2.5mg/일) (n = 16,608(자궁 포함), 5.2~5.6년 경과) | 에스트로겐만 (CEs0.625mg/일 p.o.) (n = 10,739, 자궁 없음, 6.8-7.1년 경과) | ||||
|---|---|---|---|---|---|---|---|
| HR | 95% CI | AR | HR | 95% CI | AR | ||
| 관상 동맥 심장병 | 감소. | 1.24 | 1.00–1.54 | +6/10,000 PY | 0.95 | 0.79–1.15 | - 3 / 10,000 PY |
| 스트로크 | 감소. | 1.31 | 1.02–1.68 | +8/10,000 PY | 1.37 | 1.09–1.73 | +12/10,000 PY |
| 폐색전증 | 증가된 | 2.13 | 1.45–3.11 | +10/10,000 PY | 1.37 | 0.90–2.07 | +4 / 10,000 PY |
| 정맥혈전색전증 | 증가된 | 2.06 | 1.57–2.70 | +18/10,000 PY | 1.32 | 0.99–1.75 | +8/10,000 PY |
| 유방암 | 증가된 | 1.24 | 1.02–1.50 | +8/10,000 PY | 0.80 | 0.62–1.04 | - 6 / 10,000 PY |
| 대장암 | 감소. | 0.56 | 0.38–0.81 | - 7 / 10,000 PY | 1.08 | 0.75–1.55 | +1 / 10,000 PY |
| 자궁내막암 | – | 0.81 | 0.48–1.36 | - 1 / 10,000 PY | – | – | – |
| 고관절 골절 | 감소. | 0.67 | 0.47–0.96 | - 5 / 10,000 PY | 0.65 | 0.45–0.94 | - 7 / 10,000 PY |
| 총 골절 | 감소. | 0.76 | 0.69–0.83 | - 47 / 10,000 PY | 0.71 | 0.64–0.80 | - 53 / 10,000 PY |
| 총사망률 | 감소. | 0.98 | 0.82–1.18 | - 1 / 10,000 PY | 1.04 | 0.91–1.12 | +3/10,000 PY |
| 글로벌 인덱스 | – | 1.15 | 1.03–1.28 | +19/10,000 PY | 1.01 | 1.09–1.12 | +2 / 10,000 PY |
| 당뇨병 | – | 0.79 | 0.67–0.93 | 0.88 | 0.77–1.01 | ||
| 담낭병 | 증가된 | 1.59 | 1.28–1.97 | 1.67 | 1.35–2.06 | ||
| 스트레스성 요실금 | – | 1.87 | 1.61–2.18 | 2.15 | 1.77–2.82 | ||
| 요실금을 촉진하다 | – | 1.15 | 0.99–1.34 | 1.32 | 1.10–1.58 | ||
| 말초동맥질환 | – | 0.89 | 0.63–1.25 | 1.32 | 0.99–1.77 | ||
| 치매 가능성 | 감소. | 2.05 | 1.21–3.48 | 1.49 | 0.83–2.66 | ||
| 약어: CES = 켤레 에스트로겐.MPA = 메드록시프로게스테론 아세테이트. 경구당 p.o. =HR = 위험비.AR = 귀책 위험.PYs = 인년.CI = 신뢰 구간입니다.주의:샘플 크기(n)에는 환자의 절반 정도였던 위약 수용자가 포함된다."글로벌 지수"는 각 여성에 대해 관상동맥 질환, 뇌졸중, 폐색전증, 유방암, 대장암, 자궁내막암(에스트로겐+프로게스토겐 그룹만 해당), 고관절 골절 및 기타 원인으로 인한 사망에 대한 가장 빠른 진단 시간으로 정의된다.출처:"템플릿"을 참조해 주세요. | |||||||
WHI는 유방암, 관상동맥 심장병, 뇌졸중, 폐색전증 발병률이 통계적으로 유의미하다고 보고했다.이 연구는 또한 고관절 골절과 대장암 발병률에서 통계적으로 유의한 감소를 발견했다.2002년 연구가 중단된 지 1년 뒤 에스트로겐과 프로게스틴이 치매 위험도 [96]높인다는 기사가 발표됐다.연구의 결론은 HRT 조합이 측정된 유익성보다 더 큰 위해성을 제시한다는 것이었다.그 결과는 거의 보편적으로 연구된 CEE와 MPA의 특정 독점적 조합인 Prempro가 아니라 HRT 전반에 관련된 위험과 문제로 보고되었다.
2002년 첫 번째 WHI 결과에서 발견된 혈전이 증가한 것으로 보고된 후, 채워진 Prempro 처방 건수는 거의 절반으로 감소했습니다.WHI 결과에 따라 HRT 사용자 중 많은 비율이 이 중 하나를 선택했고, 그 후 유방암 발생률이 급격히 떨어졌습니다.유방암 발병률의 감소는 그 후 몇 [97]년 동안 계속되어 왔다.연구자들은 복합호르몬이 기존의 호르몬 치료와 [98]크게 다르지 않다고 주장했지만, 알려지지 않은 수의 여성들이 복합 생체동일 호르몬과 같은 Prempro의 대체제를 복용하기 시작했다.
병행연구의 다른 부분은 자궁절제 후 위약 프로게스토겐 또는 CEEs를 단독으로 받은 여성들을 대상으로 했다.이 그룹은 결합 호르몬 연구에서 나타난 위험성을 보여주지 않았으며, 2002년 에스트로겐 전용 연구는 중단되지 않았다.그러나 2004년 2월, 그것 역시 중단되었다.에스트로겐 전용 연구 참가자의 유방암 발병률은 23% 감소했지만,[99] 뇌졸중과 폐색전증의 위험은 주로 60세 이상 HRT를 시작한 환자에서 약간 증가했다.
몇몇 다른 대규모 연구 및 메타 분석에서는 60세 미만 또는 폐경 후 10년 이내에 HRT 사망률이 감소했으며 [100][101][102][103][17][104]60세 이상 여성의 사망률에 대한 논쟁의 여지가 있거나 없는 영향이 보고되었다.
지금까지의 연구는 상당했지만,[105][106][82] 폐경기 이후의 HRT 유형과 기간에 대한 효과의 차이를 완전히 이해하기 위해서는 추가적인 연구가 필요하다.
이용 가능한 폼
인간 스테로이드 호르몬에는 에스트로겐, 프로게스토겐, 안드로겐, 미네랄 코르티코이드, 글루코코르티코이드 등 5가지 주요 호르몬이 있습니다.에스트로겐과 프로게스토겐은 갱년기에 가장 자주 사용되는 두 가지 물질이다.FDA 승인 및 비 FDA의 다양한 제품에서 사용할 수 있다.FDA가 승인한 [9]제제
자궁이 온전한 여성들에게서, 에스트로겐은 거의 항상 프로게스토겐과 함께 투여되는데, 장기간에 걸친 무저항 에스트로겐 치료는 자궁내막 과형성과 자궁내막암의 [1][2]위험 증가와 관련이 있기 때문이다.반대로 자궁 절제술을 받은 여성이나 자궁이 없는 여성에게는 프로게스토겐이 필요 없고 에스트로겐만 사용할 수 있다.에스트로겐과 프로게스토겐을 모두 포함한 많은 조합 제제가 있다.
호르몬 대체의 구체적인 유형은 다음과 같습니다.[1][2]
- 에스트로겐 – 에스트라디올 및 에스트리올과 같은 생물 동질 에스트로겐, 켤레 에스트로겐(CEEs)과 같은 동물 유래 에스트로겐 및 에티닐에스트라디올과 같은 합성 에스트로겐
- 프로게스테론 – 생체동일 프로게스테론 및 메드록시 프로게스테론 아세테이트(MPA), 노르에스티론 및 디드로게스테론 등의 프로게스틴(합성 프로게스테론)
- 안드로겐 – 생체 동질 테스토스테론 및 데히드로에피안드로스테론(DHEA) 및 메틸테스토스테론 및 난드로론 데카노에이트와[107][108] 같은 합성 아나볼릭 스테로이드
티볼론은 유럽에서 살 수 있지만 미국에서는 살 수 없는 합성 의약품으로, 위약보다는 효과가 높지만 폐경 후 여성의 복합 호르몬 치료보다는 효과가 낮다.질 출혈, 자궁내막암, 60세 [109][110]이상 여성의 뇌졸중 위험을 증가시킬 수 있지만 유방암과 대장암의 위험이 감소할 수 있습니다.
질 에스트로겐은 [111]다른 경로에서 전달되는 에스트로겐보다 적은 전신 효과로 국소 위축과 건조를 개선할 수 있습니다.때때로 안드로겐, 일반적으로 테스토스테론은 성욕 [112][113]감퇴를 치료하기 위해 첨가될 수 있다.
연속 대 주기
복용량은 종종 난소 호르몬 주기를 더 가깝게 모방하기 위해 주기적으로 변화하며, 에스트로겐은 매일 복용하고 프로게스토겐은 매달 또는 두 달에 한 번씩 복용한다. 이는 '순환적' 또는 '순차적 결합'이라고 불리는 일정이다.또는 '연속 결합' HRT는 일정한 일일 호르몬 [114]용량으로 제공될 수 있다.연속 결합 HRT는 [115]주기적 자궁내막증보다 덜 복잡한 자궁내막증상과 관련이 있다.유방 밀도에 대한 영향은 두 가지 식이요법 [116]타이밍에서 비슷한 것으로 보인다.
| 루트/폼 | 에스트로겐 | 낮다 | 표준. | 높은 | |||
|---|---|---|---|---|---|---|---|
| 오랄 | 에스트라디올 | 0.5~1mg/일 | 1일 1~2mg | 하루 2 ~ 4 mg | |||
| 에스트라디올 발라레이트 | 0.5~1mg/일 | 1일 1~2mg | 하루 2 ~ 4 mg | ||||
| 초산 에스트라디올 | 0.45~0.9mg/일 | 0.9~1.8mg/일 | 1.8~3.6mg/일 | ||||
| 켤레 에스트로겐 | 0.3~0.45mg/일 | 0.625mg/일 | 0.9~1.25mg/일 | ||||
| 에스테르화 에스트로겐 | 0.3~0.45mg/일 | 0.625mg/일 | 0.9~1.25mg/일 | ||||
| 에스트로피네이트 | 0.75mg/일 | 1.5 mg/일 | 3 mg/일 | ||||
| 에스트리올 | 1일 1~2mg | 하루 2 ~ 4 mg | 4~8mg/일 | ||||
| 에티닐에스트라디올a | 2.5~10μg/일 | 5~20μg/일 | – | ||||
| 비강 스프레이 | 에스트라디올 | 150μg/일 | 300μg/일 | 600μg/일 | |||
| 경피 패치 | 에스트라디올 | 25μg/일b | 50μg/일b | 100μg/일b | |||
| 경피겔 | 에스트라디올 | 0.5 mg/일 | 1 ~ 1.5 mg / day | 하루 2~3mg | |||
| 질내 | 에스트라디올 | 25μg/일 | – | – | |||
| 에스트리올 | 30μg/일 | 0.5mg/주 2배 | 0.5 mg/일 | ||||
| IM 또는 주입 | 에스트라디올 발라레이트 | – | – | 4 mg 1x4 주간 | |||
| 에스트라디올 시피온산염 | 1 mg (1 x 3~4 주) | 3 mg (1 x 3~4 주) | 5 mg (1 x 3~4 주) | ||||
| 에스트라디올 안식향산염 | 0.5mg/주 1회 | 1 mg/주 1회 | 1.5mg/주 1회 | ||||
| SC 이식하다 | 에스트라디올 | 25 mg 1x6개월 | 50 mg 1x6개월 | 100 mg 1x6개월 | |||
| 각주: = 건강상의 문제로 인해 더 이상 사용하지 않거나 권장하지 않습니다.b = 배합물에 따라 1주일에 1~2회 (3-4일 또는 7일 동안 사용)하여 주십시오.주의: 복용량이 반드시 동일한 것은 아닙니다.출처:"템플릿"을 참조해 주세요. | |||||||
투여 경로
갱년기 HRT에 사용되는 약물은 다양한 [1][2]투여 경로에서 사용할 수 있도록 다양한 제제로 제공됩니다.
- 경구 투여 – 정제, 캡슐
- 경피 투여 – 패치, 젤, 크림
- 질 관리 – 태블릿, 크림, 좌약, 링
- 근육내 또는 피하주사– 약병 또는 앰플용액
- 피하 임플란트 – 지방 조직에 삽입된 수술로 삽입된 펠릿
- 설하, 구강, 비강 및 직장 내 투여 및 자궁 내 투여의 빈도가 낮습니다.
최근에 개발된 약물 전달 형태는 국소적인 효과가 증가하여 복용량을 낮추고 부작용을 줄이며 순환적인 혈청 호르몬 [1][2]수치보다는 일정하다고 알려져 있다.특히 경피와 질 에스트로겐은 간을 통한 첫 번째 통과 대사를 피한다.이는 차례로 응고 인자의 증가와 항에스트로겐 대사물의 축적을 방지하여 특히 심혈관 질환과 [117]뇌졸중에 대한 부작용을 감소시킨다.
에스트라디올의 주입 가능한 형태는 다른 [118]제제의 사용 가능성 때문에 더 이상 갱년기 호르몬 치료에서 권장되지 않는다.
생체동일호르몬요법
생체동일호르몬요법(BHT)은 몸에서 생성되는 호르몬과 화학적으로 동일한 호르몬을 사용하는 것이다.비록 BHT의 지지자들이 비생물학적 혹은 전통적인 호르몬 치료법보다 이점을 주장하지만, FDA는 이러한 호르몬이 자연적으로 발생하는 [11][119]호르몬과 동일하다는 과학적 증거가 없다고 말하면서 '생물학적 호르몬'이라는 용어를 인정하지 않는다.그러나 '생물 동질'[12][9]로 분류된 호르몬을 함유한 FDA 승인 제품들이 있다.
생물학적 동일 호르몬은 의약품 또는 복합제제에 사용될 수 있으며, 생물학적 동일 호르몬은 표준화 및 규제 [11]감독 부족으로 인해 규제 기관에 의해 일반적으로 권장되지 않는다.대부분의 생체동일 호르몬 분류는 제품의 제조, 소스 또는 배송 방법을 고려하지 않으므로, 비 FDA 승인 복합 제품과 FDA 승인 의약품 모두를 '생물동일'[9]로 기술한다.영국 갱년기 학회는 규제되지 않은, 전문 약국에 의해 만들어진 관습으로 묘사되고, FDA와 같은 단체들에 의해 공식적인 감독을 받는 "규제된" 제약 등급 양식 (rBHRT) 사이의 구별을 지지하는 합의된 성명서를 발표했다.f 대부분의 임상시험.[54]복합 생체 동질 HRT를 권장하는 일부 의사들은 또한 침 또는 혈청 호르몬 테스트를 사용하여 치료에 대한 반응을 모니터링한다. 이는 미국과 [120]유럽의 현재 임상 지침에 의해 승인되지 않은 관행이다.
의약품의 생체 동질 호르몬은 임상 데이터가 매우 제한적일 수 있으며, 현재까지 동물 유래 호르몬과 비교한 무작위 대조 예비 실험은 없다.일부 임상 전 데이터는 정맥 혈전 색전증, 심혈관 질환, 유방암의 [11]위험 감소를 시사했다.2012년 현재, 북미 갱년기 학회, 내분비 학회, 국제 갱년기 학회, 유럽 갱년기 및 안드로포즈 학회의 지침은 응고 [11][121]위험이 증가한 사람들에 대한 생체 동질 의약품의 위험 감소를 지지했다.
배합
HRT에 대한 배합은 규제와 표준화된 투약 부족으로 [11][119]인해 일반적으로 미국 FDA와 의료업계에 의해 권장되지 않는다.미국 의회는 1997년 연방식품의약품화장품법(FDCA) 개정안에서 FDA에 복합약물에 대한 명시적이지만 제한적인 감독을 허용했지만, 그 이후 이 역할에서 장애물을 만났다.는 2012년 뇌막염 발생 오염된 스테로이드 주사들 때문에 64환자 사망자와 750를 입힌 환자들 후에, 의회, 하고, 전통 복합에 수송 자료 통제 활동 규제를 강화하는 등 FDA에 의한compounded 마약 제조 시설에 대한 자발적인 등록의 창조권을 행사한 것은 2013년 의약품 품질 및 보안 법을 통과시켰다.[122]DQSA와 FDCA의 규정 §503A의 강화는 FDA의 권한을 공고히 [122]하여 생체동일호르몬요법의 복합체에 대한 FDCA 규제를 시행한다.
반면에 영국에서는 복합화가 규제된 활동이다.의약품 및 의료 제품 규제 기관은 제조 스페셜 라이선스에 따라 수행되는 배합물을 규제하고 일반 약사회는 약국에서 수행되는 배합물을 규제합니다.영국에서 처방된 모든 테스토스테론은 생물학적 동질성이며, 국민 건강 서비스에 의해 사용이 지원된다.남성 테스토스테론 제품에 대한 마케팅 허가도 있습니다.국립건강관리연구소(National Institute for Health and Care Excellence)의 가이드라인 1.4.8은 "HRT만으로는 효과가 없을 경우 성욕이 낮은 갱년기 여성을 위한 테스토스테론 보충을 고려한다"고 명시하고 있다.각주에는 다음과 같이 덧붙인다. "출판 시점(2015년 11월)에 테스토스테론은 여성에 대한 이 표시에 대한 영국 시판 허가를 가지고 있지 않았다.생체동일 프로게스테론은 체외수정 치료와 조산 위험이 있는 임신부에게 사용된다.
사회와 대중의 인식
와이스 논쟁
Wyeth는 현재 Pfizer의 자회사로 HRT 제품인 Premarin(CEEs)과 Prempro(CEEs+MPA)[123][124]를 판매하는 제약 회사였습니다.2009년 Wyeth 관련 소송은 이러한 [123][124][125]의약품의 홍보에 관한 관행을 밝힌 1,500개의 문서를 공개하는 결과를 낳았다.문서에는 Wyeth가 HRT 제품의 입증되지 않은 이점을 홍보하고 위해와 위험을 경시하며 경쟁 치료법을 부정적인 [123][124][125]시각으로 캐스팅하기 위해 의학 저널에 게재된 수십 개의 대필 리뷰와 코멘트를 의뢰한 것으로 나타났다.1990년대 중반부터 시작해 10년 이상 계속된 Wyeth는 대필 [125]출판물을 사용하여 HRT 제품을 홍보하는 공격적인 "출판 계획" 전략을 추구했습니다.주로 의료용 쓰기 [125]회사인 DesignWrite와 협력했습니다.1998년부터 2005년까지 Wyeth는 HRT 제품을 홍보하는 26개의 논문을 과학 [123]저널에 실었습니다.
이러한 호의적인 출판물은 HRT 제품의 이점을 강조하고 위험, 특히 유방암과의 [125]관련성에 대한 "착각"을 과소평가했다.이 출판물은 자사 제품의 지원되지 않는 심혈관 "이점"을 옹호하고, 유방암과 같은 위험을 경시하며, 치매, 파킨슨병, 시력 문제 및 [124]주름 예방과 같은 라벨 외적이고 증명되지 않은 사용을 장려했습니다.와이스 박사는 골다공증에 대한 SERM 라록시펜에 대한 부정적 메시지를 강조하면서 WHI 이후 효과가 있거나 안전하다는 증거가 거의 없지만 대체 치료법이 사용 증가했다는 사실을 강조하라고 지시해 승인된 유전자의 품질과 치료적 등가성에 의문을 제기했다.ric CEE 제품 및 CEE와 MPA의 고유한 위해성이 모든 형태의 갱년기 HRT의 클래스 효과라는 개념을 확산시키기 위한 노력을 기울였다. "전반적으로, 이러한 데이터는 여성 건강 이니셔티브에서 보고된 유익성/위해성 분석이 모든 갱년기 후 호르몬 대체 치료 [124]제품에 일반화될 수 있음을 나타낸다."
2002년 WHI 데이터 발표 이후 제약업계의 주가가 폭락하면서 수많은 여성들이 [126]HRT 사용을 중단했다.WHI 실험에 사용된 프레마린과 프레엠프로를 공급했던 와이스의 재고량은 50% 이상 감소해 완전히 [126]회복되지 못했다.이에 대한 그들의 기사의 일부는 다음과 같은 주제를 홍보했다: "WHI는 결함이 있었다; WHI는 논란이 많은 시험이었다; WHI에서 연구된 인구는 부적절하거나 갱년기 여성의 일반 모집단을 대표하지 않았다; 임상 시험의 결과는 개인에 대한 치료를 안내해서는 안 된다; 관찰 연구.무작위 임상시험과 같거나 더 좋다.동물 연구는 임상 의사결정을 이끌 수 있다.호르몬 치료와 관련된 위험은 과장되었다.호르몬 치료의 이점은 이미 입증되었거나 입증될 것이다.최근 연구는 이상이다.[87]업계에서 급여를 받는 5명의 [87]저자가 114개의 사설, 리뷰, 가이드라인 및 서신을 분석한 2010년에서도 유사한 결과가 관찰되었다.이러한 출판물은 긍정적인 주제를 촉진하고 WHI나 [87]MWS와 같은 불리한 시험에 도전하고 비판했습니다.Wyeth는 2009년에 680억달러에 [127][128]달하는 거래로 Pfizer에 인수되었습니다.프로베라와 데포프로베라(MPA)를 생산하고 의학 대필도 해온 화이저는 베스트셀링 [87][125]의약품인 프레마린과 프레엠프로를 계속 판매하고 있다.
Fugh-Berman (2010)에 따르면, "오늘날에도, 결정적인 과학적 데이터에도 불구하고, 많은 산부인과 의사들은 여전히 [HRT]의 이점이 무증상 여성의 위험성보다 크다고 믿고 있습니다.이러한 비증거적 인식은 의학 [124]문헌에 대해 수십 년 동안 세심하게 조정된 기업의 영향의 결과일 수 있습니다."50%에 달하는 의사들이 WHI와 [129]HERS와 같은 대규모 실험에 대해 회의적인 반응을 보였다.많은 HRT 의사들이 잠재적으로 어떤 이점보다 더 큰 위험을 보여 주는데도 불구하고 긍정적인 인식을 가지고 있는 것은 [125][87]Wyeth와 같은 제약 회사의 노력 때문일 수 있습니다.
인기
1990년대는 처방률이 급격히 하락했지만 최근에는 다시 [117][130]상승하기 시작했다.경피 요법은 정맥 혈전 색전증 증가의 부족으로 인해 현재 영국에서 HRT를 위한 첫 번째 선택이다.켤레 말 에스트로겐은 혈전 위험이 더 높으며 현재 영국에서 일반적으로 사용되지 않고 혈전 위험이 낮은 에스트라디올 기반 화합물로 대체된다.메드록시프로게스테론 아세테이트와 같은 경구 프로게스토겐 조합은 정맥혈전과의 [131]연관성이 부족하기 때문에 디히드로게스테론으로 변화했다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d e f g h i Stuenkel CA, Davis SR, Gompel A, Lumsden MA, Murad MH, Pinkerton JV, Santen RJ (November 2015). "Treatment of Symptoms of the Menopause: An Endocrine Society Clinical Practice Guideline" (PDF). J. Clin. Endocrinol. Metab. 100 (11): 3975–4011. doi:10.1210/jc.2015-2236. PMID 26444994.
- ^ a b c d e f g h Santen RJ, Allred DC, Ardoin SP, Archer DF, Boyd N, Braunstein GD, Burger HG, Colditz GA, Davis SR, Gambacciani M, Gower BA, Henderson VW, Jarjour WN, Karas RH, Kleerekoper M, Lobo RA, Manson JE, Marsden J, Martin KA, Martin L, Pinkerton JV, Rubinow DR, Teede H, Thiboutot DM, Utian WH (July 2010). "Postmenopausal hormone therapy: an Endocrine Society scientific statement". J. Clin. Endocrinol. Metab. 95 (7 Suppl 1): s1–s66. doi:10.1210/jc.2009-2509. PMC 6287288. PMID 20566620.
- ^ Shuster, Lynne T.; Rhodes, Deborah J.; Gostout, Bobbie S.; Grossardt, Brandon R.; Rocca, Walter A. (2010). "Premature menopause or early menopause: Long-term health consequences". Maturitas. 65 (2): 161–166. doi:10.1016/j.maturitas.2009.08.003. ISSN 0378-5122. PMC 2815011. PMID 19733988.
- ^ a b c d e f Eden KJ, Wylie KR (1 July 2009). "Quality of sexual life and menopause". Women's Health. 6 (4): 385–396. doi:10.2217/WHE.09.24. PMID 19586430.
{{cite journal}}: CS1 maint: 작성자 파라미터 사용(링크) - ^ a b c Ziaei S., Moghasemi M., Faghihzadeh S. (2010). "Comparative effects of conventional hormone replacement therapy and tibolone on climacteric symptoms and sexual dysfunction in postmenopausal women". Climacteric. 13 (3): 147–156. doi:10.1016/j.maturitas.2006.04.014. PMID 16730929.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ a b c d Manson, JE; Aragaki, AK; Rossouw, JE; Anderson, GL; Prentice, RL; LaCroix, AZ; Chlebowski, RT; Howard, BV; Thomson, CA; Margolis, KL; Lewis, CE; Stefanick, ML; Jackson, RD; Johnson, KC; Martin, LW; Shumaker, SA; Espeland, MA; Wactawski-Wende, J; WHI, Investigators. (12 September 2017). "Menopausal Hormone Therapy and Long-term All-Cause and Cause-Specific Mortality: The Women's Health Initiative Randomized Trials". JAMA. 318 (10): 927–938. doi:10.1001/jama.2017.11217. PMC 5728370. PMID 28898378.
- ^ Langer, RD; Hodis, HN; Lobo, RA; Allison, MA (February 2021). "Hormone replacement therapy - where are we now?". Climacteric : The Journal of the International Menopause Society. 24 (1): 3–10. doi:10.1080/13697137.2020.1851183. PMID 33403881. S2CID 230783545.
- ^ a b c Løkkegaard, E; Nielsen, LH; Keiding, N (August 2017). "Risk of Stroke With Various Types of Menopausal Hormone Therapies: A National Cohort Study". Stroke. 48 (8): 2266–2269. doi:10.1161/STROKEAHA.117.017132. PMID 28626058. S2CID 207579406.
- ^ a b c d Files, JA; Ko, MG; Pruthi, S (July 2011). "Bioidentical hormone therapy". Mayo Clinic Proceedings. 86 (7): 673–80, quiz 680. doi:10.4065/mcp.2010.0714. PMC 3127562. PMID 21531972.
- ^ "Bioidentical hormones". Cleveland Clinic. 12 December 2012.
- ^ a b c d e f Conaway E (March 2011). "Bioidentical hormones: an evidence-based review for primary care providers". J Am Osteopath Assoc. 111 (3): 153–64. PMID 21464264.
- ^ a b c Cobin, RH; Goodman, NF; AACE Reproductive Endocrinology Scientific, Committee. (1 July 2017). "Position Statement on Menopause - 2017 Update" (PDF). Endocrine Practice. 23 (7): 869–880. doi:10.4158/EP171828.PS. PMID 28703650. Retrieved 1 March 2019.
- ^ a b "USPTF Consensus Statement". 2012. Archived from the original on 2013-05-30. Retrieved 2013-05-14.
- ^ Lewis, Ricki. "ACOG Revises Guidelines on Treating Menopause Symptoms". login.medscape.com. Medscape. Retrieved 4 March 2019.
- ^ "Hormone Therapy and Heart Disease - ACOG". www.acog.org. Committee on Gynecologic Practice. Retrieved 4 March 2019.
- ^ "Medscape". www.medscape.com.
- ^ a b Santen, RJ; Utian, WH (2010). "Executive Summary: Postmenopausal Hormone Therapy: An Endocrine Society Scientific Statement". J Clin Endocrinol Metab. 95 S1–S66 (Supplement 1): s1–s66. doi:10.1210/jc.2009-2509. PMC 6287288. PMID 20566620.
- ^ a b c d Marjoribanks, Jane; Farquhar, Cindy; Roberts, Helen; Lethaby, Anne; Lee, Jasmine (17 Jan 2017). "Long-term hormone therapy for perimenopausal and postmenopausal women". The Cochrane Database of Systematic Reviews. 1: CD004143. doi:10.1002/14651858.CD004143.pub5. ISSN 1469-493X. PMC 6465148. PMID 28093732.
- ^ "Menopause treatments". National Health Service, United Kingdom. 2019. Retrieved 2018-02-23.
- ^ Raine-Fenning NJ, Brincat MP, Muscat-Baron Y (2003). "Skin aging and menopause : implications for treatment". Am J Clin Dermatol. 4 (6): 371–8. doi:10.2165/00128071-200304060-00001. PMID 12762829. S2CID 20392538.
- ^ Zouboulis CC, Makrantonaki E (June 2012). "Hormonal therapy of intrinsic aging". Rejuvenation Res. 15 (3): 302–12. doi:10.1089/rej.2011.1249. PMID 22533363.
- ^ a b c d e f g 사렐, PM (2000년)호르몬 대체요법이 폐경 후 성심리생리학 및 행동에 미치는 영향.여성건강 및 성별 기반 의학 저널, 9, 25-32
- ^ a b c d e Boardman, HM; Hartley, L; Eisinga, A; Main, C; Roqué i Figuls, M; Bonfill Cosp, X; Gabriel Sanchez, R; Knight, B (10 March 2015). "Hormone therapy for preventing cardiovascular disease in post-menopausal women". The Cochrane Database of Systematic Reviews (3): CD002229. doi:10.1002/14651858.CD002229.pub4. ISSN 1469-493X. PMID 25754617. S2CID 22188456.
- ^ Hodis, HN; Mack, WJ; Henderson, VW; Shoupe, D; Budoff, MJ; Hwang-Levine, J; Li, Y; Feng, M; Dustin, L; Kono, N; Stanczyk, FZ; Selzer, RH; Azen, SP; ELITE Research, Group. (31 March 2016). "Vascular Effects of Early versus Late Postmenopausal Treatment with Estradiol". The New England Journal of Medicine. 374 (13): 1221–31. doi:10.1056/NEJMoa1505241. PMC 4921205. PMID 27028912.
- ^ Writing Group on Behalf of Workshop Consensus (October 2009). "Aging, menopause, cardiovascular disease and HRT. International Menopause Society Consensus Statement". Climacteric. 12 (5): 368–77. doi:10.1080/13697130903195606. PMID 19811229. S2CID 218865937.
- ^ a b c d e Manson, JE; Chlebowski, RT; Stefanick, ML; Aragaki, AK; Rossouw, JE; Prentice, RL; Anderson, G; Howard, BV; Thomson, CA; LaCroix, AZ; Wactawski-Wende, J; Jackson, RD; Limacher, M; Margolis, KL; Wassertheil-Smoller, S; Beresford, SA; Cauley, JA; Eaton, CB; Gass, M; Hsia, J; Johnson, KC; Kooperberg, C; Kuller, LH; Lewis, CE; Liu, S; Martin, LW; Ockene, JK; O'Sullivan, MJ; Powell, LH; Simon, MS; Van Horn, L; Vitolins, MZ; Wallace, RB (2 October 2013). "Menopausal hormone therapy and health outcomes during the intervention and extended poststopping phases of the Women's Health Initiative randomized trials". JAMA. 310 (13): 1353–68. doi:10.1001/jama.2013.278040. PMC 3963523. PMID 24084921.
- ^ a b Saeaib, N; Peeyananjarassri, K; Liabsuetrakul, T; Buhachat, R; Myriokefalitaki, E (28 January 2020). "Hormone replacement therapy after surgery for epithelial ovarian cancer". The Cochrane Database of Systematic Reviews. 1: CD012559. doi:10.1002/14651858.CD012559.pub2. PMC 7027384. PMID 31989588.
- ^ Darabi, M.; Rabbani, M.; Ani, M.; Zarean, E.; Panjehpour, M.; Movahedian, A. (2011). "Increased leukocyte ABCA1 gene expression in post-menopausal women on hormone replacement therapy". Gynecological Endocrinology. 27 (9): 701–705. doi:10.3109/09513590.2010.507826. PMID 20807164. S2CID 203464.
- ^ Gregersen, I; Høibraaten, E; Holven, KB; Løvdahl, L; Ueland, T; Mowinckel, MC; Dahl, TB; Aukrust, P; Halvorsen, B; Sandset, PM (December 2019). "Effect of hormone replacement therapy on atherogenic lipid profile in postmenopausal women". Thrombosis Research. 184: 1–7. doi:10.1016/j.thromres.2019.10.005. PMID 31677448.
- ^ Spoletini, I; Vitale, C; Pelliccia, F; Fossati, C; Rosano, GM (December 2014). "Androgens and cardiovascular disease in postmenopausal women: a systematic review". Climacteric : The Journal of the International Menopause Society. 17 (6): 625–34. doi:10.3109/13697137.2014.887669. PMID 24559253. S2CID 33413274.
- ^ a b c d Davis, SR; Baber, R; Panay, N; Bitzer, J; Perez, SC; Islam, RM; Kaunitz, AM; Kingsberg, SA; Lambrinoudaki, I; Liu, J; Parish, SJ; Pinkerton, J; Rymer, J; Simon, JA; Vignozzi, L; Wierman, ME (September 2019). "Global Consensus Position Statement on the Use of Testosterone Therapy for Women". The Journal of Sexual Medicine. 16 (9): 1331–1337. doi:10.1016/j.jsxm.2019.07.012. hdl:2158/1176450. PMID 31488288. S2CID 201845588.
- ^ a b c Shifren, JL; Davis, SR (August 2017). "Androgens in postmenopausal women: a review". Menopause. 24 (8): 970–979. doi:10.1097/GME.0000000000000903. PMID 28609390. S2CID 39876534.
- ^ a b Scarabin, P.-Y. (August 2018). "Progestogens and venous thromboembolism in menopausal women: an updated oral versus transdermal estrogen meta-analysis". Climacteric. 21 (4): 341–345. doi:10.1080/13697137.2018.1446931. ISSN 1473-0804. PMID 29570359. S2CID 4229701.
- ^ Olié, V. R.; Canonico, M.; Scarabin, P. Y. (2010). "Risk of venous thrombosis with oral versus transdermal estrogen therapy among postmenopausal women". Current Opinion in Hematology. 17 (5): 457–463. doi:10.1097/MOH.0b013e32833c07bc. PMID 20601871. S2CID 205827003.
- ^ Rott, H (2014). "Prevention and treatment of venous thromboembolism during HRT: current perspectives". International Journal of General Medicine. 7: 433–40. doi:10.2147/IJGM.S46310. PMC 4155999. PMID 25210472.
- ^ a b Carrasquilla GD, Frumento P, Berglund A, Borgfeldt C, Bottai M, Chiavenna C, Eliasson M, Engström G, Hallmans G, Jansson JH, Magnusson PK, Nilsson PM, Pedersen NL, Wolk A, Leander K (November 2017). "Postmenopausal hormone therapy and risk of stroke: A pooled analysis of data from population-based cohort studies". PLOS Med. 14 (11): e1002445. doi:10.1371/journal.pmed.1002445. PMC 5693286. PMID 29149179.
- ^ Chlebowski, RT; Anderson, GL; Sarto, GE; Haque, R; Runowicz, CD; Aragaki, AK; Thomson, CA; Howard, BV; Wactawski-Wende, J; Chen, C; Rohan, TE; Simon, MS; Reed, SD; Manson, JE (March 2016). "Continuous Combined Estrogen Plus Progestin and Endometrial Cancer: The Women's Health Initiative Randomized Trial". Journal of the National Cancer Institute. 108 (3): djv350. doi:10.1093/jnci/djv350. PMC 5072373. PMID 26668177.
- ^ Archer, DF (2001). "The effect of the duration of progestin use on the occurrence of endometrial cancer in postmenopausal women". Menopause. 8 (4): 245–51. doi:10.1097/00042192-200107000-00005. PMID 11449081. S2CID 38526018.
- ^ a b c Kim, JJ; Kurita, T; Bulun, SE (February 2013). "Progesterone action in endometrial cancer, endometriosis, uterine fibroids, and breast cancer". Endocrine Reviews. 34 (1): 130–62. doi:10.1210/er.2012-1043. PMC 3565104. PMID 23303565.
- ^ Young, Robert; Arlan F., Jr Fuller; Fuller, Arlan F.; Michael V. Seiden (2004). Uterine cancer. Hamilton, Ont: B.C. Decker. ISBN 978-1-55009-163-2.
- ^ Zang, H; Sahlin, L; Masironi, B; Eriksson, E; Lindén Hirschberg, A (June 2007). "Effects of testosterone treatment on endometrial proliferation in postmenopausal women". The Journal of Clinical Endocrinology and Metabolism. 92 (6): 2169–75. doi:10.1210/jc.2006-2171. PMID 17341565.
- ^ "Endometrial cancer risk was lower in women who used continuous combined HRT than in non-users". Evidence-based Obstetrics & Gynecology. 8 (1–2): 68–69. March 2006. doi:10.1016/j.ebobgyn.2006.01.011. ISSN 1361-259X.
- ^ a b c Zeng, Z; Jiang, X; Li, X; Wells, A; Luo, Y; Neapolitan, R (2018). "Conjugated equine estrogen and medroxyprogesterone acetate are associated with decreased risk of breast cancer relative to bioidentical hormone therapy and controls". PLOS ONE. 13 (5): e0197064. Bibcode:2018PLoSO..1397064Z. doi:10.1371/journal.pone.0197064. PMC 5955567. PMID 29768475.
- ^ Fournier, A. S.; Berrino, F.; Clavel-Chapelon, F. O. (2007). "Unequal risks for breast cancer associated with different hormone replacement therapies: Results from the E3N cohort study". Breast Cancer Research and Treatment. 107 (1): 103–111. doi:10.1007/s10549-007-9523-x. PMC 2211383. PMID 17333341.
- ^ Beral, V; Reeves, G; Bull, D; Green, J; Million Women Study, Collaborators. (16 February 2011). "Breast cancer risk in relation to the interval between menopause and starting hormone therapy". Journal of the National Cancer Institute. 103 (4): 296–305. doi:10.1093/jnci/djq527. PMC 3039726. PMID 21278356.
{{cite journal}}:first5=범용명(도움말)이 있습니다. - ^ Letendre, I.; Lopes, P. (2012). "Ménopause et risques carcinologiques". Journal de Gynécologie Obstétrique et Biologie de la Reproduction. 41 (7): F33–F37. doi:10.1016/j.jgyn.2012.09.006. PMID 23062839.
- ^ Chlebowski, RT; Anderson, GL; Aragaki, AK; Manson, JE; Stefanick, ML; Pan, K; Barrington, W; Kuller, LH; Simon, MS; Lane, D; Johnson, KC; Rohan, TE; Gass, MLS; Cauley, JA; Paskett, ED; Sattari, M; Prentice, RL (28 July 2020). "Association of Menopausal Hormone Therapy With Breast Cancer Incidence and Mortality During Long-term Follow-up of the Women's Health Initiative Randomized Clinical Trials". JAMA. 324 (4): 369–380. doi:10.1001/jama.2020.9482. PMC 7388026. PMID 32721007.
- ^ Anderson, G. L.; Limacher, M.; Assaf, A. R.; Bassford, T.; Beresford, S. A.; Black, H.; Bonds, D.; Brunner, R.; Brzyski, R.; Caan, B.; Chlebowski, R.; Curb, D.; Gass, M.; Hays, J.; Heiss, G.; Hendrix, S.; Howard, B. V.; Hsia, J.; Hubbell, A.; Jackson, R.; Johnson, K. C.; Judd, H.; Kotchen, J. M.; Kuller, L.; Lacroix, A. Z.; Lane, D.; Langer, R. D.; Lasser, N.; Lewis, C. E.; Manson, J. (2004). "Effects of Conjugated Equine Estrogen in Postmenopausal Women with Hysterectomy: The Women's Health Initiative Randomized Controlled Trial". JAMA: The Journal of the American Medical Association. 291 (14): 1701–1712. doi:10.1001/jama.291.14.1701. PMID 15082697.
- ^ Stefanick ML; Anderson GL; Margolis KL; et al. (2006). "Effects of conjugated equine estrogens on breast cancer and mammography screening in postmenopausal women with hysterectomy". JAMA. 295 (14): 1647–57. doi:10.1001/jama.295.14.1647. PMID 16609086.
- ^ "Association between hormone replacement therapy use and breast cancer risk varies by race/ethnicity, body mass index, and breast density". JNCI Journal of the National Cancer Institute. 105 (18). 2013. doi:10.1093/jnci/djt264. ISSN 0027-8874.
- 다음으로, 다음과 같은 이유를 들 수:
- ^ Kuhl, H.; Schneider, H. P. G. (2013). "Progesterone – promoter or inhibitor of breast cancer". Climacteric. 16 Suppl 1: 54–68. doi:10.3109/13697137.2013.768806. PMID 23336704. S2CID 20808536.
- ^ Azam, S; Lange, T; Huynh, S; Aro, AR; von Euler-Chelpin, M; Vejborg, I; Tjønneland, A; Lynge, E; Andersen, ZJ (June 2018). "Hormone replacement therapy, mammographic density, and breast cancer risk: a cohort study". Cancer Causes & Control. 29 (6): 495–505. doi:10.1007/s10552-018-1033-0. PMC 5938298. PMID 29671181.
- ^ Stute, P; Wildt, L; Neulen, J (April 2018). "The impact of micronized progesterone on breast cancer risk: a systematic review". Climacteric : The Journal of the International Menopause Society. 21 (2): 111–122. doi:10.1080/13697137.2017.1421925. PMID 29384406. S2CID 3642971.
- ^ a b Panay, N; Medical Advisory Council of the British Menopause, Society. (June 2019). "BMS - Consensus statement: Bioidentical HRT". Post Reproductive Health. 25 (2): 61–63. doi:10.1177/2053369119841844. PMID 31192760. S2CID 189816648.
- ^ 유방암 후 갱년기 관리 Royal Australian and New Zealand College of 산부인과 및 산부인과 의사로부터 2016-04-07년 아카이브되었습니다.대학 성명 C-Gyn 15. 제1회 승인:2003년 2월현재 : 2011년 11월리뷰:2014년 11월
- ^ Gordhandas, S; Norquist, BM; Pennington, KP; Yung, RL; Laya, MB; Swisher, EM (April 2019). "Hormone replacement therapy after risk reducing salpingo-oophorectomy in patients with BRCA1 or BRCA2 mutations; a systematic review of risks and benefits". Gynecologic Oncology. 153 (1): 192–200. doi:10.1016/j.ygyno.2018.12.014. PMID 30661763. S2CID 58593390.
- ^ Heinig, M; Schwarz, S; Haug, U (16 February 2021). "Self-selection for mammography screening according to use of hormone replacement therapy: A systematic literature review". Cancer Epidemiology. 71 (Pt A): 101812. doi:10.1016/j.canep.2020.101812. PMID 33608235. S2CID 231970420.
- ^ Kotsopoulos, J; Narod, SA (January 2012). "Androgens and breast cancer". Steroids. 77 (1–2): 1–9. doi:10.1016/j.steroids.2011.10.002. PMID 22015396. S2CID 32022318.
- ^ Collaborative Group on Epidemiological Studies of Ovarian Cancer (12 February 2015). "Menopausal hormone use and ovarian cancer risk: individual participant meta-analysis of 52 epidemiological studies". The Lancet. 385 (9980): 1835–1842. doi:10.1016/S0140-6736(14)61687-1. PMC 4427760. PMID 25684585.
- ^ a b c Shi, LF; Wu, Y; Li, CY (April 2016). "Hormone therapy and risk of ovarian cancer in postmenopausal women: a systematic review and meta-analysis". Menopause. 23 (4): 417–24. doi:10.1097/GME.0000000000000550. PMID 26506499. S2CID 32195397.
- ^ Guidozzi, F (December 2013). "Estrogen therapy in gynecological cancer survivors". Climacteric : The Journal of the International Menopause Society. 16 (6): 611–7. doi:10.3109/13697137.2013.806471. PMID 23952524. S2CID 38122562.
- ^ "Menopausal Hormone Therapy and Cancer Risk". www.cancer.org. Retrieved 4 March 2019.
- ^ Jang, YC; Huang, HL; Leung, CY (9 December 2019). "Association of hormone replacement therapy with mortality in colorectal cancer survivor: a systematic review and meta-analysis". BMC Cancer. 19 (1): 1199. doi:10.1186/s12885-019-6428-0. PMC 6902524. PMID 31818262.
- ^ Vargiu, V; Amar, ID; Rosati, A; Dinoi, G; Turco, LC; Capozzi, VA; Scambia, G; Villa, P (25 November 2020). "Hormone replacement therapy and cervical cancer: a systematic review of the literature". Climacteric : The Journal of the International Menopause Society. 24 (2): 120–127. doi:10.1080/13697137.2020.1826426. PMID 33236658. S2CID 227166430.
- ^ Miller M.M.; Franklin K.B.J. (1999). "Theoretical basis for the benefit of postmenopausal estrogen substitution". Experimental Gerontology. 34 (5): 587–604. doi:10.1016/S0531-5565(99)00032-7. PMID 10530785. S2CID 43031351.
- ^ Gonzalez M., Viagara G., Caba F., Molina E. (2004). "Sexual function, menopause and hormone replacement therapy (HRT)". The European Menopause Journal. 48 (4): 411–420. doi:10.1016/j.maturitas.2003.10.005. PMID 15283933.
{{cite journal}}: CS1 maint: 여러 이름: 작성자 목록(링크) - ^ Johansen, N; Lindén Hirschberg, A; Moen, MH (August 2020). "The role of testosterone in menopausal hormone treatment. What is the evidence?". Acta Obstetricia et Gynecologica Scandinavica. 99 (8): 966–969. doi:10.1111/aogs.13819. PMID 32027015. S2CID 211050248.
- ^ a b Dye, RV; Miller, KJ; Singer, EJ; Levine, AJ (2012). "Hormone replacement therapy and risk for neurodegenerative diseases". International Journal of Alzheimer's Disease. 2012: 258454. doi:10.1155/2012/258454. PMC 3324889. PMID 22548198.
- ^ Campdelacreu, J (November 2014). "Parkinson disease and Alzheimer disease: environmental risk factors". Neurologia (Barcelona, Spain). 29 (9): 541–9. doi:10.1016/j.nrl.2012.04.001. PMID 22703631.
- ^ Nicoletti, A; Nicoletti, G; Arabia, G; Annesi, G; De Mari, M; Lamberti, P; Grasso, L; Marconi, R; Epifanio, A; Morgante, L; Cozzolino, A; Barone, P; Quattrone, A; Zappia, M (December 2011). "Reproductive factors and Parkinson's disease: a multicenter case-control study". Movement Disorders. 26 (14): 2563–6. doi:10.1002/mds.23951. PMID 21956541. S2CID 40143658.
- ^ Noyce, AJ; Bestwick, JP; Silveira-Moriyama, L; Hawkes, CH; Giovannoni, G; Lees, AJ; Schrag, A (December 2012). "Meta-analysis of early nonmotor features and risk factors for Parkinson disease". Annals of Neurology. 72 (6): 893–901. doi:10.1002/ana.23687. PMC 3556649. PMID 23071076.
- ^ Wang, P; Li, J; Qiu, S; Wen, H; Du, J (2015). "Hormone replacement therapy and Parkinson's disease risk in women: a meta-analysis of 14 observational studies". Neuropsychiatric Disease and Treatment. 11: 59–66. doi:10.2147/NDT.S69918. PMC 4317144. PMID 25657580.
- ^ Rugbjerg, K; Christensen, J; Tjønneland, A; Olsen, JH (April 2013). "Exposure to estrogen and women's risk for Parkinson's disease: a prospective cohort study in Denmark". Parkinsonism & Related Disorders. 19 (4): 457–60. doi:10.1016/j.parkreldis.2013.01.008. PMID 23402992.
- ^ Yoon, BK; Chin, J; Kim, JW; Shin, MH; Ahn, S; Lee, DY; Seo, SW; Na, DL (August 2018). "Menopausal hormone therapy and mild cognitive impairment: a randomized, placebo-controlled trial". Menopause. 25 (8): 870–876. doi:10.1097/GME.0000000000001140. PMID 29846283. S2CID 44174553.
- ^ Rasgon, NL; Geist, CL; Kenna, HA; Wroolie, TE; Williams, KE; Silverman, DH (2014). "Prospective randomized trial to assess effects of continuing hormone therapy on cerebral function in postmenopausal women at risk for dementia". PLOS ONE. 9 (3): e89095. Bibcode:2014PLoSO...989095R. doi:10.1371/journal.pone.0089095. PMC 3951184. PMID 24622517.
- ^ Schmidt R, Fazekas F, Reinhart B, Kapeller P, Fazekas G, Offenbacher H, Eber B, Schumacher M, Freidl W (November 1996). "Estrogen replacement therapy in older women: a neuropsychological and brain MRI study". Journal of the American Geriatrics Society. 44 (11): 1307–13. doi:10.1111/j.1532-5415.1996.tb01400.x. PMID 8909345. S2CID 22921797.
- ^ Parkinson Study Group POETRY, Investigators. (December 2011). "A randomized pilot trial of estrogen replacement therapy in post-menopausal women with Parkinson's disease". Parkinsonism & Related Disorders. 17 (10): 757–60. doi:10.1016/j.parkreldis.2011.07.007. PMID 21824799.
- ^ Diamanti-Kandarakis, E; Dattilo, M; Macut, D; Duntas, L; Gonos, ES; Goulis, DG; Gantenbein, CK; Kapetanou, M; Koukkou, E; Lambrinoudaki, I; Michalaki, M; Eftekhari-Nader, S; Pasquali, R; Peppa, M; Tzanela, M; Vassilatou, E; Vryonidou, A (June 2017). "Mechanisms in Endocrinology: Aging and anti-aging: a Combo-Endocrinology overview". European Journal of Endocrinology. 176 (6): R283–R308. doi:10.1530/EJE-16-1061. PMID 28264815.
- ^ Vest, RS; Pike, CJ (February 2013). "Gender, sex steroid hormones, and Alzheimer's disease". Hormones and Behavior. 63 (2): 301–7. doi:10.1016/j.yhbeh.2012.04.006. PMC 3413783. PMID 22554955.
- ^ Pike, CJ; Carroll, JC; Rosario, ER; Barron, AM (July 2009). "Protective actions of sex steroid hormones in Alzheimer's disease". Frontiers in Neuroendocrinology. 30 (2): 239–58. doi:10.1016/j.yfrne.2009.04.015. PMC 2728624. PMID 19427328.
- ^ Zhu, L; Jiang, X; Sun, Y; Shu, W (April 2016). "Effect of hormone therapy on the risk of bone fractures: a systematic review and meta-analysis of randomized controlled trials". Menopause. 23 (4): 461–70. doi:10.1097/GME.0000000000000519. PMID 26529613. S2CID 26110755.
- ^ a b Studd J (March 2010). "Ten reasons to be happy about hormone replacement therapy: a guide for patients". Menopause Int. 16 (1): 44–6. doi:10.1258/mi.2010.010001. PMID 20424287. S2CID 33414205.
- ^ Tiidus, PM (August 2011). "Benefits of estrogen replacement for skeletal muscle mass and function in post-menopausal females: evidence from human and animal studies". The Eurasian Journal of Medicine. 43 (2): 109–14. doi:10.5152/eajm.2011.24. PMC 4261347. PMID 25610174.
- ^ Deleruyelle, LJ (2017). "Menopausal Symptom Relief and Side Effects Experienced by Women Using Compounded Bioidentical Hormone Replacement Therapy and Synthetic Conjugated Equine Estrogen and/or Progestin Hormone Replacement Therapy, Part 3". International Journal of Pharmaceutical Compounding. 21 (1): 6–16. PMID 28346192.
- ^ Suchowersky O, Muthipeedika J (December 2005). "A case of late-onset chorea". Nat Clin Pract Neurol. 1 (2): 113–6. doi:10.1038/ncpneuro0052. PMID 16932507. S2CID 11410333.
- ^ MacLennan, AH (August 2011). "HRT in difficult circumstances: are there any absolute contraindications?". Climacteric. 14 (4): 409–17. doi:10.3109/13697137.2010.543496. PMID 21355685. S2CID 25426141.
- ^ a b c d e f g h i j Fugh-Berman, Adriane (2015). "The Science of Marketing: How Pharmaceutical Companies Manipulated Medical Discourse on Menopause". Women's Reproductive Health. 2 (1): 18–23. doi:10.1080/23293691.2015.1039448. ISSN 2329-3691.
- ^ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans; World Health Organization; International Agency for Research on Cancer (2007). Combined Estrogen-progestogen Contraceptives and Combined Estrogen-progestogen Menopausal Therapy. World Health Organization. pp. 205–. ISBN 978-92-832-1291-1.
- ^ a b c Writing Group for the Women's Health Initiative Investigators (2002). "Risks and Benefits of Estrogen Plus Progestin in Healthy Postmenopausal Women: Principal Results From the Women's Health Initiative Randomized Controlled Trial". JAMA. 288 (3): 321–333. doi:10.1001/jama.288.3.321. PMID 12117397.
- ^ Chlebowski RT, Kuller LH, Prentice RL, Stefanick ML, Manson JE, Gass M, et al. (February 2009). "Breast cancer after use of estrogen plus progestin in postmenopausal women". The New England Journal of Medicine. 360 (6): 573–87. doi:10.1056/NEJMoa0807684. PMC 3963492. PMID 19196674.
- ^ Kreatsoulas, C.; Anand, S. S. (2013). "Menopausal hormone therapy for the primary prevention of chronic conditions. U.S. Preventive Services Task Force Recommendation Statement" (PDF). Polskie Archiwum Medycyny Wewnetrznej. 123 (3): 112–117. PMID 23396275.
- ^ Nelson, H. D.; Walker, M.; Zakher, B.; Mitchell, J. (2012). "Menopausal hormone therapy for the primary prevention of chronic conditions: A systematic review to update the U.S. Preventive Services Task Force recommendations". Annals of Internal Medicine. 157 (2): 104–113. doi:10.7326/0003-4819-157-2-201207170-00466. PMID 22786830.
- ^ George, James L.; Colman, Robert W.; Goldhaber, Samuel Z.; Victor J. Marder (2006). Hemostasis and thrombosis: basic principles and clinical practice. Hagerstown, MD: Lippincott Williams & Wilkins. pp. 1239. ISBN 978-0-7817-4996-1.
- ^ Darabi M, Ani M, Panjehpour M, Rabbani M, Movahedian A, Zarean E (2011). "Effect of estrogen receptor β A1730G polymorphism on ABCA1 gene expression response to postmenopausal hormone replacement therapy". Genetic Testing and Molecular Biomarkers. 15 (1–2): 11–5. doi:10.1089/gtmb.2010.0106. PMID 21117950.
- ^ Chlebowski, R. T.; Anderson, G. L. (2015). "Menopausal hormone therapy and breast cancer mortality: clinical implications". Therapeutic Advances in Drug Safety. 6 (2): 45–56. doi:10.1177/2042098614568300. ISSN 2042-0986. PMC 4406918. PMID 25922653.
- ^ Mazzucco AE, Santoro E, DeSoto M, Lee JH (December 2010). "Hormone Therapy and Menopause". National Research Center for Women and Families.
- ^ Gina Kolata (2007-04-19). "Sharp Drop in Rates of Breast Cancer Holds". New York Times.
- ^ Roni Caryn Rabin (2007-08-28). "For a Low-Dose Hormone, Take Your Pick". New York Times.
Many women seeking natural remedies have turned to compounding pharmacies, which use bioidentical hormones that are chemically synthesized but with the same molecular structure as hormones produced by a woman's body.
- ^ John Gever (2011-04-05). "New WHI Estrogen Analysis Shows Lower Breast Ca Risk". MedPageToday.
- ^ Salpeter, S. R.; Cheng, J.; Thabane, L.; Buckley, N. S.; Salpeter, E. E. (2009). "Bayesian Meta-analysis of Hormone Therapy and Mortality in Younger Postmenopausal Women". The American Journal of Medicine. 122 (11): 1016–1022.e1. doi:10.1016/j.amjmed.2009.05.021. PMID 19854329.
- ^ Anderson, G. L.; Chlebowski, R. T.; Rossouw, J. E.; Rodabough, R. J.; McTiernan, A.; Margolis, K. L.; Aggerwal, A.; David Curb, J. D.; Hendrix, S. L.; Allan Hubbell, F. A.; Khandekar, J.; Lane, D. S.; Lasser, N.; Lopez, A. M.; Potter, J.; Ritenbaugh, C. (2006). "Prior hormone therapy and breast cancer risk in the Women's Health Initiative randomized trial of estrogen plus progestin". Maturitas. 55 (2): 103–115. doi:10.1016/j.maturitas.2006.05.004. PMID 16815651.
- ^ Hulley, S.; Grady, D.; Bush, T.; Furberg, C.; Herrington, D.; Riggs, B.; Vittinghoff, E. (1998). "Randomized trial of estrogen plus progestin for secondary prevention of coronary heart disease in postmenopausal women. Heart and Estrogen/progestin Replacement Study (HERS) Research Group". JAMA: The Journal of the American Medical Association. 280 (7): 605–613. doi:10.1001/jama.280.7.605. PMID 9718051.
- ^ Salpeter, S. R.; Walsh, J. M. E.; Greyber, E.; Ormiston, T. M.; Salpeter, E. E. (2004). "Mortality associated with hormone replacement therapy in younger and older women". Journal of General Internal Medicine. 19 (7): 791–804. doi:10.1111/j.1525-1497.2004.30281.x. PMC 1492478. PMID 15209595.
- ^ Grodstein, F.; Stampfer, M. J.; Colditz, G. A.; Willett, W. C.; Manson, J. E.; Joffe, M.; Rosner, B.; Fuchs, C.; Hankinson, S. E.; Hunter, D. J.; Hennekens, C. H.; Speizer, F. E. (1997). "Postmenopausal Hormone Therapy and Mortality". New England Journal of Medicine. 336 (25): 1769–1775. doi:10.1056/NEJM199706193362501. PMID 9187066.
- ^ Bethea CL (Feb 2011). "MPA: Medroxy-Progesterone Acetate Contributes to Much Poor Advice for Women". Endocrinology. 152 (2): 343–345. doi:10.1210/en.2010-1376. PMC 3037166. PMID 21252179.
- ^ Harman SM, Brinton EA, Cedars M, Lobo R, Manson JE, Merriam GR, Miller VM, Naftolin F, Santoro N (March 2005). "KEEPS: The Kronos Early Estrogen Prevention Study". Climacteric. 8 (1): 3–12. doi:10.1080/13697130500042417. PMID 15804727. S2CID 37219662.
- ^ Morley JE, Perry HM (May 2003). "Androgens and women at the menopause and beyond". J. Gerontol. A Biol. Sci. Med. Sci. 58 (5): M409–16. doi:10.1093/gerona/58.5.M409. PMID 12730248.
- ^ Garefalakis M, Hickey M (2008). "Role of androgens, progestins and tibolone in the treatment of menopausal symptoms: a review of the clinical evidence". Clin Interv Aging. 3 (1): 1–8. doi:10.2147/CIA.S1043. PMC 2544356. PMID 18488873.
- ^ Formoso, G; Perrone, E; Maltoni, S; Balduzzi, S; Wilkinson, J; Basevi, V; Marata, AM; Magrini, N; D'Amico, R; Bassi, C; Maestri, E (12 October 2016). "Short-term and long-term effects of tibolone in postmenopausal women". The Cochrane Database of Systematic Reviews. 10: CD008536. doi:10.1002/14651858.CD008536.pub3. ISSN 1469-493X. PMC 6458045. PMID 27733017.
- ^ Cummings, SR; Ettinger, B; Delmas, PD; Kenemans, P; Stathopoulos, V; Verweij, P; Mol-Arts, M; Kloosterboer, L; Mosca, L; Christiansen, C; Bilezikian, J; Kerzberg, EM; Johnson, S; Zanchetta, J; Grobbee, DE; Seifert, W; Eastell, R; LIFT Trial, Investigators. (14 August 2008). "The effects of tibolone in older postmenopausal women". The New England Journal of Medicine. 359 (7): 697–708. doi:10.1056/NEJMoa0800743. PMC 3684062. PMID 18703472.
- ^ Mayo Clinic / Thomson Healthcare Inc.의 에스트로겐(Vaginal Route)이 문서의 최종 갱신일 : 2011년 11월 1일
- ^ Somboonporn, W; Davis, S; Seif, MW; Bell, R (19 October 2005). "Testosterone for peri- and postmenopausal women". The Cochrane Database of Systematic Reviews (4): CD004509. doi:10.1002/14651858.CD004509.pub2. PMID 16235365. S2CID 21619940.
- ^ North American Menopause, Society. (2005). "The role of testosterone therapy in postmenopausal women: position statement of The North American Menopause Society". Menopause. 12 (5): 496–511, quiz 649. doi:10.1097/01.gme.0000177709.65944.b0. PMID 16145303. S2CID 5122078.
- ^ Drapier-Faure, E; Azoulay, C; Abramovici, Y (July 2005). "[Acceptability of continuous combined versus cyclical HRT: a French multicentric randomized clinical study]". Gynécologie, obstétrique & fertilité. 33 (7–8): 498–504. doi:10.1016/j.gyobfe.2005.04.024. PMID 16005674.
- ^ Feeley, KM; Wells, M (June 2001). "Hormone replacement therapy and the endometrium". Journal of Clinical Pathology. 54 (6): 435–40. doi:10.1136/jcp.54.6.435. PMC 1731456. PMID 11376015.
- ^ Junkermann, H; von Holst, T; Lang, E; Rakov, V (14 February 2005). "Influence of different HRT regimens on mammographic density". Maturitas. 50 (2): 105–10. doi:10.1016/j.maturitas.2004.04.008. PMID 15653007.
- ^ a b Beck, KL; Anderson, MC; Kirk, JK (August 2017). "Transdermal estrogens in the changing landscape of hormone replacement therapy". Postgraduate Medicine. 129 (6): 632–636. doi:10.1080/00325481.2017.1334507. PMID 28540770. S2CID 205452835.
- ^ Martin, K. A.; Barbieri, R. L.; Crowley Jr., W. F. (September 24, 2021). "Preparations for menopausal hormone therapy". UpToDate. UpToDate. Retrieved February 2, 2022.
Not recommended. Depot estrogen—Estrogen is also available in some, but not all, countries as long-acting (three to four weeks) injections of either estradiol cypionate or estradiol valerate. Given the other effective estrogen options, we do not use this approach (table 1).
- ^ a b "FDA Takes Action Against Compounded Menopause Hormone Therapy Drugs". FDA. 2008-01-09. Retrieved 2009-02-17.
- ^ Cirigliano, M (June 2007). "Bioidentical hormone therapy: a review of the evidence". Journal of Women's Health. 16 (5): 600–31. doi:10.1089/jwh.2006.0311. PMID 17627398.
- ^ Simon JA (July 2014). "What if the Women's Health Initiative had used transdermal estradiol and oral progesterone instead?". Menopause. 21 (7): 769–83. doi:10.1097/GME.0000000000000169. PMID 24398406. S2CID 30292136.
- ^ a b Pinkerton, JV; Pickar, JH (February 2016). "Update on medical and regulatory issues pertaining to compounded and FDA-approved drugs, including hormone therapy". Menopause. 23 (2): 215–23. doi:10.1097/GME.0000000000000523. PMC 4927324. PMID 26418479.
- ^ a b c d Singer, Natasha (4 August 2009). "Medical Papers by Ghostwriters Pushed Therapy". The New York Times. Retrieved 13 July 2018.
- ^ a b c d e f Fugh-Berman AJ (September 2010). "The haunting of medical journals: how ghostwriting sold "HRT"". PLOS Med. 7 (9): e1000335. doi:10.1371/journal.pmed.1000335. PMC 2935455. PMID 20838656.
- ^ a b c d e f g Steve Kent May; Steve May (20 January 2012). Case Studies in Organizational Communication: Ethical Perspectives and Practices: Ethical Perspectives and Practices. SAGE. pp. 197–. ISBN 978-1-4129-8309-9.
- ^ a b Miller VM, Harman SM (November 2017). "An update on hormone therapy in postmenopausal women: mini-review for the basic scientist". Am. J. Physiol. Heart Circ. Physiol. 313 (5): H1013–H1021. doi:10.1152/ajpheart.00383.2017. PMC 5792205. PMID 28801526.
- ^ Sorkin, Andrew Ross; Wilson, Duff (2009-01-25). "Pfizer Agrees to Pay $68 Billion for Rival Drug Maker Wyeth". The New York Times.
- ^ "Pfizer Sizes Up: Closes $68B Wyeth Deal". CNBC. 2009-10-19.
- ^ Tao M, Teng Y, Shao H, Wu P, Mills EJ (2011). "Knowledge, perceptions and information about hormone therapy (HT) among menopausal women: a systematic review and meta-synthesis". PLOS ONE. 6 (9): e24661. Bibcode:2011PLoSO...624661T. doi:10.1371/journal.pone.0024661. PMC 3174976. PMID 21949743.
- ^ "Hormone therapy for brain performance: No effect, whether started early or late". www.sciencedaily.com.
- ^ Davies, M; Hamoda, H; British Menopause Society Medical Advisory, Council. (11 February 2019). "Hormone replacement therapy: changes in prescribing practice". BMJ (Clinical Research Ed.). 364: l633. doi:10.1136/bmj.l633. PMID 30745316. S2CID 73435897.