암 후생유전학
Cancer epigenetics암 후생유전학은 암세포의 DNA에 대한 후생유전학적 변형을 연구하는 것으로, 이는 뉴클레오티드 배열의 변화를 수반하지 않지만, 대신 유전 코드가 발현되는 방식에 변화를 수반한다.후생유전 메커니즘은 조직 특이적 유전자 발현의 정상적인 염기서열을 유지하기 위해 필요하며 정상적인 [1]발달에 중요하다.그것들은 세포의 암으로의 전환에서 유전자 돌연변이만큼 중요하거나 심지어 더 중요할 수 있다.암에서 후생유전적 과정의 교란은 돌연변이에 의한 것보다 전사 소음(CpG 섬의 후생유전적 촉진제 과메틸화에 의해 야기됨)에 의해 약 10배 더 자주 발생하는 유전자의 발현 상실을 초래할 수 있다.Vogelstein 외 연구진이 지적했듯이, 대장암의 경우 보통 3~6명의 운전자 돌연변이와 33~66명의 히치하이커 또는 승객 [2]돌연변이가 있다.단, 대장종양과 인접한 정상출현성대장점막에 비해 종양 내 유전자의 촉진제에는 약 600~800개의 중메틸화 CpG섬이 존재하지만 이들 CpG섬은 인접한 점막에서 [3][4][5]메틸화되지 않는다.후생유전적 변이의 조작은 암 예방, 발견, 치료에 [6][7]큰 가능성을 가지고 있다.다른 종류의 암에서는 종양억제유전자의 사일런트화, 변화된 CpG섬 메틸화 패턴에 의한 종양유전자의 활성화, 히스톤 수식 및 DNA 결합단백질의 조절장애 등 다양한 후생유전 메커니즘을 교란시킬 수 있다.후생유전적인 영향을 미치는 몇몇 약들이 현재 이러한 질병들 중 몇 가지에 사용되고 있다.
메커니즘
DNA메틸화
체세포에서 DNA 메틸화 패턴은 일반적으로 높은 [8]충실도로 딸세포에 전달된다.전형적으로, 이 메틸화는 고차 진핵생물의 [9]CpG 다이뉴클레오티드에서 구아노신에 5'에 위치한 세포신에서만 발생한다.그러나 후생유전자 DNA 메틸화는 인간의 정상세포와 종양세포 사이에 차이가 있다."정상적인" CpG 메틸화 프로파일은 종종 종양 [10]유발 세포에서 반전된다.정상 세포에서, 유전자 촉진제 이전의 CpG 섬은 일반적으로 비메틸화되어 전사적으로 활성화되는 경향이 있는 반면, 게놈 전체의 다른 개별 CpG 디뉴클레오티드는 메틸화되는 경향이 있다.단, 암세포에서는 종양억제유전자 촉진제 앞의 CpG섬이 과메틸화되는 경우가 많은 반면 종양유전자 촉진제 영역 및 기생 반복배열의 CpG 메틸화는 감소하는 [11]경우가 많다.
종양억제유전자 프로모터 영역의 과메틸화는 이들 유전자의 침묵을 초래할 수 있다.후생유전성 돌연변이는 세포가 통제불능으로 성장하고 번식하여 종양유전성을 [10]일으킨다.사이토신에 메틸기를 추가하면 DNA가 히스톤 단백질 주위에 단단히 감겨 전사를 거칠 수 없는 DNA가 생긴다.프로모터 과메틸화로 인해 전사적으로 침묵하는 것으로 일반적으로 밝혀진 유전자는 다음과 같습니다.세포주기억제제인 사이클린의존성인산화효소억제제 p16, DNA복구유전자 MGMT, 세포주기조절제인 APC, DNA복구유전자 MLH1, DNA복구유전자 [10][12]BRCA1.실제로 암세포는 후생유전자 [13]중독으로 알려진 일부 핵심 종양 억제 유전자의 과메틸화 촉진제 때문에 전사 사일링에 중독될 수 있다.
게놈의 다른 부분에서 CpG 디뉴클레오티드의 저메틸화는 각인 상실과 트랜스포저블 [14][15][16][17]요소의 재활성화와 같은 메커니즘으로 인해 염색체 불안정성을 초래한다.인슐린 유사 성장인자 유전자(IGF2)의 각인 상실은 대장암의 위험을 증가시키고 [18]신생아의 암 위험을 크게 증가시키는 벡위드 비데만 증후군과 관련이 있다.건강한 세포에서 낮은 밀도의 CpG 디뉴클레오티드는 부호화 및 비부호화 유전자 간 영역 내에서 발견된다.일부 반복 배열의 발현과 동원체에서의 감수성 재조합은 메틸화를 통해 억제된다.
암세포의 전체 게놈은 건강한 세포의 게놈보다 훨씬 적은 메틸시토신을 함유하고 있다.실제로 암세포 게놈은 [14][15][16][17]게놈 전체의 개별 CpG 디뉴클레오티드에서 메틸화가 20-50% 감소한다.프로모터 지역에서 발견되는 CpG 섬은 보통 DNA 메틸화로부터 보호된다.암세포에서 CpG 섬은 저메틸화된다 CpG 섬 해안이라고 불리는 CpG 섬 옆에 있는 지역은 CpG 디뉴클레오티드 맥락에서 대부분의 DNA 메틸화가 일어나는 곳입니다.암세포는 CpG섬 해안에서 경구적으로 메틸화된다.암세포에서는 CpG섬 해안의 과메틸화가 CpG섬으로 이동하거나 CpG섬의 저메틸화가 CpG섬 해안으로 이동하여 이들 유전자 [21]요소 사이의 명확한 후생유전학적 경계를 제거한다.암세포에서 DNA메틸전달효소(DNMT)의 교란으로 인한 "글로벌 저메틸화"는 유사분열 중 염색체가 제대로 분리되지 않을 때 궁극적으로 유사분열과 [14][15][16][17]염색체 재배열을 촉진할 수 있다.
CpG 섬 메틸화는 유전자 발현 조절에 중요하지만, 시토신 메틸화는 유전자 돌연변이를 불안정하게 하고 암 전 세포 상태를 직접적으로 초래할 수 있다.메틸화 사이토신은 아민기의 가수분해와 티민으로의 자발적 전환을 보다 유리하게 만든다.그것들은 염색질 단백질의 비정상적인 유입을 야기할 수 있다.시토신 메틸화는 뉴클레오티드 염기의 자외선 흡수량을 변화시켜 피리미딘 이합체를 생성한다.돌연변이가 종양 억제 유전자 부위의 헤테로 접합성을 상실하는 결과를 초래하면, 이러한 유전자들은 비활성화 될 수 있다.복제 중 단일 염기쌍 돌연변이도 악영향을 [12]미칠 수 있습니다.
히스톤 수식
진핵생물 DNA는 복잡한 구조를 가지고 있다.그것은 일반적으로 뉴클레오솜이라고 불리는 구조를 형성하기 위해 히스톤이라고 불리는 특별한 단백질에 싸여 있다.뉴클레오솜은 4개의 히스톤으로 구성된 2세트로 구성됩니다.H2A, H2B, H3, H4.또한 히스톤 H1은 뉴클레오솜 외부의 DNA 패키징에 기여한다.특정 히스톤 수정 효소는 히스톤에 작용기를 추가하거나 제거할 수 있으며, 이러한 수정은 히스톤을 둘러싼 유전자의 전사 수준과 DNA 복제 수준에 영향을 미친다.건강한 세포와 암세포의 히스톤 변형 프로파일은 다른 경향이 있다.
암세포는 건강한 세포에 비해 감소된 모노아세틸화 및 트리메틸화 히스톤 H4(감소 H4ac 및 H4me3)[22] 형태를 보인다.또한 마우스 모델에서는 p19의 히스톤 H4R3 비대칭 디메틸화(H4R3me2a)의 감소가 나타났다.ARF 프로모터는 종양 발생 및 [23]전이의 더 진행된 사례와 관련이 있다.마우스 모델에서 히스톤 H4 아세틸화와 트리메틸화의 손실은 종양 성장이 [22]계속됨에 따라 증가한다.텔로미어의 노화 표시인 히스톤 H4 Lysine 16 아세틸화(H4K16ac)의 손실은 아세틸화를 구체적으로 상실한다.일부 과학자들은 히스톤 아세틸화의 이러한 특별한 손실이 H4K16에 [10][24]특화된 HDAC인 SIRT1에 특화된 히스톤탈아세틸화효소(HDAC) 억제제와 싸울 수 있기를 바라고 있다.
종양유전과 관련된 다른 히스톤 마크로는 히스톤 H3 및 H4의 탈아세틸화 증가(아세틸화 감소), 히스톤 H3 리신 4(H3K4me3)의 트리메틸화 감소, 히스톤 H3 리신 9(H3K9me3)의 모노메틸화 증가 및 히스톤 H3의 트리메틸화 증가 등이 있다.이러한 히스톤 변형은 유전자의 CpG섬의 메틸화 감소에도 불구하고 종양 억제 유전자를 [25][26]침묵시킬 수 있습니다.
일부 연구는 아세틸화 히스톤에 대한 BRD4의 작용을 차단하는 데 초점을 맞추고 있는데, 이것은 몇몇 암과 관련된 Myc 단백질의 발현을 증가시키는 것으로 나타났다.BRD4에 결합하는 약물의 개발 과정은 팀이 [27]취하고 있는 협업적이고 개방적인 접근법에 주목할 만하다.
종양억제유전자 p53은 DNA수복을 조절하고 조절불량세포에서 아포토시스를 유도할 수 있다.E Soto-Reyes와 F Recillas-Targa는 p53 [28]발현 조절에서 CTCF 단백질의 중요성을 설명했다.CTCF 또는 CCCTC 결합 인자는 p53 프로모터가 억제성 히스톤 마크를 축적하지 않도록 절연하는 아연 핑거 단백질입니다.특정 종류의 암세포에서는 CTCF 단백질이 정상적으로 결합하지 않고 p53 프로모터가 억제 히스톤 마크를 축적하여 p53 발현을 [28]감소시킨다.
후생유전기계 자체의 돌연변이도 발생할 수 있으며, 암세포의 후생유전 프로파일 변화에 잠재적으로 책임이 있다.H2A 계열의 히스톤 변종들은 포유동물에서 매우 보존되어 염색질 구조를 변화시킴으로써 많은 핵 과정을 조절하는 데 중요한 역할을 한다.주요 H2A 변종 중 하나인 H2A.X는 DNA 손상을 나타내며, 게놈 무결성을 회복하기 위한 DNA 복구 단백질의 채용을 용이하게 한다.또 다른 변종인 H2A.Z는 유전자 활성화와 억제 모두에서 중요한 역할을 한다.높은 수준의 H2A.Z 발현은 많은 암에서 검출되며 세포 증식 및 [11]게놈 불안정성과 유의하게 관련되어 있습니다.히스톤 변이형 매크로H2A1은 간세포암 [29]등 여러 유형의 암 발생에 중요하다.다른 메커니즘 H4K16ac의 감소는 히스톤 acetyltransferases(HATs)의 활동에 감소 또는 아세틸 이탈에 SIRT1.[10]마찬가지로, HDAC2, 많은histone-tail lysines에 동작하는 히스톤 deacetylase에 있는inactivating 프레임 시프트 돌연 변이에 의해 증가하고 암을 변경 hist을 보이는 것으로 나타나 연결되어 왔다 때문에 발생할 수 있습니다.하나.아세틸화 [30]패턴이러한 발견은 효소 억제 또는 강화를 통해 후생유전 프로파일을 변경하기 위한 유망한 메커니즘을 나타낸다.
자외선, 이온화 방사선, 환경 독소, 대사 화학물질에 의해 야기되는 DNA 손상은 또한 게놈 불안정과 암을 초래할 수 있다.이중 가닥 DNA 파괴(DSB)에 대한 DNA 손상 반응은 부분적으로 히스톤 수식에 의해 매개된다.DSB에서 MRE11-RAD50-NBS1(MRN) 단백질 복합체는 히스톤2A의 세린129를 인산화시키는 아탁시아 텔랑지옥타지아 돌연변이(ATM) 키나제를 모집한다.DNA 손상 검사점 1의 매개체인 MDC1은 포스포펩타이드와 결합하며, H2AX의 인산화도 MRN-ATM의 모집 및 인산화 양의 피드백 루프에 의해 확산될 수 있다.TIP60은 δH2AX를 아세틸화시킨 후 폴리유비퀴틸화한다.DNA 수복형 유방암 1형 감수성 단백질 복합체(BRCA1-A)의 서브유닛인 RAP80은 히스톤에 부착된 유비퀴틴을 결합시킨다.BRCA1-A 활성은 G2/M 체크포인트에서 세포주기를 정지시켜 DNA 수복을 위한 시간을 허용하거나 아포토시스를 [31]시작할 수 있다.
마이크로RNA유전자사일링
포유동물에서, 마이크로 RNA는 단백질을 암호화하는 [32]유전자의 전사 활성의 약 60%를 조절합니다.또한 일부 miRNA는 [33][34]암세포에서 메틸화 관련 사일런싱을 거친다.Let-7과 miR15/16은 RAS와 BCL2 종양유전자를 하향 조절하는 데 중요한 역할을 하며, [18]이들의 침묵은 암세포에서 발생한다.전립선, 난소, 유방암, 글리아 세포암에서 종양 억제제 역할을 하는 miRNA인 miR-125b1의 발현 감소가 관찰되었다.시험관내 실험 결과 miR-125b1은 유방암과 관련된 두 개의 유전자, HER2/neu와 ESR1을 대상으로 하는 것으로 나타났다.DNA 메틸화, 특히 과메틸화는 miR-125b1이 후생적으로 무음화되는 주요 방법 중 하나이다.유방암 환자에서는 전사 시작 부위 근처에 위치한 CpG 섬의 과메틸화가 관찰되었다.CTCF 결합의 손실과 억제 히스톤 마크의 증가, H3K9me3, H3K27me3는 DNA 메틸화 및 miR-125b1 사일링과 관련이 있다.기계적으로 CTCF는 DNA 메틸화의 확산을 막기 위한 경계 요소로서 기능할 수 있다.Soto-Reyes [35]등에 의해 수행된 실험 결과는 miR-125b1의 기능과 발현에 대한 메틸화의 부정적인 영향을 나타낸다.따라서, 그들은 DNA 메틸화가 유전자를 침묵시키는 역할을 한다고 결론지었다.또한 일부 miRNA는 유방암 초기에 후생적으로 무음화되므로 이러한 miRNA는 종양 [35]마커로서 잠재적으로 유용할 수 있다.이상 DNA 메틸화에 의한 miRNA 유전자의 후생유전학적 침묵은 암세포에서 빈번한 사건이다. 정상 유방세포에서 활성화된 miRNA 프로모터의 거의 1/3은 유방암세포에서 과메틸화되었으며, 이는 보통 단백질 코딩 [36]유전자에 대해 관찰되는 것보다 몇 배 더 큰 비율이다.
암에서 후생유전학의 대사 기록
신진대사의 조절 장애는 종양세포가 필요한 구성 요소를 생성하고 후생유전적 표시를 조절하여 암의 시작과 진행을 지원하도록 한다.암에 의한 대사 변화는 후생유전적 지형, 특히 히스톤과 DNA의 변형을 변화시켜 악성 변형, 불충분한 영양에 대한 적응 및 전이를 촉진한다.암에서 특정 대사물의 축적은 후생유전효소를 표적으로 하여 후생유전적 지형을 전체적으로 변화시킬 수 있다.암 관련 대사 변화는 후생유전적 표시의 궤적 특이적 재기록으로 이어진다.1) 대사물에 의한 암 후생유전학의 용량응답 변조, 2) 대사효소의 배열 특이적 모집, 3) 영양신호에 [37]의한 후생유전효소의 표적화를 통해 세포대사에 의해 암 후생유전학을 정밀하게 재분류할 수 있다.
마이크로RNA 및 DNA 복구
DNA 손상은 [38][39]암의 주된 근본 원인인 것으로 보인다.DNA 복구가 부족하면 DNA 손상이 축적되는 경향이 있다.이러한 과도한 DNA 손상은 오류가 발생하기 쉬운 전이 합성으로 인해 DNA 복제 중 돌연변이 오류를 증가시킬 수 있습니다.과도한 DNA 손상은 또한 DNA 복구 [40][41]중 오류로 인한 후생유전학적 변화를 증가시킬 수 있다.이러한 돌연변이와 후생유전적 변화는 암을 유발할 수 있다(악성 종양 참조).
DNA 복구 유전자의 생식계 돌연변이는 대장암 [42]사례의 2 - 5%만 유발한다.그러나, DNA 복구 결핍을 야기하는 미세 RNA의 변화된 발현은 암과 자주 관련되며 이러한 암의 중요한 원인 인자가 될 수 있다.
특정 miRNA의 과잉 발현은 특정 DNA 복구 단백질의 발현을 직접적으로 감소시킬 수 있다.Wan [43]등은 괄호 안에 표시된 miRNA에 의해 직접 표적이 되는 6개의 DNA 복구 유전자를 언급했다. ATM(miR-421), RAD52(miR-210, miR-373), RAD23B(miR-373), MSH2(miR-21), BRCA1(miR-1853)더 최근에는 테시토어 [44]외ATM(miR-18a, miR-101), DNA-PK(miR-101), ATR(miR-185), Wip1(miR-16), MLH1, MSH2 및 MSH6(miR-155)를 포함한 추가 miRNA에 의해 직접 표적이 되는 추가 DNA 복구 유전자를 열거했다.이들 miRNA 중 miR-16, miR-18a, miR-21, miR-34c, miR-125b, miR-101, miR-155, miR-182, miR-185 및 miR-192는 Schnekenburger에 의해 식별되고 대장[45] 이상 발현된 것으로서 사망한다.이러한 miRNA 중 하나의 과잉 발현은 표적 DNA 복구 유전자의 발현 감소를 야기할 수 있다.
산발성 대장암에서 MLH1 결핍의 최대 15%는 MLH1 [46]발현을 억제하는 마이크로RNA miR-155의 과잉 발현으로 나타났다.그러나, DNA 불일치 복구 단백질 MLH1의 발현을 감소시킨 68개의 산발성 대장암 대부분은 MLH1 [47]유전자의 CpG 섬의 후생적 메틸화에 의해 결핍된 것으로 밝혀졌다.
교아세포종의 28%에서 MGMT DNA 복구 단백질은 결핍되지만 MGMT 프로모터는 [48]메틸화되지 않는다.메틸화 MGMT 촉진제가 없는 교아세포종에서 마이크로RNA miR-181d의 수준은 MGMT의 단백질 발현과 역상관되며 miR-181d의 직접 타깃은 MGMT mRNA 3'UTR(MGMT MRNA의 [48]3대 미번역 영역)이다.따라서 교아종의 28%에서 miR-181d의 발현 증가와 DNA 복구 효소 MGMT의 발현 감소가 원인 요인이 될 수 있다.교아종의 29~66%[48][49]에서, MGMT 유전자의 후생적 메틸화로 인해 DNA 복구가 부족하여 MGMT의 단백질 발현을 감소시킨다.
AT-훅으로 특징지어지는 고이동성 그룹 A(HMGA) 단백질은 전사를 변조할 수 있는 작은 비히스톤 염색질 관련 단백질이다.마이크로RNA는 HMGA 단백질의 발현을 제어하며, 이러한 단백질(HMGA1 및 HMGA2)은 구조적인 크로마틴 전사 제어 요소이다.Palmieri [50]et al.은 정상 조직에서 HGMA1 및 HMGA2 유전자가 miR-15, miR-16, miR-26a2, Let-7a에 의해 표적화(따라서 발현을 강하게 감소)된다는 것을 보여주었다.
HMGA 발현은 분화된 성인 조직에서는 거의 검출되지 않지만 많은 암에서 증가한다.HGMA 단백질은 모듈러 배열 구성에 의해 특징지어지는 최대 100개의 아미노산 잔류물의 폴리펩타이드이다.이 단백질들은 AT 후크라고 불리는 3개의 양전하를 띤 영역을 가지고 있으며, 이는 특정 DNA 영역에서 AT가 풍부한 DNA의 작은 홈과 결합한다.갑상선, 전립선, 자궁경부, 대장암, 췌장암, 난소암을 포함한 인간 종양은 HMGA1a와 HMGA1b 단백질의 [51]강한 증가를 보인다.림프세포를 대상으로 한 HMGA1을 가진 트랜스제닉 마우스는 공격성 림프종을 발생시켜 높은 HMGA1 발현이 암뿐만 아니라 [52]HMGA1 유전자가 암을 유발하는 종양 유전자로 작용할 수 있음을 보여준다.발다사르 외 연구진은 [53]HMGA1 단백질이 DNA 복구 유전자 BRCA1의 프로모터 영역에 결합하고 BRCA1 프로모터 활성을 억제한다는 것을 보여주었다.그들은 또한 유방암의 11%만이 BRCA1 유전자의 과메틸화를 가지고 있는 반면, 공격적인 유방암의 82%는 낮은 BRCA1 단백질 발현을 가지고 있으며, 이러한 감소의 대부분은 높은 수준의 HMGA1 단백질에 의한 염색질 리모델링에 의한 것임을 보여주었다.
HMGA2 단백질은 특히 ERCC1의 프로모터를 표적으로 하여 이 DNA 수복 [54]유전자의 발현을 감소시킨다.ERCC1 단백질 발현은 평가된 대장암 47개 중 100%에서 결핍되었다(HGMA2가 관여한 정도는 [55]알려지지 않았다).
Palmieri et al.[50]은 HMGA 유전자를 대상으로 하는 각각의 miRNA가 정상 뇌하수체와 비교했을 때 연구된 거의 모든 인간 뇌하수체 선종에서 급격하게 감소한다는 것을 보여주었다.이러한 HMGA 표적 miRNA의 하향 조절과 일관되게 HMGA1 및 HMGA2 특이 mRNA의 증가가 관찰되었다.이들 마이크로RNA 중 3개(miR-16, miR-196a 및 Let-7a)[45][56]는 메틸화 촉진제를 가지고 있어 대장암에서 발현률이 낮다.이들 중 두 가지 miR-15 및 miR-16의 경우 히스톤탈아세틸라아제 [57]활성에 의해 후생적으로 암에서 코드 영역이 무음화된다.이들 마이크로RNA가 낮은 수준에서 발현되면 HMGA1과 HMGA2 단백질이 높은 수준에서 발현된다.HMGA1 및 HMGA2 표적(발현 감소) BRCA1 및 ERCC1 DNA 복구 유전자.따라서 DNA 복구가 줄어들어 암 [39]진행에 기여할 수 있다.
DNA복구경로
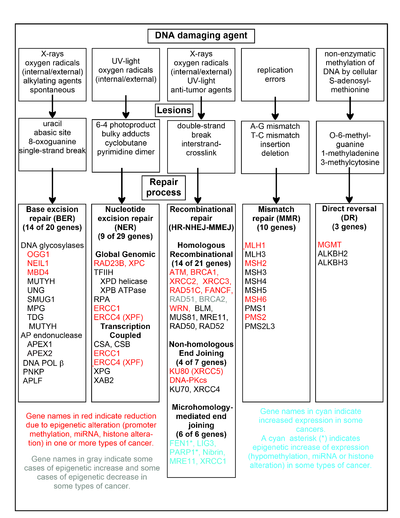
이 섹션의 차트는 몇 가지 빈번한 DNA 손상 물질, 그것이 야기하는 DNA 병변의 예, 그리고 이러한 DNA 손상을 다루는 경로를 보여줍니다.적어도 169개의 효소가 DNA 수복에 직접 이용되거나 DNA 수복 [58]과정에 영향을 준다.이 중 83개는 도표에 나타난 5가지 DNA 손상을 수리하는 데 직접 사용된다.
이러한 복구 과정의 핵심인 보다 잘 연구된 유전자 중 일부는 차트에 나와 있습니다.빨간색, 회색 또는 시안으로 표시된 유전자 명칭은 다양한 유형의 암에서 후생유전적으로 자주 변경되는 유전자를 나타냅니다.빨간색, 회색 또는 청록색으로 강조 표시된 각 유전자에 대한 위키피디아 기사는 후생유전학적 변화와 이러한 후생이 발견되는 암을 설명한다.두 개의 광범위한 실험 조사[59][60] 기사는 또한 암에서 이러한 후생적 DNA 복구 결핍의 대부분을 문서화한다.
빨간색으로 강조된 유전자는 다양한 암에서 후생유전 메커니즘에 의해 종종 감소되거나 침묵된다.이 유전자들이 발현이 낮거나 없을 때, DNA 손상이 축적될 수 있다.이러한 손상(트랜슬레이션 합성 참조)이 지난 복제 오류는 돌연변이를 증가시키고 궁극적으로 암을 유발할 수 있습니다.정확한 DNA 복구 경로에서 DNA 복구 유전자의 후생적 억제는 발암의 중심인 것으로 보인다.
상동 재조합 수복에는 회색으로 강조된 두 유전자 RAD51, BRCA2가 필요하다.그들은 때로는 후생적으로 과잉 발현되기도 하고 때로는 과소 발현되기도 한다.RAD51과 BRCA2에 관한 위키피디아 기사에서 알 수 있듯이, 그러한 암은 보통 다른 DNA 복구 유전자에 후생유전학적 결함을 가지고 있다.이러한 복구 결함으로 인해 복구되지 않은 DNA 손상이 증가할 수 있습니다.이러한 암에서 나타나는 RAD51 및 BRCA2의 과잉 발현은 보상 RAD51 또는 BRCA2 과잉 발현에 대한 선택적 압력과 그러한 과잉 DNA 손상을 최소한 부분적으로 다루기 위한 상동 재조합 수복 증가를 반영할 수 있다.RAD51 또는 BRCA2가 충분히 발현되지 않은 경우, 그 자체가 복구되지 않은 DNA 손상을 증가시킨다.이러한 손상을 통과한 복제 오류(트랜슬레이션 합성 참조)는 돌연변이와 암을 증가시킬 수 있으므로 RAD51 또는 BRCA2의 발현 부족 자체가 발암성이 될 수 있다.
시안 강조 유전자는 마이크로 호몰로지 매개 말단 결합(MMEJ) 경로에 있으며 암에서 상향 조절된다.MMEJ는 이중 스트랜드 절단에 대한 오류 발생 가능성이 높은 추가적인 부정확한 수리 경로입니다.이중 스트랜드 파단의 MMEJ 수리에서는 쌍으로 구성된 양쪽 스트랜드 사이의 5-25개의 상보적 베이스 쌍의 호몰로지는 스트랜드를 정렬하기에 충분하지만, 일반적으로 일치하지 않는 엔드(플랩)가 존재한다.MMEJ는 가닥이 연결된 여분의 뉴클레오티드(플랩)를 제거하고 가닥을 묶어 온전한 DNA 이중나선을 만든다.MMEJ는 거의 항상 작은 결실을 수반하므로 돌연변이 유발 [61]경로이다.MMEJ의 플랩 핵산가수분해효소인 FEN1은 후생적으로 저메틸화 프로모터에 의해 증가하며 유방암,[62] 전립선,[63] 위,[64][65] 신경아세포종,[66] [67]췌장 및 [68]폐의 대부분의 암에서 과잉 발현된다.PARP1은 프로모터 부위가 후생적으로 저메틸화되어 자궁내막암,[69][70] BRCA 변이 난소암 및 BRCA 변이 장액성 난소암 [71]진행에 기여하는 경우에도 과잉 발현된다.MMEJ 경로의 다른 유전자들도 다수의 암에서 과잉 발현되며(요약 내용은 MMEJ 참조), 파란색으로 표시된다.
DNA 복구 유전자의 에피메이션 빈도
정확한 DNA 복구 경로에서 기능하는 DNA 복구 단백질의 결핍은 돌연변이의 위험을 증가시킨다.돌연변이율은 DNA 불일치[72][73] 복구 또는 상동 재조합 복구(HRR)[74]에서 돌연변이를 가진 세포에서 크게 증가한다.34개의 DNA 복구 유전자 중 하나에서 유전적인 돌연변이를 가진 개인은 암에 걸릴 위험이 높아집니다(DNA 복구 결함 및 암 위험 증가 참조).
산발성 암의 경우 DNA 수복 유전자의 돌연변이에 의한 DNA 수복 부족이 종종 발견되지만, DNA 수복 유전자의 발현 감소 또는 부재는 유전자 발현을 감소 또는 침묵시키는 후생 유전자 변화 때문이다.예를 들어 순차적으로 검사한 대장암 113개의 경우, DNA 복구 유전자 MGMT에서 미센스 돌연변이를 보인 사람은 4명뿐이었고, 대부분은 MGMT 프로모터 영역의 메틸화로 인해 MGMT 발현을 감소시켰다(후생유전자 [75]변화).마찬가지로 DNA수복유전자 PMS2 발현이 결여된 119건의 불일치수복결손대장암 중 PMS2 단백질은 6건의 PMS2 유전자 돌연변이로 결핍된 반면, 103건의 경우 짝짓기 파트너 MLH1은 메틸촉진제(Abse 단백질의 불안정성)로 억제되어 PMS2 발현이 결핍된 것으로 나타났다.mlH1)의 [47]nce입니다.다른 10가지 사례에서, PMS2 발현 손실은 MLH1을 [46]하향 조절하는 마이크로RNA, miR-155의 후생성 과발현에 의한 것일 수 있다.
DNA 복구 유전자의 후생유전적 결함은 암에서 자주 발생한다.표에서 관심 있는 DNA 복구 유전자의 발현 감소 또는 부재에 대해 여러 암을 평가했으며, 표시된 빈도는 암이 유전자 발현 후생성 결핍을 가진 빈도이다.그러한 후생유전학적 결핍은 발암 초기에 발생할 수 있다. 이는 암이 발생할 가능성이 있는 암 주변의 현장 결함에서도 자주 발견되기 때문이다(표 참조).
| 암 | 진 | 암 발생 빈도 | 필드 결함의 빈도 | 레퍼런스 |
|---|---|---|---|---|
| 대장균 | 관리 | 46% | 34% | [76] |
| 대장균 | 관리 | 47% | 11% | [77] |
| 대장균 | 관리 | 70% | 60% | [78] |
| 대장균 | MSH2 | 13% | 5% | [77] |
| 대장균 | ERCC1 | 100% | 40% | [55] |
| 대장균 | PMS2 | 88% | 50% | [55] |
| 대장균 | XPF | 55% | 40% | [55] |
| 머리와 목 | 관리 | 54% | 38% | [79] |
| 머리와 목 | MLH1 | 33% | 25% | [80] |
| 머리와 목 | MLH1 | 31% | 20% | [81] |
| 배 | 관리 | 88% | 78% | [82] |
| 배 | MLH1 | 73% | 20% | [83] |
| 배 | ERCC1 | 95-100% | 14-65% | [84] |
| 배 | PMS2 | 95-100% | 14-60% | [84] |
| 식도 | MLH1 | 77%–100% | 23%–79% | [85] |
암은 하나 이상의 DNA 복구 효소의 발현에서 후생유전학적 감소에 의해 자주 발생할 수 있다.감소된 DNA 복구는 DNA 손상의 축적을 가능하게 할 것이다.이러한 DNA 손상 중 일부를 지나 오류가 발생하기 쉬운 전이 합성은 선택적 이점을 가진 돌연변이를 일으킬 수 있습니다.선택적 이점을 가진 클론 패치는 성장하여 인접 세포를 능가하여 필드 결함을 형성할 수 있다.세포가 DNA 수복을 감소시키는 뚜렷한 선택적인 이점은 없지만, 선택적으로 유리한 돌연변이를 가진 세포가 복제될 때 DNA 수복 유전자의 표상은 탑승자로서 휴대할 수 있다.DNA수복유전자의 에피메이션과 선택적 우위성을 가진 돌연변이를 모두 가진 세포에서는 더 많은 DNA 손상이 축적되어 결과적으로 더 큰 선택적 우위로 더 큰 돌연변이를 일으킬 수 있다.DNA 수복의 후생유전학적 결함은 암의 게놈에서 돌연변이의 특징적인 높은 빈도에 기여하고 암의 발암 진행을 유발할 수 있다.
암은 높은 돌연변이와 관련된 높은 수준의 게놈 불안정성을 가지고 있다.게놈 돌연변이의 빈도가 높으면 종양유전자를 활성화하고 종양억제유전자를 비활성화시켜 발암을 일으키는 특정 돌연변이가 발생할 가능성이 높아진다.전체 게놈 염기서열 분석을 바탕으로 암은 전체 [86]게놈에 수천에서 수십만 개의 돌연변이가 있는 것으로 밝혀졌다.(암의 돌연변이 빈도도 참조).이에 비해 인간(부모 대 자녀) 세대 간 전체 게놈의 돌연변이 빈도는 [87][88]세대당 약 70개의 새로운 돌연변이다.게놈의 단백질 코딩 영역에서는 부모/자녀 세대 간에 약 0.35개의 돌연변이([89]세대당 하나의 돌연변이 단백질 미만)만 존재한다.100세 된 일란성 쌍둥이 한 쌍에 대한 혈액 세포의 전체 게놈 배열 분석 결과, 비록 20% 미만의 혈액 세포에서 일어나는 체세포 변이가 [90]발견되지 않았지만, 오직 8개의 체세포 차이만을 발견했다.
DNA 손상은 오류가 발생하기 쉬운 전이 합성을 통해 돌연변이를 일으킬 수 있는 반면, DNA 손상은 또한 결함이 있는 DNA [40][41][91][92]복구 과정에서 후생유전학적 변화를 일으킬 수 있다.후생유전학적 DNA 복구 결함으로 인해 축적되는 DNA 손상은 암의 많은 유전자에서 발견되는 후생유전학적 변화의 원인이 될 수 있다.초기 연구에서, 제한된 일련의 전사 촉진제를 조사하면서, 페르난데스 [93]외 연구진은 855개의 1차 종양의 DNA 메틸화 프로파일을 조사했다.각 종양 유형을 해당 정상 조직과 비교한 결과, 729개의 CpG 섬 부위(평가된 1322개의 CpG 부위 중 55%)에서 차이 DNA 메틸화가 나타났다.이들 부위 중 496개가 과메틸화(억제)되었고 233개가 저메틸화(활성)되었다.따라서 종양에서는 후생 프로모터 메틸화 변화가 높다.이러한 후생유전학적 변화들 중 일부는 암 진행에 기여할 수 있다.
후생 발암 물질
다양한 화합물이 후생발암물질로 간주되어 종양 발생률이 증가하지만 돌연변이 유발 활성을 보이지 않는다(재생 증가를 유발하는 독성 화합물 또는 병원체도 제외되어야 한다).예를 들어 디에틸스틸베스트롤, 비산염, 헥사클로로벤젠 및 니켈 화합물이 있다.
많은 기형물질은 후생유전 [94][95]메커니즘에 의해 태아에게 특정한 영향을 미친다.후생유전학적 효과는 영향을 받는 아이의 일생 동안 디에틸스틸베스트롤과 같은 테라토겐의 효과를 보존할 수 있지만, 아버지나 2세대에 걸친 자손의 노출로 인한 선천적 기형의 가능성은 이론적인 근거와 [96]증거 부족으로 일반적으로 거부되어 왔다.그러나, 남성 매개 이상 범위가 입증되었고,[97] 더 많은 이상이 존재할 가능성이 있다.FDA는 5-아자시티딘(DNA에 통합될 때 저메틸화를 일으키는 시티딘의 비메틸화 유사물질)의 제제인 비다자에 대한 라벨 정보에서 "남성은 출산율 감소, 배아 손실 증가, 비정상적인 배아 발육의 증거를 인용하여 약을 사용하는 동안 "아이를 낳지 말 것"을 권고한다.쥐의 [98]경우 [99]모르핀에 노출된 수컷의 자손에서 내분비 차이가 관찰되었다.마우스에서는 후생유전 메커니즘에 [100]의해 디에틸스틸베스트롤의 2세대 효과가 발생하는 것으로 보고되었다.
암의 아형
피부암
흑색종은 멜라노사이트에서 발생하는 치명적인 피부암이다.몇몇 후생유전학적 변화는 멜라노사이트가 흑색종 세포로 이행하는 데 역할을 하는 것으로 알려져 있다.여기에는 DNA 염기서열을 변경하지 않고 유전될 수 있는 DNA 메틸화뿐만 아니라 오랜 [101]기간 자외선에 노출된 표피의 종양 억제 유전자를 침묵시키는 것도 포함됩니다.종양 억제 유전자의 침묵은 DNA 메틸화, DNA 메틸전달효소 및 히스톤 아세틸화의 [101]후생학적 변화와 연관된 광암 형성을 이끈다.이러한 변화는 해당 효소의 규제 해제의 결과이다.몇몇 [102]히스톤 메틸전달효소 및 데메틸라아제들이 이러한 효소들 중 하나이다.
전립선암
전립선암으로 인해 매년 약 35,000명의 남성이 사망하고 북미에서만 [103]약 22,000명의 남성이 전립선암으로 진단됩니다.전립선암은 남성에서 암으로 인한 사망의 두 번째 주요 원인이며, 한 사람이 평생 동안 6명 중 1명이 암에 [103]걸릴 것이다.히스톤 아세틸화와 DNA 메틸화의 변화는 전립선암에 영향을 미치는 다양한 유전자에서 발생하며 호르몬 [104]반응에 관여하는 유전자에서 나타났다.전립선암의 90% 이상이 서로 다른 산화제나 발암물질에 [105]의해 유발되는 유전자 손상으로부터 전립선 세포를 보호하는 GSTP1 유전자 프로모터의 CpG섬 과메틸화에 의한 유전자 소음화를 보인다.실시간 메틸화 특이적 중합효소 연쇄반응(PCR)은 다른 많은 유전자들도 [105]과메틸화됨을 시사한다.전립선의 유전자 발현은 영양과 생활습관의 [106]변화에 의해 조절될 수 있다.
자궁경부암
여성에게서 두 번째로 흔한 악성 종양은 침습성 자궁경부암(ICC)이며 모든 침습성 자궁경부암(ICC)의 50% 이상이 무공성 인간 유두종 바이러스 16(HPV16)[107]에 의해 발생한다.또한 자궁경부 상피내신생물증(CIN)은 주로 발암성 HPV16에 [107]의해 발생한다.많은 경우처럼 암의 원인인자가 항상 감염에서 암 발병으로 직접 연결되는 것은 아니다.유전체 메틸화 패턴은 침습성 자궁경부암과 관련이 있다.HPV16L1 영역 내에서 14개의 테스트된 CpG 사이트는 CIN3가 없는 여성의 HPV16 게놈보다 CIN3+[107]에서 유의하게 높은 메틸화를 보였다.HPV16 상류 규제 영역에서 테스트한 2/16 CpG 사이트만 CIN3+[107]의 메틸화 증가와 관련이 있는 것으로 밝혀졌다.이것은 감염에서 암으로 가는 직접적인 경로가 자궁경부 상피내 종양에서 때때로 전암 상태로 우회된다는 것을 암시한다.또한 5/5 TERT, 1/4 DAPK1, 2/5 RARB, MAL,[107] CADM1을 포함한 연구 대상 5개 숙주핵유전자 대부분에서 CpG 부위 메틸화 증가가 확인되었으며, 또한 미토콘드리아 DNA의 CpG 부위 1/3이 CIN+[107]3에서 메틸화 증가와 관련이 있었다.따라서 HPV16 L1 [107]오픈 판독 프레임에서 CpG 부위의 메틸화 증가와 CIN3+ 사이에는 상관관계가 존재한다.이것은 암과 전암 자궁경부 [107]질환의 미래 검사에서 잠재적인 바이오마커가 될 수 있다.
백혈병
최근 연구에 따르면 혼합계열백혈병(MLL) 유전자는 후생유전학적 [108]통제 하에 있는 다른 염색체의 다른 유전자와 재배열하고 융합함으로써 백혈병을 유발한다.MLL의 돌연변이는 HOX [109]유전자에 의해 제어되는 악성 변형을 일으키는 백혈병과 관련된 전위 또는 삽입에서 올바른 조절 영역을 차단한다.이것이 백혈구의 증가를 이끈다.백혈병 관련 유전자는 후생유전학, 신호전달, 전사조절, 에너지 대사를 제어하는 동일한 경로로 관리된다.감염, 전자장, 출생 체중 증가가 [110]백혈병의 원인이 될 수 있다고 지적되었다.
육종
미국에서는 매년 약 15,000건의 새로운 육종 환자가 발생하고 있으며,[111] 2014년에는 약 6,200명이 육종으로 사망할 것으로 예측되고 있다.육종은 연골육종, 유잉육종, 평활근종, 지방육종, 골육종, 활액육종, 활액육종, 그리고 (치경 및 배아) 횡문근육종을 포함하는 많은 희귀 조직학적으로 이질적인 간엽성 종양을 포함한다.몇몇 종양유전자와 종양억제 유전자는 육종에서 후생유전적으로 변화한다.여기에는 APC, CDKN1A, CDKN2A, CDKN2B, Ezrin, FGFR1, GADD45A, MGMT, STK3, STK4, PTEN, RASSF1A, WIF1 등이 포함됩니다.[112]연골육종, 유잉육종 및 골육종에서는 PRC1 복합체의 BMI1 성분 등의 후생성 수식제의 발현이 규제 해제되고 유잉육종 및 횡문근육종에서는 PRC2 복합체의 EZH2 성분의 발현이 변화한다.마찬가지로 연골육종, 유잉육종, 골육종 및 횡문근육종에서 또 다른 후생유전학적 수식제인 LSD1 히스톤 데메틸라아제의 발현이 증가한다.유잉 육종에서 [113]EZH2의 표적화 및 억제, 또는 여러 [114]육종에서 LSD1의 약물화는 이들 육종에서 종양세포의 성장을 억제한다.
식별 방법
이전에 후생유전자 프로파일은 특정 연구팀에 의해 정밀 조사 중인 개별 유전자로 제한되었다.그러나 최근 과학자들은 암세포와 건강한 [10]세포에 대한 전체 게놈 프로파일을 결정하기 위해 보다 게놈적인 접근으로 나아가고 있다.
세포 내 CpG 메틸화를 측정하기 위한 일반적인 접근법은 다음과 같다.
- 아황산수소염 배열법
- 복합 아황산염 제한 분석(COBRA)
- 메틸화 특이 PCR
- 메티라이트
- 파이로시퀀싱
- 제한 랜드마크 게놈 스캔
- 임의의 프라이밍 PCR
- HELP 어세이(Hpa)II 결찰 매개 PCR에 의한 미세 단편 농축)
- 메틸-CpG 결합 도메인 단백질 특이 항체를 이용한 크로마틴 면역침강 ChIP-Chip
- 메틸화DNA면역침강메틸-DIP
- DNA 마이크로어레이를 통한 유전자 발현 프로파일 : 치료 전후의 암세포주 mRNA 수치와 탈메틸화제 비교
CpG 메틸화 측정을 위한 황금 표준으로 간주되기 때문에 다른 방법 중 하나를 사용할 경우, 결과는 보통 중황산염 배열[1]을 사용하여 확인된다.암세포 대 건강한 세포에서 히스톤 변형 프로파일을 결정하기 위한 일반적인 접근법에는 다음이 포함된다.[10]
- 질량 분석
- 염색질 면역 침강 검사
진단 및 예후
연구자들은 이러한 프로파일을 개인을 보다 구체적이고 [10]정확하게 진단하기 위한 도구로서 사용하는 것을 목표로 암의 다양한 종류와 아형의 특정한 후생유전학적 프로파일을 확인하기를 희망하고 있다.후생유전학적 프로파일이 바뀌기 때문에 과학자들은 환자의 특정 암 발병 단계나 공격성 수준을 결정하기 위해 다른 후생유전학적 프로파일을 사용하기를 원한다.예를 들어, Death-Associated Protein Kinase(DAPK), p16 및 상피막 단백질 3(EMP3)를 코드하는 유전자의 과메틸화는 보다 공격적인 형태의 폐암,[17] 대장암 및 뇌암과 관련이 있다.이런 종류의 지식은 의사들이 환자를 진단하고 치료하는 방법에 영향을 미칠 수 있다.
환자의 치료에 영향을 미치는 또 다른 요인은 환자가 특정 치료에 얼마나 잘 반응하는지 아는 것입니다.암세포의 개인화된 후생유전학적 프로파일은 이 분야에 대한 통찰력을 제공할 수 있다.예를 들어, MGMT는 뉴클레오티드 구아닌에 [115]대한 알킬기의 첨가를 역전시키는 효소이다.그러나 알킬화 구아닌은 DNA를 교란시키고 세포사를 [116][117][118][119]일으키기 위해 여러 화학요법 약물이 작용하는 메커니즘이다.따라서 암세포에서 MGMT를 코드하는 유전자가 과메틸화되어 실질적으로 침묵 또는 억제된다면 기능성 MGMT 효소를 가진 암세포보다 구아닌을 메틸화함으로써 작용하는 화학요법 약물이 더 효과적일 것이다.
후생생물학적 바이오마커는 분자 예후를 위한 도구로 사용될 수도 있다.1차 종양 및 종격 림프절 생검 샘플에서 CDKN2A와 CDH13의 과메틸화는 암 재발의 빠른 위험과 [120]환자의 높은 사망률의 지표 역할을 한다.
치료
히스톤의 구조변화에 의한 원생온코 영역과 종양억제서열의 후생적 제어는 [121]암의 형성 및 진행에 관여한다.후생유전학적 변화를 되돌리는 약물은 다양한 [104][121][122]암에서 역할을 할 수 있다.
최근 특정 암 조직형과 후생유전학적 변화 사이의 연관성이 새로운 후생약 [123]개발을 촉진할 수 있다는 것이 명백하게 알려져 있다.약물 개발은 주로 DNA 메틸전달효소, 히스톤아세틸전달효소(HAT), 히스톤탈아세틸화효소(HDAC)[124]를 수정하는 데 초점이 맞춰져 있다.
암세포의 역메틸화 패턴을 특이적으로 표적으로 하는 약물은 DNA메틸전달효소 억제제인 아자시티딘과[125][126] [127][128]데시타빈을 포함한다.이 하이포메틸화제들은 비정상적인 골수줄기세포에 [12]의해 생성되는 혈액암인 골수이형성증후군을 [129]치료하는데 사용된다.이들 약물은 세 가지 유형의 활성 DNA 메틸전달효소를 모두 억제하고 독성이 강한 것으로 여겨졌으나 저용량 사용 시 효과가 입증되어 골수이형성증후군의 [130]백혈병 진행을 감소시켰다.
히스톤탈아세틸라아제(HDAC) 억제제는 T세포 림프종 치료에 효과를 나타낸다.두 가지 HDAC 억제제인 보리노스타트와 로미덱신이 식품의약품안전청에 [131][132]의해 승인되었습니다.그러나 이들 HDAC 억제제는 관심 히스톤 외에 많은 단백질의 아세틸화 상태를 변화시키기 때문에 이러한 억제제를 치료제로 사용하는 [18]효율성을 높이기 위해 환자 반응의 분자 수준에서 기초 메커니즘에 대한 지식이 필요하다.HDAC 억제제를 사용한 치료는 DNA 메틸전달효소 억제제가 [133]전사를 억제한 후 유전자 재활성화를 촉진하는 것으로 밝혀졌다.Panobinostat은 골수종의 [134]특정 상황에 대해 승인되었습니다.
연구 대상으로는 히스톤리신메틸전달효소(KMT)와 단백질 아르기닌메틸전달효소(PRMT)[135]가 있다.임상 전 연구는 루나신이 잠재적으로 유익한 후생유전학적 효과를 [136]가질 수 있다는 것을 시사했다.
「 」를 참조해 주세요.
레퍼런스
- ^ Sharma, S.; Kelly, T. K.; Jones, P. A. (2010-01-01). "Epigenetics in cancer". Carcinogenesis. 31 (1): 27–36. doi:10.1093/carcin/bgp220. ISSN 0143-3334. PMC 2802667. PMID 19752007.
- ^ Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA, Kinzler KW (March 2013). "Cancer genome landscapes". Science. 339 (6127): 1546–58. Bibcode:2013Sci...339.1546V. doi:10.1126/science.1235122. PMC 3749880. PMID 23539594.
- ^ Illingworth RS, Gruenewald-Schneider U, Webb S, Kerr AR, James KD, Turner DJ, Smith C, Harrison DJ, Andrews R, Bird AP (September 2010). "Orphan CpG islands identify numerous conserved promoters in the mammalian genome". PLOS Genetics. 6 (9): e1001134. doi:10.1371/journal.pgen.1001134. PMC 2944787. PMID 20885785.
- ^ Wei J, Li G, Dang S, Zhou Y, Zeng K, Liu M (2016). "Discovery and Validation of Hypermethylated Markers for Colorectal Cancer". Disease Markers. 2016: 2192853. doi:10.1155/2016/2192853. PMC 4963574. PMID 27493446.
- ^ Beggs AD, Jones A, El-Bahrawy M, El-Bahwary M, Abulafi M, Hodgson SV, Tomlinson IP (April 2013). "Whole-genome methylation analysis of benign and malignant colorectal tumours". The Journal of Pathology. 229 (5): 697–704. doi:10.1002/path.4132. PMC 3619233. PMID 23096130.
- ^ Novak K (December 2004). "Epigenetics changes in cancer cells". MedGenMed. 6 (4): 17. PMC 1480584. PMID 15775844.
- ^ Banno K, Kisu I, Yanokura M, Tsuji K, Masuda K, Ueki A, Kobayashi Y, Yamagami W, Nomura H, Tominaga E, Susumu N, Aoki D (September 2012). "Epimutation and cancer: a new carcinogenic mechanism of Lynch syndrome (Review)". International Journal of Oncology. 41 (3): 793–7. doi:10.3892/ijo.2012.1528. PMC 3582986. PMID 22735547.
- ^ Bird A (January 2002). "DNA methylation patterns and epigenetic memory". Genes & Development. 16 (1): 6–21. doi:10.1101/gad.947102. PMID 11782440.
- ^ Herman, James G.; Graff, Jeremy R.; Myöhänen, Sanna; Nelkin, Barry D.; Baylin, Stephen B. (September 1996). "Methylation-specific PCR: A novel PCR assay for methylation status of CpG islands". Proceedings of the National Academy of Sciences of the United States of America. 93 (18): 9821–6. Bibcode:1996PNAS...93.9821H. doi:10.1073/pnas.93.18.9821. PMC 38513. PMID 8790415.
- ^ a b c d e f g h Esteller M (April 2007). "Cancer epigenomics: DNA methylomes and histone-modification maps". Nature Reviews Genetics. 8 (4): 286–98. doi:10.1038/nrg2005. PMID 17339880. S2CID 4801662.
- ^ a b Wong NC, Craig JM (2011). Epigenetics: A Reference Manual. Norfolk, England: Caister Academic Press. ISBN 978-1-904455-88-2.
- ^ a b c Jones PA, Baylin SB (June 2002). "The fundamental role of epigenetic events in cancer". Nature Reviews Genetics. 3 (6): 415–28. doi:10.1038/nrg816. PMID 12042769. S2CID 2122000.
- ^ De Carvalho DD, Sharma S, You JS, Su SF, Taberlay PC, Kelly TK, Yang X, Liang G, Jones PA (May 2012). "DNA methylation screening identifies driver epigenetic events of cancer cell survival". Cancer Cell. 21 (5): 655–67. doi:10.1016/j.ccr.2012.03.045. PMC 3395886. PMID 22624715.
- ^ a b c Herman JG, Baylin SB (November 2003). "Gene silencing in cancer in association with promoter hypermethylation". The New England Journal of Medicine. 349 (21): 2042–54. doi:10.1056/NEJMra023075. PMID 14627790.
- ^ a b c Feinberg AP, Tycko B (February 2004). "The history of cancer epigenetics". Nature Reviews. Cancer. 4 (2): 143–53. doi:10.1038/nrc1279. PMID 14732866. S2CID 31655008.
- ^ a b c Egger G, Liang G, Aparicio A, Jones PA (May 2004). "Epigenetics in human disease and prospects for epigenetic therapy". Nature. 429 (6990): 457–63. Bibcode:2004Natur.429..457E. doi:10.1038/nature02625. PMID 15164071. S2CID 4424126.
- ^ a b c d Esteller M (2005). "Aberrant DNA methylation as a cancer-inducing mechanism". Annual Review of Pharmacology and Toxicology. 45: 629–56. doi:10.1146/annurev.pharmtox.45.120403.095832. PMID 15822191.
- ^ a b c Baylin SB, Jones PA (September 2011). "A decade of exploring the cancer epigenome - biological and translational implications". Nature Reviews. Cancer. 11 (10): 726–34. doi:10.1038/nrc3130. PMC 3307543. PMID 21941284.
- ^ Ellermeier C, Higuchi EC, Phadnis N, Holm L, Geelhood JL, Thon G, Smith GR (May 2010). "RNAi and heterochromatin repress centromeric meiotic recombination". Proceedings of the National Academy of Sciences of the United States of America. 107 (19): 8701–5. Bibcode:2010PNAS..107.8701E. doi:10.1073/pnas.0914160107. PMC 2889303. PMID 20421495.
- ^ Esteller M (April 2007). "Cancer epigenomics: DNA methylomes and histone-modification maps". Nature Reviews Genetics. 8 (4): 286–98. doi:10.1038/nrg2005. PMID 17339880. S2CID 4801662.
- ^ Timp W, Feinberg AP (July 2013). "Cancer as a dysregulated epigenome allowing cellular growth advantage at the expense of the host". Nature Reviews. Cancer. 13 (7): 497–510. doi:10.1038/nrc3486. PMC 4636434. PMID 23760024.
- ^ a b Fraga MF, Ballestar E, Villar-Garea A, Boix-Chornet M, Espada J, Schotta G, Bonaldi T, Haydon C, Ropero S, Petrie K, Iyer NG, Pérez-Rosado A, Calvo E, Lopez JA, Cano A, Calasanz MJ, Colomer D, Piris MA, Ahn N, Imhof A, Caldas C, Jenuwein T, Esteller M (April 2005). "Loss of acetylation at Lys16 and trimethylation at Lys20 of histone H4 is a common hallmark of human cancer". Nature Genetics. 37 (4): 391–400. doi:10.1038/ng1531. PMID 15765097. S2CID 27245550.
- ^ Aprelikova O, Chen K, El Touny LH, Brignatz-Guittard C, Han J, Qiu T, Yang HH, Lee MP, Zhu M, Green JE (Apr 2016). "The epigenetic modifier JMJD6 is amplified in mammary tumors and cooperates with c-Myc to enhance cellular transformation, tumor progression, and metastasis". Clinical Epigenetics. 8 (38): 38. doi:10.1186/s13148-016-0205-6. PMC 4831179. PMID 27081402.
- ^ Dang W, Steffen KK, Perry R, Dorsey JA, Johnson FB, Shilatifard A, Kaeberlein M, Kennedy BK, Berger SL (June 2009). "Histone H4 lysine 16 acetylation regulates cellular lifespan". Nature. 459 (7248): 802–7. Bibcode:2009Natur.459..802D. doi:10.1038/nature08085. PMC 2702157. PMID 19516333.
- ^ Viré E, Brenner C, Deplus R, Blanchon L, Fraga M, Didelot C, Morey L, Van Eynde A, Bernard D, Vanderwinden JM, Bollen M, Esteller M, Di Croce L, de Launoit Y, Fuks F (February 2006). "The Polycomb group protein EZH2 directly controls DNA methylation". Nature. 439 (7078): 871–4. Bibcode:2006Natur.439..871V. doi:10.1038/nature04431. PMID 16357870. S2CID 4409726.
- ^ Richon VM, Sandhoff TW, Rifkind RA, Marks PA (August 2000). "Histone deacetylase inhibitor selectively induces p21WAF1 expression and gene-associated histone acetylation". Proceedings of the National Academy of Sciences of the United States of America. 97 (18): 10014–9. Bibcode:2000PNAS...9710014R. doi:10.1073/pnas.180316197. JSTOR 123305. PMC 27656. PMID 10954755.
- ^ Maxmen A (August 2012). "Cancer research: Open ambition". Nature. 488 (7410): 148–50. Bibcode:2012Natur.488..148M. doi:10.1038/488148a. PMID 22874946.
- ^ a b Soto-Reyes E, Recillas-Targa F (April 2010). "Epigenetic regulation of the human p53 gene promoter by the CTCF transcription factor in transformed cell lines". Oncogene. 29 (15): 2217–27. doi:10.1038/onc.2009.509. PMID 20101205.
- ^ Rappa F, Greco A, Podrini C, Cappello F, Foti M, Bourgoin L, Peyrou M, Marino A, Scibetta N, Williams R, Mazzoccoli G, Federici M, Pazienza V, Vinciguerra M (2013). Folli F (ed.). "Immunopositivity for histone macroH2A1 isoforms marks steatosis-associated hepatocellular carcinoma". PLOS ONE. 8 (1): e54458. Bibcode:2013PLoSO...854458R. doi:10.1371/journal.pone.0054458. PMC 3553099. PMID 23372727.
- ^ Ropero S, Fraga MF, Ballestar E, Hamelin R, Yamamoto H, Boix-Chornet M, Caballero R, Alaminos M, Setien F, Paz MF, Herranz M, Palacios J, Arango D, Orntoft TF, Aaltonen LA, Schwartz S, Esteller M (May 2006). "A truncating mutation of HDAC2 in human cancers confers resistance to histone deacetylase inhibition". Nature Genetics. 38 (5): 566–9. doi:10.1038/ng1773. PMID 16642021. S2CID 9073684.
- ^ van Attikum H, Gasser SM (May 2009). "Crosstalk between histone modifications during the DNA damage response". Trends in Cell Biology. 19 (5): 207–17. doi:10.1016/j.tcb.2009.03.001. PMID 19342239.
- ^ Friedman RC, Farh KK, Burge CB, Bartel DP (January 2009). "Most mammalian mRNAs are conserved targets of microRNAs". Genome Research. 19 (1): 92–105. doi:10.1101/gr.082701.108. PMC 2612969. PMID 18955434.
- ^ Saito Y, Liang G, Egger G, Friedman JM, Chuang JC, Coetzee GA, Jones PA (June 2006). "Specific activation of microRNA-127 with downregulation of the proto-oncogene BCL6 by chromatin-modifying drugs in human cancer cells". Cancer Cell. 9 (6): 435–43. doi:10.1016/j.ccr.2006.04.020. PMID 16766263.
- ^ Lujambio A, Ropero S, Ballestar E, Fraga MF, Cerrato C, Setién F, Casado S, Suarez-Gauthier A, Sanchez-Cespedes M, Git A, Gitt A, Spiteri I, Das PP, Caldas C, Miska E, Esteller M (February 2007). "Genetic unmasking of an epigenetically silenced microRNA in human cancer cells". Cancer Research. 67 (4): 1424–9. doi:10.1158/0008-5472.CAN-06-4218. PMID 17308079.
- ^ a b Soto-Reyes E, González-Barrios R, Cisneros-Soberanis F, Herrera-Goepfert R, Pérez V, Cantú D, Prada D, Castro C, Recillas-Targa F, Herrera LA (January 2012). "Disruption of CTCF at the miR-125b1 locus in gynecological cancers". BMC Cancer. 12: 40. doi:10.1186/1471-2407-12-40. PMC 3297514. PMID 22277129.
- ^ Vrba L, Muñoz-Rodríguez JL, Stampfer MR, Futscher BW (2013). "miRNA gene promoters are frequent targets of aberrant DNA methylation in human breast cancer". PLOS ONE. 8 (1): e54398. Bibcode:2013PLoSO...854398V. doi:10.1371/journal.pone.0054398. PMC 3547033. PMID 23342147.
- ^ Wang YP, Lei QY (May 2018). "Metabolic recoding of epigenetics in cancer". Cancer Communications. 38 (1): 25. doi:10.1186/s40880-018-0302-3. PMC 5993135. PMID 29784032.
- ^ Kastan MB (2008). "DNA damage responses: mechanisms and roles in human disease: 2007 G.H.A. Clowes Memorial Award Lecture". Mol. Cancer Res. 6 (4): 517–24. doi:10.1158/1541-7786.MCR-08-0020. PMID 18403632.
- ^ a b Bernstein C, Prasad AR, Nfonsam V, Bernstein H (2013). "Chapter 16: DNA Damage, DNA Repair and Cancer". In Chen C (ed.). New Research Directions in DNA Repair. p. 413. ISBN 978-953-51-1114-6.
- ^ a b O'Hagan HM, Mohammad HP, Baylin SB (August 2008). "Double strand breaks can initiate gene silencing and SIRT1-dependent onset of DNA methylation in an exogenous promoter CpG island". PLOS Genetics. 4 (8): e1000155. doi:10.1371/journal.pgen.1000155. PMC 2491723. PMID 18704159.
- ^ a b Cuozzo C, Porcellini A, Angrisano T, Morano A, Lee B, Di Pardo A, Messina S, Iuliano R, Fusco A, Santillo MR, Muller MT, Chiariotti L, Gottesman ME, Avvedimento EV (July 2007). "DNA damage, homology-directed repair, and DNA methylation". PLOS Genetics. 3 (7): e110. doi:10.1371/journal.pgen.0030110. PMC 1913100. PMID 17616978.
- ^ Jasperson KW, Tuohy TM, Neklason DW, Burt RW (June 2010). "Hereditary and familial colon cancer". Gastroenterology. 138 (6): 2044–58. doi:10.1053/j.gastro.2010.01.054. PMC 3057468. PMID 20420945.
- ^ Wan G, Mathur R, Hu X, Zhang X, Lu X (September 2011). "miRNA response to DNA damage". Trends in Biochemical Sciences. 36 (9): 478–84. doi:10.1016/j.tibs.2011.06.002. PMC 3532742. PMID 21741842.
- ^ Tessitore A, Cicciarelli G, Del Vecchio F, Gaggiano A, Verzella D, Fischietti M, Vecchiotti D, Capece D, Zazzeroni F, Alesse E (2014). "MicroRNAs in the DNA Damage/Repair Network and Cancer". International Journal of Genomics. 2014: 820248. doi:10.1155/2014/820248. PMC 3926391. PMID 24616890.
- ^ a b Schnekenburger M, Diederich M (March 2012). "Epigenetics Offer New Horizons for Colorectal Cancer Prevention". Current Colorectal Cancer Reports. 8 (1): 66–81. doi:10.1007/s11888-011-0116-z. PMC 3277709. PMID 22389639.
- ^ a b Valeri N, Gasparini P, Fabbri M, Braconi C, Veronese A, Lovat F, Adair B, Vannini I, Fanini F, Bottoni A, Costinean S, Sandhu SK, Nuovo GJ, Alder H, Gafa R, Calore F, Ferracin M, Lanza G, Volinia S, Negrini M, McIlhatton MA, Amadori D, Fishel R, Croce CM (April 2010). "Modulation of mismatch repair and genomic stability by miR-155". Proceedings of the National Academy of Sciences of the United States of America. 107 (15): 6982–7. Bibcode:2010PNAS..107.6982V. doi:10.1073/pnas.1002472107. JSTOR 25665289. PMC 2872463. PMID 20351277.
- ^ a b Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers JO, Bannwart F, Yurtsever H, Neuweiler J, Riehle HM, Cattaruzza MS, Heinimann K, Schär P, Jiricny J, Marra G (May 2005). "Immunohistochemical analysis reveals high frequency of PMS2 defects in colorectal cancer". Gastroenterology. 128 (5): 1160–71. doi:10.1053/j.gastro.2005.01.056. PMID 15887099.
- ^ a b c Zhang W, Zhang J, Hoadley K, Kushwaha D, Ramakrishnan V, Li S, Kang C, You Y, Jiang C, Song SW, Jiang T, Chen CC (June 2012). "miR-181d: a predictive glioblastoma biomarker that downregulates MGMT expression". Neuro-Oncology. 14 (6): 712–9. doi:10.1093/neuonc/nos089. PMC 3367855. PMID 22570426.
- ^ Spiegl-Kreinecker S, Pirker C, Filipits M, Lötsch D, Buchroithner J, Pichler J, Silye R, Weis S, Micksche M, Fischer J, Berger W (January 2010). "O6-Methylguanine DNA methyltransferase protein expression in tumor cells predicts outcome of temozolomide therapy in glioblastoma patients". Neuro-Oncology. 12 (1): 28–36. doi:10.1093/neuonc/nop003. PMC 2940563. PMID 20150365.
- ^ a b Palmieri D, D'Angelo D, Valentino T, De Martino I, Ferraro A, Wierinckx A, Fedele M, Trouillas J, Fusco A (August 2012). "Downregulation of HMGA-targeting microRNAs has a critical role in human pituitary tumorigenesis". Oncogene. 31 (34): 3857–65. doi:10.1038/onc.2011.557. PMID 22139073.
- ^ Sgarra R, Rustighi A, Tessari MA, Di Bernardo J, Altamura S, Fusco A, Manfioletti G, Giancotti V (September 2004). "Nuclear phosphoproteins HMGA and their relationship with chromatin structure and cancer". FEBS Letters. 574 (1–3): 1–8. doi:10.1016/j.febslet.2004.08.013. PMID 15358530. S2CID 28903539.
- ^ Xu Y, Sumter TF, Bhattacharya R, Tesfaye A, Fuchs EJ, Wood LJ, Huso DL, Resar LM (May 2004). "The HMG-I oncogene causes highly penetrant, aggressive lymphoid malignancy in transgenic mice and is overexpressed in human leukemia". Cancer Research. 64 (10): 3371–5. doi:10.1158/0008-5472.CAN-04-0044. PMID 15150086.
- ^ Baldassarre G, Battista S, Belletti B, Thakur S, Pentimalli F, Trapasso F, Fedele M, Pierantoni G, Croce CM, Fusco A (April 2003). "Negative regulation of BRCA1 gene expression by HMGA1 proteins accounts for the reduced BRCA1 protein levels in sporadic breast carcinoma". Molecular and Cellular Biology. 23 (7): 2225–38. doi:10.1128/MCB.23.7.2225-2238.2003. PMC 150734. PMID 12640109.
- ^ Borrmann L, Schwanbeck R, Heyduk T, Seebeck B, Rogalla P, Bullerdiek J, Wisniewski JR (December 2003). "High mobility group A2 protein and its derivatives bind a specific region of the promoter of DNA repair gene ERCC1 and modulate its activity". Nucleic Acids Research. 31 (23): 6841–51. doi:10.1093/nar/gkg884. PMC 290254. PMID 14627817.
- ^ a b c d Facista A, Nguyen H, Lewis C, Prasad AR, Ramsey L, Zaitlin B, Nfonsam V, Krouse RS, Bernstein H, Payne CM, Stern S, Oatman N, Banerjee B, Bernstein C (April 2012). "Deficient expression of DNA repair enzymes in early progression to sporadic colon cancer". Genome Integrity. 3 (1): 3. doi:10.1186/2041-9414-3-3. PMC 3351028. PMID 22494821.
- ^ Malumbres M (2013). "miRNAs and cancer: an epigenetics view". Molecular Aspects of Medicine. 34 (4): 863–74. doi:10.1016/j.mam.2012.06.005. PMC 5791883. PMID 22771542.
- ^ Sampath D, Liu C, Vasan K, Sulda M, Puduvalli VK, Wierda WG, Keating MJ (February 2012). "Histone deacetylases mediate the silencing of miR-15a, miR-16, and miR-29b in chronic lymphocytic leukemia". Blood. 119 (5): 1162–72. doi:10.1182/blood-2011-05-351510. PMC 3277352. PMID 22096249.
- ^ 인간 DNA 복구 유전자, 2014년 4월 15일, 텍사스 대학 MD Anderson Cancer Center
- ^ Krishnan K, Steptoe AL, Martin HC, Wani S, Nones K, Waddell N, Mariasegaram M, Simpson PT, Lakhani SR, Gabrielli B, Vlassov A, Cloonan N, Grimmond SM (February 2013). "MicroRNA-182-5p targets a network of genes involved in DNA repair". RNA. 19 (2): 230–42. doi:10.1261/rna.034926.112. PMC 3543090. PMID 23249749.
- ^ Chaisaingmongkol J, Popanda O, Warta R, Dyckhoff G, Herpel E, Geiselhart L, Claus R, Lasitschka F, Campos B, Oakes CC, Bermejo JL, Herold-Mende C, Plass C, Schmezer P (December 2012). "Epigenetic screen of human DNA repair genes identifies aberrant promoter methylation of NEIL1 in head and neck squamous cell carcinoma". Oncogene. 31 (49): 5108–16. doi:10.1038/onc.2011.660. PMID 22286769.
- ^ Liang L, Deng L, Chen Y, Li GC, Shao C, Tischfield JA (September 2005). "Modulation of DNA end joining by nuclear proteins". The Journal of Biological Chemistry. 280 (36): 31442–9. doi:10.1074/jbc.M503776200. PMID 16012167.
- ^ Singh P, Yang M, Dai H, Yu D, Huang Q, Tan W, Kernstine KH, Lin D, Shen B (November 2008). "Overexpression and hypomethylation of flap endonuclease 1 gene in breast and other cancers". Molecular Cancer Research. 6 (11): 1710–7. doi:10.1158/1541-7786.MCR-08-0269. PMC 2948671. PMID 19010819.
- ^ Lam JS, Seligson DB, Yu H, Li A, Eeva M, Pantuck AJ, Zeng G, Horvath S, Belldegrun AS (August 2006). "Flap endonuclease 1 is overexpressed in prostate cancer and is associated with a high Gleason score". BJU International. 98 (2): 445–51. doi:10.1111/j.1464-410X.2006.06224.x. PMID 16879693. S2CID 22165252.
- ^ Kim JM, Sohn HY, Yoon SY, Oh JH, Yang JO, Kim JH, Song KS, Rho SM, Yoo HS, Yoo HS, Kim YS, Kim JG, Kim NS (January 2005). "Identification of gastric cancer-related genes using a cDNA microarray containing novel expressed sequence tags expressed in gastric cancer cells". Clinical Cancer Research. 11 (2 Pt 1): 473–82. doi:10.1158/1078-0432.473.11.2. PMID 15701830.
- ^ Wang K, Xie C, Chen D (May 2014). "Flap endonuclease 1 is a promising candidate biomarker in gastric cancer and is involved in cell proliferation and apoptosis". International Journal of Molecular Medicine. 33 (5): 1268–74. doi:10.3892/ijmm.2014.1682. PMID 24590400.
- ^ Krause A, Combaret V, Iacono I, Lacroix B, Compagnon C, Bergeron C, Valsesia-Wittmann S, Leissner P, Mougin B, Puisieux A (July 2005). "Genome-wide analysis of gene expression in neuroblastomas detected by mass screening" (PDF). Cancer Letters. 225 (1): 111–20. doi:10.1016/j.canlet.2004.10.035. PMID 15922863.
- ^ Iacobuzio-Donahue CA, Maitra A, Olsen M, Lowe AW, van Heek NT, Rosty C, Walter K, Sato N, Parker A, Ashfaq R, Jaffee E, Ryu B, Jones J, Eshleman JR, Yeo CJ, Cameron JL, Kern SE, Hruban RH, Brown PO, Goggins M (April 2003). "Exploration of global gene expression patterns in pancreatic adenocarcinoma using cDNA microarrays". The American Journal of Pathology. 162 (4): 1151–62. doi:10.1016/S0002-9440(10)63911-9. PMC 1851213. PMID 12651607.
- ^ Sato M, Girard L, Sekine I, Sunaga N, Ramirez RD, Kamibayashi C, Minna JD (October 2003). "Increased expression and no mutation of the Flap endonuclease (FEN1) gene in human lung cancer". Oncogene. 22 (46): 7243–6. doi:10.1038/sj.onc.1206977. PMID 14562054.
- ^ Bi FF, Li D, Yang Q (2013). "Hypomethylation of ETS transcription factor binding sites and upregulation of PARP1 expression in endometrial cancer". BioMed Research International. 2013: 946268. doi:10.1155/2013/946268. PMC 3666359. PMID 23762867.
- ^ Li D, Bi FF, Cao JM, Cao C, Li CY, Liu B, Yang Q (January 2014). "Poly (ADP-ribose) polymerase 1 transcriptional regulation: a novel crosstalk between histone modification H3K9ac and ETS1 motif hypomethylation in BRCA1-mutated ovarian cancer". Oncotarget. 5 (1): 291–7. doi:10.18632/oncotarget.1549. PMC 3960209. PMID 24448423.
- ^ Bi FF, Li D, Yang Q (February 2013). "Promoter hypomethylation, especially around the E26 transformation-specific motif, and increased expression of poly (ADP-ribose) polymerase 1 in BRCA-mutated serous ovarian cancer". BMC Cancer. 13: 90. doi:10.1186/1471-2407-13-90. PMC 3599366. PMID 23442605.
- ^ Narayanan L, Fritzell JA, Baker SM, Liskay RM, Glazer PM (April 1997). "Elevated levels of mutation in multiple tissues of mice deficient in the DNA mismatch repair gene Pms2". Proceedings of the National Academy of Sciences of the United States of America. 94 (7): 3122–7. Bibcode:1997PNAS...94.3122N. doi:10.1073/pnas.94.7.3122. JSTOR 41786. PMC 20332. PMID 9096356.
- ^ Hegan DC, Narayanan L, Jirik FR, Edelmann W, Liskay RM, Glazer PM (December 2006). "Differing patterns of genetic instability in mice deficient in the mismatch repair genes Pms2, Mlh1, Msh2, Msh3 and Msh6". Carcinogenesis. 27 (12): 2402–8. doi:10.1093/carcin/bgl079. PMC 2612936. PMID 16728433.
- ^ Tutt AN, van Oostrom CT, Ross GM, van Steeg H, Ashworth A (March 2002). "Disruption of Brca2 increases the spontaneous mutation rate in vivo: synergism with ionizing radiation". EMBO Reports. 3 (3): 255–60. doi:10.1093/embo-reports/kvf037. PMC 1084010. PMID 11850397.
- ^ Halford S, Rowan A, Sawyer E, Talbot I, Tomlinson I (June 2005). "O(6)-methylguanine methyltransferase in colorectal cancers: detection of mutations, loss of expression, and weak association with G:C>A:T transitions". Gut. 54 (6): 797–802. doi:10.1136/gut.2004.059535. PMC 1774551. PMID 15888787.
- ^ Shen L, Kondo Y, Rosner GL, Xiao L, Hernandez NS, Vilaythong J, Houlihan PS, Krouse RS, Prasad AR, Einspahr JG, Buckmeier J, Alberts DS, Hamilton SR, Issa JP (September 2005). "MGMT promoter methylation and field defect in sporadic colorectal cancer". Journal of the National Cancer Institute. 97 (18): 1330–8. doi:10.1093/jnci/dji275. PMID 16174854.
- ^ a b Lee KH, Lee JS, Nam JH, Choi C, Lee MC, Park CS, Juhng SW, Lee JH (October 2011). "Promoter methylation status of hMLH1, hMSH2, and MGMT genes in colorectal cancer associated with adenoma-carcinoma sequence". Langenbeck's Archives of Surgery. 396 (7): 1017–26. doi:10.1007/s00423-011-0812-9. PMID 21706233. S2CID 8069716.
- ^ Svrcek M, Buhard O, Colas C, Coulet F, Dumont S, Massaoudi I, Lamri A, Hamelin R, Cosnes J, Oliveira C, Seruca R, Gaub MP, Legrain M, Collura A, Lascols O, Tiret E, Fléjou JF, Duval A (November 2010). "Methylation tolerance due to an O6-methylguanine DNA methyltransferase (MGMT) field defect in the colonic mucosa: an initiating step in the development of mismatch repair-deficient colorectal cancers". Gut. 59 (11): 1516–26. doi:10.1136/gut.2009.194787. PMID 20947886. S2CID 206950452.
- ^ Paluszczak J, Misiak P, Wierzbicka M, Woźniak A, Baer-Dubowska W (February 2011). "Frequent hypermethylation of DAPK, RARbeta, MGMT, RASSF1A and FHIT in laryngeal squamous cell carcinomas and adjacent normal mucosa". Oral Oncology. 47 (2): 104–7. doi:10.1016/j.oraloncology.2010.11.006. PMID 21147548.
- ^ Zuo C, Zhang H, Spencer HJ, Vural E, Suen JY, Schichman SA, Smoller BR, Kokoska MS, Fan CY (October 2009). "Increased microsatellite instability and epigenetic inactivation of the hMLH1 gene in head and neck squamous cell carcinoma". Otolaryngology–Head and Neck Surgery. 141 (4): 484–90. doi:10.1016/j.otohns.2009.07.007. PMID 19786217. S2CID 8357370.
- ^ Tawfik HM, El-Maqsoud NM, Hak BH, El-Sherbiny YM (2011). "Head and neck squamous cell carcinoma: mismatch repair immunohistochemistry and promoter hypermethylation of hMLH1 gene". American Journal of Otolaryngology. 32 (6): 528–36. doi:10.1016/j.amjoto.2010.11.005. PMID 21353335.
- ^ Zou XP, Zhang B, Zhang XQ, Chen M, Cao J, Liu WJ (November 2009). "Promoter hypermethylation of multiple genes in early gastric adenocarcinoma and precancerous lesions". Human Pathology. 40 (11): 1534–42. doi:10.1016/j.humpath.2009.01.029. PMID 19695681.
- ^ Wani M, Afroze D, Makhdoomi M, Hamid I, Wani B, Bhat G, Wani R, Wani K (2012). "Promoter methylation status of DNA repair gene (hMLH1) in gastric carcinoma patients of the Kashmir valley". Asian Pacific Journal of Cancer Prevention. 13 (8): 4177–81. doi:10.7314/APJCP.2012.13.8.4177. PMID 23098428.
- ^ a b Raza Y, Ahmed A, Khan A, Chishti AA, Akhter SS, Mubarak M, Bernstein C, Zaitlin B, Kazmi SU (May 2020). "Helicobacter pylori severely reduces expression of DNA repair proteins PMS2 and ERCC1 in gastritis and gastric cancer". DNA Repair (Amst). 89: 102836. doi:10.1016/j.dnarep.2020.102836. PMID 32143126. S2CID 212622031.
- ^ Agarwal A, Polineni R, Hussein Z, Vigoda I, Bhagat TD, Bhattacharyya S, Maitra A, Verma A (2012). "Role of epigenetic alterations in the pathogenesis of Barrett's esophagus and esophageal adenocarcinoma". International Journal of Clinical and Experimental Pathology. 5 (5): 382–96. PMC 3396065. PMID 22808291.
- ^ Tuna M, Amos CI (November 2013). "Genomic sequencing in cancer". Cancer Letters. 340 (2): 161–70. doi:10.1016/j.canlet.2012.11.004. PMC 3622788. PMID 23178448.
- ^ Roach JC, Glusman G, Smit AF, Huff CD, Hubley R, Shannon PT, Rowen L, Pant KP, Goodman N, Bamshad M, Shendure J, Drmanac R, Jorde LB, Hood L, Galas DJ (April 2010). "Analysis of genetic inheritance in a family quartet by whole-genome sequencing". Science. 328 (5978): 636–9. Bibcode:2010Sci...328..636R. doi:10.1126/science.1186802. PMC 3037280. PMID 20220176.
- ^ Campbell CD, Chong JX, Malig M, Ko A, Dumont BL, Han L, Vives L, O'Roak BJ, Sudmant PH, Shendure J, Abney M, Ober C, Eichler EE (November 2012). "Estimating the human mutation rate using autozygosity in a founder population". Nature Genetics. 44 (11): 1277–81. doi:10.1038/ng.2418. PMC 3483378. PMID 23001126.
- ^ Keightley PD (February 2012). "Rates and fitness consequences of new mutations in humans". Genetics. 190 (2): 295–304. doi:10.1534/genetics.111.134668. PMC 3276617. PMID 22345605.
- ^ Ye K, Beekman M, Lameijer EW, Zhang Y, Moed MH, van den Akker EB, Deelen J, Houwing-Duistermaat JJ, Kremer D, Anvar SY, Laros JF, Jones D, Raine K, Blackburne B, Potluri S, Long Q, Guryev V, van der Breggen R, Westendorp RG, 't Hoen PA, den Dunnen J, van Ommen GJ, Willemsen G, Pitts SJ, Cox DR, Ning Z, Boomsma DI, Slagboom PE (December 2013). "Aging as accelerated accumulation of somatic variants: whole-genome sequencing of centenarian and middle-aged monozygotic twin pairs" (PDF). Twin Research and Human Genetics. 16 (6): 1026–32. doi:10.1017/thg.2013.73. PMID 24182360.
- ^ Shanbhag NM, Rafalska-Metcalf IU, Balane-Bolivar C, Janicki SM, Greenberg RA (June 2010). "ATM-dependent chromatin changes silence transcription in cis to DNA double-strand breaks". Cell. 141 (6): 970–81. doi:10.1016/j.cell.2010.04.038. PMC 2920610. PMID 20550933.
- ^ Morano A, Angrisano T, Russo G, Landi R, Pezone A, Bartollino S, Zuchegna C, Babbio F, Bonapace IM, Allen B, Muller MT, Chiariotti L, Gottesman ME, Porcellini A, Avvedimento EV (January 2014). "Targeted DNA methylation by homology-directed repair in mammalian cells. Transcription reshapes methylation on the repaired gene". Nucleic Acids Research. 42 (2): 804–21. doi:10.1093/nar/gkt920. PMC 3902918. PMID 24137009.
- ^ Fernandez AF, Assenov Y, Martin-Subero JI, Balint B, Siebert R, Taniguchi H, Yamamoto H, Hidalgo M, Tan AC, Galm O, Ferrer I, Sanchez-Cespedes M, Villanueva A, Carmona J, Sanchez-Mut JV, Berdasco M, Moreno V, Capella G, Monk D, Ballestar E, Ropero S, Martinez R, Sanchez-Carbayo M, Prosper F, Agirre X, Fraga MF, Graña O, Perez-Jurado L, Mora J, Puig S, Prat J, Badimon L, Puca AA, Meltzer SJ, Lengauer T, Bridgewater J, Bock C, Esteller M (February 2012). "A DNA methylation fingerprint of 1628 human samples". Genome Research. 22 (2): 407–19. doi:10.1101/gr.119867.110. PMC 3266047. PMID 21613409.
- ^ Bishop JB, Witt KL, Sloane RA (December 1997). "Genetic toxicities of human teratogens". Mutation Research. 396 (1–2): 9–43. doi:10.1016/S0027-5107(97)00173-5. PMID 9434858.
- ^ Gurvich N, Berman MG, Wittner BS, Gentleman RC, Klein PS, Green JB (July 2005). "Association of valproate-induced teratogenesis with histone deacetylase inhibition in vivo". FASEB Journal. 19 (9): 1166–8. doi:10.1096/fj.04-3425fje. PMID 15901671. S2CID 25874971.
- ^ Smithells D (November 1998). "Does thalidomide cause second generation birth defects?". Drug Safety. 19 (5): 339–41. doi:10.2165/00002018-199819050-00001. PMID 9825947. S2CID 9014237.
- ^ Friedler G (December 1996). "Paternal exposures: impact on reproductive and developmental outcome. An overview". Pharmacology Biochemistry and Behavior. 55 (4): 691–700. doi:10.1016/S0091-3057(96)00286-9. PMID 8981601. S2CID 2260876.
- ^ WebCite 쿼리 결과
- ^ Cicero TJ, Adams ML, Giordano A, Miller BT, O'Connor L, Nock B (March 1991). "Influence of morphine exposure during adolescence on the sexual maturation of male rats and the development of their offspring". The Journal of Pharmacology and Experimental Therapeutics. 256 (3): 1086–93. PMID 2005573.
- ^ Newbold RR, Padilla-Banks E, Jefferson WN (June 2006). "Adverse effects of the model environmental estrogen diethylstilbestrol are transmitted to subsequent generations". Endocrinology. 147 (6 Suppl): S11-7. doi:10.1210/en.2005-1164. PMID 16690809.
- ^ a b Katiyar, Santosh K.; Singh, Tripti; Prasad, Ram; Sun, Qian; Vaid, Mudit (September 2012). "Epigenetic Alterations in Ultraviolet Radiation-Induced Skin Carcinogenesis: Interaction of Bioactive Dietary Components on Epigenetic Targets†". Photochemistry and Photobiology. 88 (5): 1066–1074. doi:10.1111/j.1751-1097.2011.01020.x. PMC 3288155. PMID 22017262.
- ^ Orouji E, Utikal J (2018). "Tackling malignant melanoma epigenetically: histone lysine methylation". Clinical Epigenetics. 10 (1): 145. doi:10.1186/s13148-018-0583-z. PMC 6249913. PMID 30466474.
- ^ a b Collins CC, Volik SV, Lapuk AV, Wang Y, Gout PW, Wu C, Xue H, Cheng H, Haegert A, Bell RH, Brahmbhatt S, Anderson S, Fazli L, Hurtado-Coll A, Rubin MA, Demichelis F, Beltran H, Hirst M, Marra M, Maher CA, Chinnaiyan AM, Gleave M, Bertino JR, Lubin M, Wang Y (March 2012). "Next generation sequencing of prostate cancer from a patient identifies a deficiency of methylthioadenosine phosphorylase, an exploitable tumor target". Molecular Cancer Therapeutics. 11 (3): 775–83. doi:10.1158/1535-7163.MCT-11-0826. PMC 3691697. PMID 22252602.
- ^ a b Li LC, Carroll PR, Dahiya R (January 2005). "Epigenetic changes in prostate cancer: implication for diagnosis and treatment". Journal of the National Cancer Institute. 97 (2): 103–15. doi:10.1093/jnci/dji010. PMID 15657340.
- ^ a b Gurel B, Iwata T, Koh CM, Yegnasubramanian S, Nelson WG, De Marzo AM (November 2008). "Molecular alterations in prostate cancer as diagnostic, prognostic, and therapeutic targets". Advances in Anatomic Pathology. 15 (6): 319–31. doi:10.1097/PAP.0b013e31818a5c19. PMC 3214657. PMID 18948763.
- ^ Ornish D, Magbanua MJ, Weidner G, Weinberg V, Kemp C, Green C, Mattie MD, Marlin R, Simko J, Shinohara K, Haqq CM, Carroll PR (June 2008). "Changes in prostate gene expression in men undergoing an intensive nutrition and lifestyle intervention". Proceedings of the National Academy of Sciences of the United States of America. 105 (24): 8369–74. Bibcode:2008PNAS..105.8369O. doi:10.1073/pnas.0803080105. PMC 2430265. PMID 18559852.
- ^ a b c d e f g h Sun C, Reimers LL, Burk RD (April 2011). "Methylation of HPV16 genome CpG sites is associated with cervix precancer and cancer". Gynecologic Oncology. 121 (1): 59–63. doi:10.1016/j.ygyno.2011.01.013. PMC 3062667. PMID 21306759.
- ^ Mandal SS (April 2010). "Mixed lineage leukemia: versatile player in epigenetics and human disease". The FEBS Journal. 277 (8): 1789. doi:10.1111/j.1742-4658.2010.07605.x. PMID 20236314. S2CID 37705117.
- ^ Nebbioso, Angela; Tambaro, Francesco Paolo; Dell'Aversana, Carmela; Altucci, Lucia (2018-06-07). Greally, John M. (ed.). "Cancer epigenetics: Moving forward". PLOS Genetics. 14 (6): e1007362. doi:10.1371/journal.pgen.1007362. ISSN 1553-7404. PMC 5991666. PMID 29879107.
- ^ Butcher, James (March 2001). "Electromagnetic fields may cause leukaemia in children". The Lancet. 357 (9258): 777. doi:10.1016/S0140-6736(05)71207-1. S2CID 54400632.
- ^ "Soft Tissue Sarcoma". January 1980.
- ^ Bennani-Baiti IM (December 2011). "Epigenetic and epigenomic mechanisms shape sarcoma and other mesenchymal tumor pathogenesis". Epigenomics. 3 (6): 715–32. doi:10.2217/epi.11.93. PMID 22126291.
- ^ Richter GH, Plehm S, Fasan A, Rössler S, Unland R, Bennani-Baiti IM, Hotfilder M, Löwel D, von Luettichau I, Mossbrugger I, Quintanilla-Martinez L, Kovar H, Staege MS, Müller-Tidow C, Burdach S (March 2009). "EZH2 is a mediator of EWS/FLI1 driven tumor growth and metastasis blocking endothelial and neuro-ectodermal differentiation". Proceedings of the National Academy of Sciences of the United States of America. 106 (13): 5324–9. Bibcode:2009PNAS..106.5324R. doi:10.1073/pnas.0810759106. PMC 2656557. PMID 19289832.
- ^ Bennani-Baiti IM, Machado I, Llombart-Bosch A, Kovar H (August 2012). "Lysine-specific demethylase 1 (LSD1/KDM1A/AOF2/BHC110) is expressed and is an epigenetic drug target in chondrosarcoma, Ewing's sarcoma, osteosarcoma, and rhabdomyosarcoma". Human Pathology. 43 (8): 1300–7. doi:10.1016/j.humpath.2011.10.010. PMID 22245111.
- ^ Esteller M, Herman JG (January 2004). "Generating mutations but providing chemosensitivity: the role of O6-methylguanine DNA methyltransferase in human cancer". Oncogene. 23 (1): 1–8. doi:10.1038/sj.onc.1207316. PMID 14712205.
- ^ Esteller M, Garcia-Foncillas J, Andion E, Goodman SN, Hidalgo OF, Vanaclocha V, Baylin SB, Herman JG (November 2000). "Inactivation of the DNA-repair gene MGMT and the clinical response of gliomas to alkylating agents". The New England Journal of Medicine. 343 (19): 1350–4. doi:10.1056/NEJM200011093431901. hdl:2445/176306. PMID 11070098.
- ^ Hegi ME, Diserens AC, Gorlia T, Hamou MF, de Tribolet N, Weller M, Kros JM, Hainfellner JA, Mason W, Mariani L, Bromberg JE, Hau P, Mirimanoff RO, Cairncross JG, Janzer RC, Stupp R (March 2005). "MGMT gene silencing and benefit from temozolomide in glioblastoma". The New England Journal of Medicine. 352 (10): 997–1003. doi:10.1056/NEJMoa043331. PMID 15758010.
- ^ Esteller M, Gaidano G, Goodman SN, Zagonel V, Capello D, Botto B, Rossi D, Gloghini A, Vitolo U, Carbone A, Baylin SB, Herman JG (January 2002). "Hypermethylation of the DNA repair gene O(6)-methylguanine DNA methyltransferase and survival of patients with diffuse large B-cell lymphoma". Journal of the National Cancer Institute. 94 (1): 26–32. doi:10.1093/jnci/94.1.26. PMID 11773279.
- ^ Glasspool RM, Teodoridis JM, Brown R (April 2006). "Epigenetics as a mechanism driving polygenic clinical drug resistance". British Journal of Cancer. 94 (8): 1087–92. doi:10.1038/sj.bjc.6603024. PMC 2361257. PMID 16495912.
- ^ Brock MV, Hooker CM, Ota-Machida E, Han Y, Guo M, Ames S, Glöckner S, Piantadosi S, Gabrielson E, Pridham G, Pelosky K, Belinsky SA, Yang SC, Baylin SB, Herman JG (March 2008). "DNA methylation markers and early recurrence in stage I lung cancer". The New England Journal of Medicine. 358 (11): 1118–28. doi:10.1056/NEJMoa0706550. PMID 18337602. S2CID 18279123.
- ^ a b Iglesias-Linares A, Yañez-Vico RM, González-Moles MA (May 2010). "Potential role of HDAC inhibitors in cancer therapy: insights into oral squamous cell carcinoma". Oral Oncology. 46 (5): 323–9. doi:10.1016/j.oraloncology.2010.01.009. PMID 20207580.
- ^ Wang LG, Chiao JW (September 2010). "Prostate cancer chemopreventive activity of phenethyl isothiocyanate through epigenetic regulation (review)". International Journal of Oncology. 37 (3): 533–9. doi:10.3892/ijo_00000702. PMID 20664922.
- ^ Gherardini L, Sharma A, Capobianco E, Cinti C (2016-05-27). "Targeting Cancer with Epi-Drugs: A Precision Medicine Perspective". Current Pharmaceutical Biotechnology. 17 (10): 856–65. doi:10.2174/1381612822666160527154757. PMID 27229488.
- ^ Spannhoff A, Sippl W, Jung M (January 2009). "Cancer treatment of the future: inhibitors of histone methyltransferases". The International Journal of Biochemistry & Cell Biology. 41 (1): 4–11. doi:10.1016/j.biocel.2008.07.024. PMID 18773966.
- ^ Garcia-Manero G, Stoltz ML, Ward MR, Kantarjian H, Sharma S (September 2008). "A pilot pharmacokinetic study of oral azacitidine". Leukemia. 22 (9): 1680–4. doi:10.1038/leu.2008.145. PMID 18548103.
- ^ Garcia-Manero G (November 2008). "Demethylating agents in myeloid malignancies". Current Opinion in Oncology. 20 (6): 705–10. doi:10.1097/CCO.0b013e328313699c. PMC 3873866. PMID 18841054.
- ^ Aribi A, Borthakur G, Ravandi F, Shan J, Davisson J, Cortes J, Kantarjian H (February 2007). "Activity of decitabine, a hypomethylating agent, in chronic myelomonocytic leukemia". Cancer. 109 (4): 713–7. doi:10.1002/cncr.22457. PMID 17219444.
- ^ De Padua Silva L, de Lima M, Kantarjian H, Faderl S, Kebriaei P, Giralt S, Davisson J, Garcia-Manero G, Champlin R, Issa JP, Ravandi F (June 2009). "Feasibility of allo-SCT after hypomethylating therapy with decitabine for myelodysplastic syndrome". Bone Marrow Transplantation. 43 (11): 839–43. doi:10.1038/bmt.2008.400. PMID 19151791.
- ^ Hambach L, Ling KW, Pool J, Aghai Z, Blokland E, Tanke HJ, Bruijn JA, Halfwerk H, van Boven H, Wieles B, Goulmy E (March 2009). "Hypomethylating drugs convert HA-1-negative solid tumors into targets for stem cell-based immunotherapy". Blood. 113 (12): 2715–22. doi:10.1182/blood-2008-05-158956. PMID 19096014.
- ^ Fenaux P, Mufti GJ, Hellstrom-Lindberg E, Santini V, Finelli C, Giagounidis A, Schoch R, Gattermann N, Sanz G, List A, Gore SD, Seymour JF, Bennett JM, Byrd J, Backstrom J, Zimmerman L, McKenzie D, Beach C, Silverman LR (March 2009). "Efficacy of azacitidine compared with that of conventional care regimens in the treatment of higher-risk myelodysplastic syndromes: a randomised, open-label, phase III study". The Lancet. Oncology. 10 (3): 223–32. doi:10.1016/S1470-2045(09)70003-8. PMC 4086808. PMID 19230772.
- ^ Duvic M, Talpur R, Ni X, Zhang C, Hazarika P, Kelly C, Chiao JH, Reilly JF, Ricker JL, Richon VM, Frankel SR (January 2007). "Phase 2 trial of oral vorinostat (suberoylanilide hydroxamic acid, SAHA) for refractory cutaneous T-cell lymphoma (CTCL)". Blood. 109 (1): 31–9. doi:10.1182/blood-2006-06-025999. PMC 1785068. PMID 16960145.
- ^ Olsen EA, Kim YH, Kuzel TM, Pacheco TR, Foss FM, Parker S, Frankel SR, Chen C, Ricker JL, Arduino JM, Duvic M (July 2007). "Phase IIb multicenter trial of vorinostat in patients with persistent, progressive, or treatment refractory cutaneous T-cell lymphoma". Journal of Clinical Oncology. 25 (21): 3109–15. doi:10.1200/JCO.2006.10.2434. PMID 17577020. S2CID 19558322.
- ^ Cameron EE, Bachman KE, Myöhänen S, Herman JG, Baylin SB (January 1999). "Synergy of demethylation and histone deacetylase inhibition in the re-expression of genes silenced in cancer". Nature Genetics. 21 (1): 103–7. doi:10.1038/5047. PMID 9916800. S2CID 25070861.
- ^ http://www.accessdata.fda.gov/drugsatfda_docs/nda/2015/205353Orig1s000MedR.pdf[베어 URL PDF]
- ^ Dowden J, Hong W, Parry RV, Pike RA, Ward SG (April 2010). "Toward the development of potent and selective bisubstrate inhibitors of protein arginine methyltransferases". Bioorganic & Medicinal Chemistry Letters. 20 (7): 2103–5. doi:10.1016/j.bmcl.2010.02.069. PMID 20219369.
- ^ Galvez AF, Chen N, Macasieb J, de Lumen BO (October 15, 2001). "Chemopreventive Property of a Soybean Peptide (Lunasin) That Binds to Deacetylated Histones and Inhibits Acetylation". Cancer Research. 61.