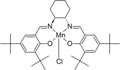C-대칭2 리간드
C2-Symmetric ligands동질 촉매에서 C대칭2 리간드는 거울 대칭은 부족하지만2 C 대칭(이중 회전 대칭)이 있는 리간드를 가리킨다.그러한 리간드는 보통 광합성이며 카탈루냐에 가치가 있다.[1]리간드의 C2 대칭은 가능한 반응 경로의 수를 제한하며, 따라서 비대칭 유사성에 비례하여 항항우울성을 증가시킨다.C-대칭2 리간드는 치랄 리간드의 서브셋이다.C-대칭2 리간드를 포함한 치랄 리간드는 금속이나 다른 그룹과 결합하여 치랄 촉매를 형성한다.이 촉매들은 항저항 화학 합성에 관여하는데, 촉매 내의 치례성이 반응 제품에서 치례성을 산출한다.null
예
초기 C-대칭2 리간드, 디프인산 촉매 리간드 DIPAMP는 2001년 노벨 화학상을 공동 수상한 윌리엄 S. Knowles와 몬산토 컴퍼니의 동료들에 의해 1968년에 개발되었다.[2]이 리간드는 L-DOPA의 산업 생산에 사용되었다.null
C-대칭2 리간드의 일부 계급을 특권 리간드라고 하는데, 이는 단일 반응형만이 아니라 다중 촉매 작용에 광범위하게 적용되는 리간드다.[3][4]null
- 리간즈 앤 콤플렉스
C-대칭2 diphosphine DIOP는 역사적으로 중요하다.[5]null
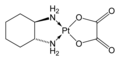
C대칭2(R,R)-다이아미노시클로헥산 리간드를 함유한 옥살리플라틴은 중요한 항암제다.null
제이콥센의 에폭시드 촉매제는 C대칭2 살렌형 리간드의 복합체다.null
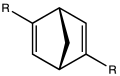
C대칭2 디엔 [7]리간드null
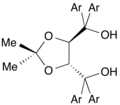
유기합성에 사용되는 bis(oxazoline)와 tridentate bis(oxazoline) 리간드는 모두
BINAP의 두 가지 반물질
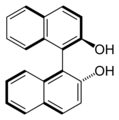
비놀, 또 다른 비나프탈렌 기반 리간드
DIPAMP, 역사적으로 중요한 diphosphine.
샤를리스 비대칭 다이히드록실화에 사용되는 AD-믹스 α, 디히드로퀴닌 유도체
기계론적 개념
비대칭 유도를 위해 고안된 리간드 내의 대칭 요소의 존재는 직관에 반하는 것처럼 보일 수 있지만, 비대칭 유도는 리간드가 치랄(즉, 부적절한 회전 축이 없는 경우)만 요구한다.비대칭(즉, 대칭 원소의 부재)은 필요하지 않다.C2 대칭은 전환 상태에서 고유한 기하학적 수를 줄임으로써 복합체의 항저항성을 향상시킨다.강직과 운동적 요인은 보통 단일 제품의 형성을 선호한다.[1][8]null
치랄 울타리
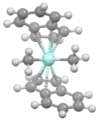
치랄 리간드는 반응 좌표를 따라 어딘가에서 비대칭 유도에 의해 작용한다.오른쪽의 이미지는 키랄 리간드가 어떻게 항우울제 반응을 유발할 수 있는지를 보여준다.리간드(녹색)는 질소, 산소 또는 인 원자가 중앙 금속 원자(빨간색)를 껴안고 있는2 C 대칭이다.이 특별한 리간드에서는 오른쪽이 튀어나와 있고 왼쪽이 방향을 가리키고 있다.이 감소의 기질은 아세토페논과 시약(파란색)이온이다.금속과 리간드가 없는 경우, 하이드라이드 이온의 Re face 접근은 (S)-enantiomer를 주고 Si face는 (R)-enantiomer에 동일한 양으로 접근한다(예상과 같은 레이스 혼합물).리간드와 금속의 존재는 모든 것을 변화시킨다.카보닐 그룹은 금속과 조정되며, 페닐 그룹의 강체 덩어리 때문에 이상적인 상황에서 (R) 엔안티머의 배타적 형성을 가진 하이드라이드 이온에 노출되는 Si 면에서만 그렇게 할 수 있다.재면은 단순히 치랄 울타리에 부딪힐 것이다.[9]리간드가 거울 이미지로 대체될 때 다른 에반토머가 형성되고 리간드의 레이스믹 혼합물이 다시 한번 레이스틱 제품을 만들어 낸다는 점에 유의하십시오.또한 두 카보닐 대체물의 견고한 부피가 매우 유사할 경우 전략이 실패한다는 점에 유의하십시오.null
기타 C-대칭2 복합체
많은 C-대칭2 콤플렉스가 알려져 있다.일부는 C-대칭2 리간드에서가 아니라 금속의 조정 영역 내에서 고대칭 리간드의 방향이나 배치에서 발생한다.특히 EDTA와 트리에틸네테트라아민은 리간드가 금속 중심을 감싸는 방식 때문에 C대칭인2 복합체를 형성한다.(인데닐)2에 대해 두 개의 이소머가 가능하다.MX2, C-s 및 C-대칭2.C-대칭2 콤플렉스는 광학적으로 안정적이다.null
비대칭 리간즈
일반적으로 C-대칭이2 없는 비대칭 탄소와 같은 원자 치랄성 중심을 포함하는 리간드는 촉매에서 중요한 것으로 남아 있다.예를 들면 신코나 알칼로이드와 특정 인광산염 등이 있다.P-chiral monophosphines도 조사되었다.null
참고 항목
추가 읽기
- Desimoni, G.; Faita, G.; Jorgensen, K. A. (2006). "C2-Symmetric Chiral Bis(Oxazoline) Ligands in Asymmetric Catalysis". Chem. Rev. 106 (9): 3561–3651. doi:10.1021/cr0505324. PMID 16967916.
- Liu, X.; Lin, L.; Feng, X. (2011). "Chiral N,N'-Dioxides: New Ligands and Organocatalysts for Catalytic Asymmetric Reactions". Acc. Chem. Res. 44pages=574-587 (8): 574–87. doi:10.1021/ar200015s. PMID 21702458.
- Evans, D. A.; Kozlowski, M. C.; Murry, J. A.; Burgey, C. S.; Campos, K. R.; Connell, B. T.; Staples, R. J. (1999). "C2-Symmetric Copper(II) Complexes as Chiral Lewis Acids. Scope and Mechanism of Catalytic Enantioselective Aldol Additions of Enolsilanes to (Benzyloxy)Acetaldehyde". J. Am. Chem. Soc. 121, 669–685 (4): 669–685. doi:10.1021/JA9829822.
- Gao, J.-X.; Ikariya, T.; Noyori, R. (1996). "A Ruthenium(II) Complex with a C2-Symmetric Diphosphine/Diamine Tetradentate Ligand for Asymmetric Transfer Hydrogenation of Aromatic Ketones". Organometallics. 15: 1087–1089. doi:10.1021/OM950833B.
- Pye, P. J.; Rossen, K.; Reamer, R. A.; Tsou, N. N.; Volante, R. P.; Reider, P. J. (1997). "New Planar Chiral Bisphosphine Ligand for Asymmetric Catalysis: Highly Enantioselective Hydrogenations under Mild Conditions". J. Am. Chem. Soc. 119 (26): 6207–6208. doi:10.1021/JA970654G.
참조
- ^ a b James K. Whitesell (1989). "C2 Symmetry and Symmetric Induction". Chem. Rev. 89 (7): 1581–1590. doi:10.1021/cr00097a012.
- ^ 2001년 노벨상 www.nobelprize.org 링크 웨이백 머신에 2007-07-13
- ^ Pfaltz, A. (2004). "Asymmetric Catalysis Special Feature Part II: Design of chiral ligands for asymmetric catalysis: From C2-symmetric P,P- and N,N-ligands to sterically and electronically nonsymmetrical P,N-ligands". Proceedings of the National Academy of Sciences. 101 (16): 5723–5726. doi:10.1073/pnas.0307152101. PMC 395974. PMID 15069193.
- ^ Yoon, TP; Jacobsen, EN (March 2003). "Privileged chiral catalysts". Science. 299 (5613): 1691–3. doi:10.1126/science.1083622. PMID 12637734. S2CID 27416160.
- ^ Dang, T. P.; Kagan, H. B. (1971). "The asymmetric synthesis of hydratropic acid and amino-acids by homogeneous catalytic hydrogenation". Journal of the Chemical Society D: Chemical Communications (10): 481. doi:10.1039/C29710000481.
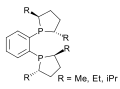
- ^ Burk, M. J.; Feaster, J. E.; Nugent, W. A.; Harlow, R. L. (1993). "Preparation and Use of C2-Symmetric Bis(Phospholanes): Production of a-Amino Acid Derivatives Via Highly Enantioselective Hydrogenation Reactions". J. Am. Chem. Soc. 115: 10125–10138. doi:10.1021/ja00075a031.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Hayashi, T.; Ueyama, K.; Tokunaga, N.; Yoshida, K. (2003). "A Chiral Chelating Diene as a New Type of Chiral Ligand for Transition Metal Catalysts: Its Preparation and Use for the Rhodium-Catalyzed Asymmetric 1,4-Addition". J. Am. Chem. Soc. 125 (38): 11508–11509. doi:10.1021/ja037367z. PMID 13129348.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크) - ^ Rasappan, Ramesh; Laventine, Dominic; Reiser, Oliver (2008). "Metal-bis(oxazoline) complexes: From coordination chemistry to asymmetric catalysis". Coordination Chemistry Reviews. 252 (5–7): 702–714. doi:10.1016/j.ccr.2007.11.007.
- ^ Hisao, Nishiyama (1989). "Chiral and C2-symmetrical bis(oxazolinylpyridine)rhodium(III) complexes: effective catalysts for asymmetric hydrosilylation of ketones". Organometallics. 8 (3): 846–848. doi:10.1021/om00105a047.
- ^ Atwood, J. L.; Hunter, W. E.; Hrncir, D. C.; Samuel, E.; Alt, H.; Rausch, M. D. (1975). "Molecular Structures of the Bis(η5-Indenyl)Dimethyl Derivatives of Titanium, Zirconium, and Hafnium". Inorganic Chemistry. 14 (8): 1757–1762. doi:10.1021/ic50150a003.
{{cite journal}}: CS1 maint: 작성자 매개변수 사용(링크)