S-아데노실메티오닌
S-Adenosyl methionine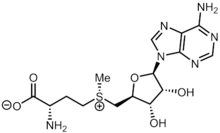 | |||
| | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 (2S)-2-아미노-4-[(S)-{(2S,3S,4R,5R)-5-(4-아미노-9H-푸린-9-일)-3,4-디히드록소란-2-일]}메틸술파늄산염 | |||
| 기타 이름 S-아데노실-L-메티오닌, SAMe, AdoMet, 헤파랍(인도), 아데메티오닌 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 첸블 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.045.391 | ||
| 케그 | |||
| 메쉬 | S-아데노실메티오닌 | ||
PubChem CID | |||
| 유니 | |||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| C15H22N6O5S | |||
| 몰 질량 | 398.44 g/120−1 | ||
| 약리학 | |||
| A16AA02(WHO) | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
S-아데노실 메티오닌(SAMe, SAM-e 또는 AdoMet)은 메틸기 전이, 황화 및 아미노프로필화에 관여하는 일반적인 코기질이다.이러한 동화 반응이 몸 전체에서 일어나지만, 대부분의 SAM은 [1]간에서 생성되고 소비됩니다.핵산, 단백질, 지질 및 2차 대사물과 같은 다양한 기질에 대한 SAM으로부터의 40개 이상의 메틸 전달이 알려져 있다.메티오닌 아데노실전달효소에 의해 아데노신 삼인산(ATP)과 메티오닌으로 만들어진다.SAM은 1952년 [1]Giulio Cantoni에 의해 처음 발견되었다.
박테리아에서 SAM은 메티오닌 또는 시스테인 생합성에 관여하는 유전자를 조절하는 SAM 리보스위치에 의해 결합된다.진핵 세포에서 SAM은 DNA, tRNA 및 rRNA 메틸화, 면역 반응,[2] 아미노산 대사, 황화 등을 포함한 다양한 과정의 조절제 역할을 한다.식물에서 SAM은 중요한 식물 호르몬과 신호 분자인 [3]에틸렌의 생합성에 중요하다.
구조.
S-아데노실메티오닌은 메티오닌의 황에 아데노실카티온으로 구성되어 있다.S-아데노실메티오닌 합성효소에 의해 ATP 및 메티오닌으로부터 다음과 같은 반응을 통해 합성된다.
ATP + L-메티오닌 + HO2 { \ 인산염 + 2인산 + S-아데노실-L-메티오닌
S-아데노실 메티오닌에 존재하는 술포늄 관능기가 특이 반응성의 중심이다.효소에 따라 S-아데노실 메티오닌은 다음 세 가지 제품 중 하나로 전환될 수 있습니다.
- 디옥시아데노신(AdO)으로 변환되는 아데노실라디칼: 고전적인 rSAM 반응, 또한 메티오닌을 공생시킨다.
- 메틸라디칼을 방출하는 S-아데노실 호모시스테인
- 메틸티오아데노신(SMT), 호모알라닌라디칼
생화학
SAM 사이클
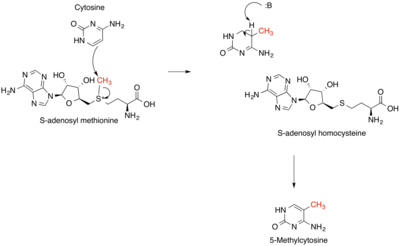
SAM을 생성, 소비 및 재생하는 반응을 SAM 사이클이라고 합니다.이 사이클의 첫 번째 단계에서는 SAM을 기질로 하는 SAM 의존성 메틸화효소(EC 2.1.1)가 생성물로 S-아데노실 호모시스테인을 [4]생성한다.S-아데노실 호모시스테인은 생물학적 다양성에도 불구하고 거의 모든 SAM 의존성 메틸화효소의 강력한 음성 조절제이다.이는 S-아데노실호모시스테인 가수분해효소 EC 3.3.1에 의해 호모시스테인과 아데노신에 가수분해되며, 호모시스테인은 메티오닌 신타아제(코발라민 의존성)의 두 종류 중 하나에 의해 5-메틸기 전달을 통해 메티오닌으로 재생된다.이 메티오닌은 다시 SAM으로 변환되어 [5]사이클을 완료할 수 있습니다.SAM 회로의 속도 제한 공정에서 MTHFR(메틸렌테트라히드로폴레이트 환원효소)은 5,10-메틸렌테트라히드로폴레이트를 [6]5-메틸테트라히드로폴레이트로 불가역적으로 환원한다.
래디칼 SAM 효소
많은 효소들이 SAM을 환원 분해하여 라디칼을 생성한다: 5'-디옥시아데노실 5'-라디칼, 메틸라디칼.이 효소들은 래디칼 SAM이라고 불린다.모두 활성 [7]부위에 철-황 클러스터가 특징입니다.이 기능을 가진 대부분의 효소는 CxxCxxC 또는 근접 변종을 포함하는 배열 상동 영역을 공유합니다.이 배열은 4Fe-4S 클러스터에서 4개의 금속 중 3개에 결합하는 3개의 시스테닐 티올레이트 배위자를 제공합니다.네 번째 Fe는 SAM을 바인드합니다.
이들 효소에 의해 생성된 래디칼 중간체들은 매우 다양한 특이한 화학 반응을 일으킨다.래디칼 SAM 효소의 예로는 포자광생성분해효소, 피루브산포름산분해효소 및 혐기성 술파타아제 활성효소, 리신2,3-아미노무타아제 및 보조인자 생합성, 펩타이드 수식, 금속단백질 클러스터 형성, tRNA 수식, 지질대사 등의 다양한 효소가 있다.일부 래디칼 SAM 효소는 메틸 공여체로 두 번째 SAM을 사용한다.래디칼 SAM 효소는 호기성 유기체보다 혐기성 박테리아에 훨씬 더 풍부하다.그것들은 삶의 모든 영역에서 발견될 수 있고 대부분 미개척이다.최근의 생물정보학 연구는 이 효소군이 65개의 독특한 반응을 포함한 [8]최소 114,000개의 배열을 포함한다고 결론지었다.
폴리아민생합성
SAM의 또 다른 주요 역할은 폴리아민 생합성이다.여기서 SAM은 아데노실메티오닌탈카르복실화효소(EC4.1.1.50)에 의해 탈탄산화되어 S-아데노실메티오닌아민을 형성한다.그런 다음 이 화합물은 n-프로필아민기를 푸트레신으로부터 [9]스펠미딘과 스펠민과 같은 폴리아민의 생합성에 기증한다.
SAM은 세포의 성장과 복구를 위해 필요합니다.그것은 또한 에피네프린과 같이 기분에 영향을 미치는 여러 호르몬과 신경전달물질의 생합성에도 관여합니다.메틸전달효소는 또한 메신저 [10][11]RNA의 5' 캡 옆에 있는 첫 번째 및 두 번째 뉴클레오티드의 2' 히드록실기에 메틸기를 추가하는 역할을 한다.
치료 용도
2012년 현재, SAM이 골관절염의 통증을 완화할 수 있는지에 대한 증거는 명확하지 않았다. 수행된 임상 실험은 일반화하기에는 너무 [12]작았다.
SAM 순환은 1947년부터 간 알코올성 간경변증이 있는 사람들은 그들의 [13]혈액에 많은 양의 메티오닌을 축적할 것이기 때문에 간과 밀접하게 연결되어 있다.세포와 동물 모델에 대한 실험실 테스트의 여러 증거 라인은 SAM이 다양한 간 질환 치료에 유용할 수 있음을 시사하지만, 2012년 현재 SAM은 효과와 [14][15]안전성의 평가를 허용하는 대규모 무작위 위약 대조 임상 시험에서 연구되지 않았다.
우울증.
2016년 코크란 리뷰는 주요 우울증 질환에 대해 "고품질 증거가 없고 그 증거에 기초하여 확실한 결론을 도출할 수 없는 점을 고려할 때 성인의 우울증 치료에 SAMe를 사용하는 것을 [16]더 연구해야 한다"고 결론지었다.
2020년 체계적 검토 결과 위약보다 상당히 잘 수행되었으며 일반적으로 사용되는 다른 항우울제(이미프라민 또는 에스시탈로프람)[17]와 유사한 결과를 보였다.
약동학
경구 SAM은 장용성 코팅 정제(400–1000mg)를 섭취한 후 3~5시간 후에 혈장 농도에 도달한다.반감기는 약 100분입니다.[18]
부작용
SAM [18]섭취 시 위장 장애, 소화불량 및 불안이 발생할 수 있습니다.장기적인 영향은 알려지지 않았다.SAM은 약한 DNA 알킬화제입니다.[19]
SAM의 또 다른 부작용은 불면증이다. 따라서 보충제는 종종 아침에 복용한다.가벼운 부작용에 대한 다른 보고로는 식욕부진, 변비, 메스꺼움, 구강건조, 땀 흘림, 불안/긴장 등이 있지만 위약 대조 연구에서 이러한 부작용은 위약 [medical citation needed]그룹에서 거의 같은 발생률로 발생한다.
SAM은 최근 후생유전학적 조절에서 역할을 하는 것으로 나타났다.DNA 메틸화는 포유동물 세포의 발달과 분화 과정에서 후생유전학적 변형의 핵심 조절제이다.마우스 모델에서, 과도한 수준의 SAM은 당뇨병 신경 장애와 관련된 잘못된 메틸화 패턴과 관련이 있다.SAM은 주요 후생유전자 조절 [20]과정인 시토신 메틸화에서 메틸 공여체 역할을 한다.후생유전자 조절에 대한 이러한 영향 때문에 SAM은 항암 치료제로 테스트되었다.암세포의 증식은 낮은 수준의 DNA 메틸화에 의존한다.시험관내 첨가는 프로모터 배열을 재메틸화하고 프로토온코겐의 [21]생산을 감소시키는 것으로 나타났다.
래디칼 SAM 효소의 결핍은 선천성 심장병, 근위축성 측삭경화증, 바이러스 감수성 [8]증가를 포함한 다양한 질병과 연관되어 왔다.
2022년 연구에서는 SAMe가 독성이 있을 수 있다는 결론을 내렸다.맨체스터 대학의 Jean-Michel Fustin은 연구원들이 SAMe가 체내에서 독성 물질인 아데닌과 메틸티오아데노신으로 분해된다는 것을 발견했다고 말했다.이것은 실험용 쥐에서 발견되었고, 건강에 해를 끼쳤고, 인간 [22][23]세포에 대한 체외 테스트에서 발견되었다.
상호 작용 및 금지 사항
일부 약물과 동시에 SAM을 복용하는 것은 세로토닌 신드롬의 위험을 증가시킬 수 있다. 세로토닌은 너무 많은 세로토닌을 가지고 있기 때문에 잠재적으로 위험한 상태이다.이러한 약물에는 덱스트로메토르판(로비투신), 메페리딘(데메롤), 펜타조신(탈윈), 트라마돌(울트라람)[medical citation needed]이 포함된다.
SAM은 트립토판 및 Hypericum peratum(St.John's wort) 세로토닌 증후군 또는 다른 부작용의 가능성을 증가시키고 파킨슨병에 [24]대한 레보도파의 효과를 감소시킬 수 있다.
조울증이 있는 사람들은 조울증의 [24]위험을 증가시키기 때문에 SAM을 사용하지 말아야 한다.
다른 국가에서의 이용 가능
캐나다,[23] 영국 및 미국에서 SAM은 SAM-e(SAME 또는 SAMe로 표기,[25] "Sammy"로 발음)라는 마케팅 이름으로 식이 보조 식품으로 판매된다.그것은 1994년 [26]건강 및 교육법이 통과된 후 1999년에 미국에서 도입되었다.
1979년 이탈리아, 1985년 스페인,[26] 1989년 독일에서 처방약으로 도입됐다.2012년 현재 러시아, 인도, 중국, 이탈리아, 독일, 베트남,[15] 멕시코에서 처방약으로 판매되고 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b Cantoni, GL (1952). "The Nature of the Active Methyl Donor Formed Enzymatically from L-Methionine and Adenosinetriphosphate". J Am Chem Soc. 74 (11): 2942–3. doi:10.1021/ja01131a519.
- ^ Ding, Wei; Smulan, Lorissa J.; Hou, Nicole S.; Taubert, Stefan; Watts, Jennifer L.; Walker, Amy K. (2015-10-06). "S-Adenosylmethionine Levels Govern Innate Immunity through Distinct Methylation-Dependent Pathways". Cell Metabolism. 22 (4): 633–645. doi:10.1016/j.cmet.2015.07.013. PMC 4598287. PMID 26321661.
- ^ Wang, X.; Oh, M. W.; Komatsu, S. (2016-06-01). "Characterization of S-adenosylmethionine synthetases in soybean under flooding and drought stresses". Biologia Plantarum. 60 (2): 269–278. doi:10.1007/s10535-016-0586-6. ISSN 0006-3134. S2CID 15567646.
- ^ Finkelstein J, Martin J (2000). "Homocysteine". The International Journal of Biochemistry & Cell Biology. 32 (4): 385–9. doi:10.1016/S1357-2725(99)00138-7. PMID 10762063.
- ^ Födinger M, Hörl W, Sunder-Plassmann G (Jan–Feb 2000). "Molecular biology of 5,10-methylenetetrahydrofolate reductase". J Nephrol. 13 (1): 20–33. PMID 10720211.
- ^ Goyette, P.; Sumner, J. S.; Milos, R.; Duncan, A. M.; Rosenblatt, D. S.; Matthews, R. G.; Rozen, R. (1994-06-01). "Human methylenetetrahydrofolate reductase: isolation of cDNA, mapping and mutation identification". Nature Genetics. 7 (2): 195–200. doi:10.1038/ng0694-195. ISSN 1061-4036. PMID 7920641. S2CID 23877329.
- ^ Booker, SJ; Grove, TL (2010). "Mechanistic and functional versatility of radical SAM enzymes". F1000 Biology Reports. 2: 52. doi:10.3410/B2-52. PMC 2996862. PMID 21152342.
- ^ a b Landgraf, Bradley J.; McCarthy, Erin L.; Booker, Squire J. (2016-06-13). "Radical S-Adenosylmethionine Enzymes in Human Health and Disease". Annual Review of Biochemistry. 85: 485–514. doi:10.1146/annurev-biochem-060713-035504. PMID 27145839.
- ^ Roje S (2006). "S-Adenosyl-L-methionine: beyond the universal methyl group donor". Phytochemistry. 67 (15): 1686–98. doi:10.1016/j.phytochem.2006.04.019. PMID 16766004.
- ^ Loenen W (2006). "S-Adenosylmethionine: jack of all trades and master of everything?". Biochem Soc Trans. 34 (Pt 2): 330–3. doi:10.1042/BST20060330. PMID 16545107.
- ^ Chiang P, Gordon R, Tal J, Zeng G, Doctor B, Pardhasaradhi K, McCann P (1996). "S-Adenosylmethionine and methylation". FASEB J. 10 (4): 471–80. doi:10.1096/fasebj.10.4.8647346. PMID 8647346. S2CID 11214528.
- ^ Rutjes, AW; Nüesch, E; Reichenbach, S; Jüni, P (7 October 2009). "S-Adenosylmethionine for osteoarthritis of the knee or hip" (PDF). The Cochrane Database of Systematic Reviews (4): CD007321. doi:10.1002/14651858.CD007321.pub2. PMC 7061276. PMID 19821403.
- ^ Mato, Jose M (1997). "S-adenosylmethionine synthesis: Molecular mechanisms and clinical implications". Pharmacology & Therapeutics. 73 (3): 265–280. doi:10.1016/s0163-7258(96)00197-0. hdl:10261/79246. PMID 9175157.
- ^ Anstee, QM; Day, CP (November 2012). "S-Adenosylmethionine (SAMe) therapy in liver disease: a review of current evidence and clinical utility". Journal of Hepatology. 57 (5): 1097–109. doi:10.1016/j.jhep.2012.04.041. PMID 22659519.
- ^ a b Lu, SC; Mato, JM (October 2012). "S-Adenosylmethionine in liver health, injury, and cancer". Physiological Reviews. 92 (4): 1515–42. doi:10.1152/physrev.00047.2011. PMC 3698976. PMID 23073625.
- ^ Galizia, I; Oldani, L; Macritchie, K; Amari, E; Dougall, D; Jones, TN; Lam, RW; Massei, GJ; Yatham, LN; Young, AH (10 October 2016). "S-Adenosyl methionine (SAMe) for depression in adults". The Cochrane Database of Systematic Reviews. 2016 (10): CD011286. doi:10.1002/14651858.CD011286.pub2. PMC 6457972. PMID 27727432.
- ^ Cuomo, Alessandro; Beccarini Crescenzi, Bruno; Bolognesi, Simone; Goracci, Arianna; Koukouna, Despoina; Rossi, Rodolfo; Fagiolini, Andrea (2020-09-05). "S-Adenosylmethionine (SAMe) in major depressive disorder (MDD): a clinician-oriented systematic review". Annals of General Psychiatry. Springer Science and Business Media LLC. 19 (1): 50. doi:10.1186/s12991-020-00298-z. ISSN 1744-859X. PMC 7487540. PMID 32939220.
- ^ a b Najm WI, Reinsch S, Hoehler F, Tobis JS, Harvey PW (February 2004). "S-Adenosyl methionine (SAMe) versus celecoxib for the treatment of osteoarthritis symptoms: A double-blind cross-over trial. ISRCTN36233495". BMC Musculoskelet Disord. 5: 6. doi:10.1186/1471-2474-5-6. PMC 387830. PMID 15102339.
- ^ Rydberg B, Lindahl T (1982). "Nonenzymatic methylation of DNA by the intracellular methyl group donor S-adenosyl-L-methionine is a potentially mutagenic reaction". EMBO J. 1 (2): 211–6. doi:10.1002/j.1460-2075.1982.tb01149.x. PMC 553022. PMID 7188181.
- ^ Varela-Rey, Marta (2014). "S-Adenosylmethionine Levels Regulate the Schwann Cell DNA Methylome". Neuron. 81 (5): 1024–1039. doi:10.1016/j.neuron.2014.01.037. PMC 3960855. PMID 24607226.
- ^ Schmidt, Thomas; Leha, Andreas; Salinas-Riester, Gabriela (2016-12-31). "Treatment of prostate cancer cells with S-adenosylmethionine leads to genome-wide alterations in transcription profiles". Gene. 595 (2): 161–167. doi:10.1016/j.gene.2016.09.032. PMID 27688072.
- ^ Fukumoto, Kazuki; Ito, Kakeru; Saer, Benjamin; Taylor, George; Ye, Shiqi; Yamano, Mayu; Toriba, Yuki; Hayes, Andrew; Okamura, Hitoshi; Fustin, Jean-Michel (5 April 2022). "Excess S-adenosylmethionine inhibits methylation via catabolism to adenine". Communications Biology. Nature Publishing Group. 5 (1). doi:10.1038/s42003-022-03280-5. ISSN 2399-3642. PMID 35383287.
- ^ a b McKie, Robin (10 April 2022). "Biologists warn against toxic SAMe 'health' supplement". The Observer.
- ^ a b "S-Adenosyl-L-Methionine (SAMe): In Depth". National Center for Complementary and Integrative Health (NCCIH). January 11, 2017.
- ^ Woolston, Chris (31 December 2020). "What is SAM-e?". HealthDay.
- ^ a b Bottiglieri, T (November 2002). "S-Adenosyl-L-methionine (SAMe): from the bench to the bedside--molecular basis of a pleiotrophic molecule". The American Journal of Clinical Nutrition. 76 (5): 1151S–1157S. doi:10.1093/ajcn/76.5.1151S. PMID 12418493.
외부 링크
- EINECS 번호 249-946-8
- Shippy, R Andrew; Mendez, Douglas; Jones, Kristina; Cergnul, Irene; Karpiak, Stephen E (2004). "S-Adenosylmethionine (SAM-e) for the treatment of depression in people living with HIV/AIDS". BMC Psychiatry. 4: 38. doi:10.1186/1471-244X-4-38. PMC 535560. PMID 15538952.


