ALOX15
ALOX15
| ALOX15 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 식별자 | |||||||||||||||||||||||||
| 별칭 | ALOX15, 12-LOX, 15-LOX-1, 15LOX-1, 아라키돈산염 15-리포시제네아제, 15-LOX, LOG15 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 152392 MGI: 87997 HomoloGene: 44935 GeneCard: ALOX15 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 직교체 | |||||||||||||||||||||||||
| 종 | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레스 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) | |||||||||||||||||||||||||
| 위치(UCSC) | Cr 17: 4.63 – 4.64Mb | Chr 11: 70.23 – 70.24Mb | |||||||||||||||||||||||
| PubMed 검색 | [3] | [4] | |||||||||||||||||||||||
| 위키다타 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
ALOX15(아라키돈산염 15-리포시겐아제, 15-리포시겐아제-1, 15-LO-1, 15-LOX-1)는 다른 리포시겐아제와 마찬가지로 생리학적으로나 병적으로 중요한 산물에 대한 다불포화지방산의 신진대사에 있어 정합효소다.▼ 유전자 함수
켈라브카르와 바드르(1999)는 ALOX15 유전자 제품이 인플루엔자 예방, 막 리모델링, 암 발생/전이에 관여하고 있다고 밝혔다.켈라브카르와 바드르(1999)는 TP53 유전자의 상실 또는 돌연변이 형태의 발현에 따른 기능상실 활동은 비록 방향적으로 반대되는 매너이긴 하지만 인간과 마우스에서의 ALOX15 촉진 활동을 규제한다는 가설을 뒷받침하는 실험을 설명했다.이 연구들은 ALOX15 유전자 활동과 염색체 가까이에 위치한 확립된 종양 억제 유전자 사이의 직접적인 연관성을 정의했다.켈라브카르와 바드르(1999)는 이를 15리폭시겐아제가 돌연변이 유전자라는 증거로 언급했다.▼ 매핑
펑크 외 연구진(1992)은 인간-햄스터 체성혼합 DNA 패널의 PCR 분석을 통해 인간 17번 염색체에 12리포시제네아제와 15리포시제네아제 유전자가 위치하는 반면, 가장 관련이 없는 리포시제네아제(5리포시제네아제)는 10번 염색체에 매핑된 것으로 나타났다.
켈라브카르와 바드르(1999)는 ALOX15 유전자가 종양 억제 유전자 TP53(191170)에 근접해 17p13.3에 매핑된다고 밝혔다.인간에서는 17p13.3 염색체에 위치한 ALOX15 유전자에 의해 암호화된다.[5]이 11 킬로베이스 쌍 유전자는 아미노산 662개로 구성된 75 킬로달튼 단백질을 위해 14 엑손과 13 인트론 코딩으로 구성되어 있다. 15-LO는 또 다른 인간 15-리포스게나제 효소인 ALOX15B (15-리포스게나제-2라고도 함)와 구별된다.[6]알록스15라고 불리는 ALOX15의 직교체는 동물과 식물 종에 널리 분포하지만 일반적으로 효소 활동이 다르고 알록스15와는 다소 다른 제품을 만든다.
명명법
인간 ALOX15는 처음에 아라키돈산염 15-리포시제네아제 또는 15-리포시제네아제라고 명명되었지만 후속 연구에서는 15-리포시제네아제 활성을 가진 두 번째 인간 효소와 인간 ALOX15의 직교와 밀접하게 관련되어 있는 다양한 비인간 포유류 알록스15 효소가 발견되었다.그럼에도 불구하고 후자의 많은 Alox15 효소들은 15-lipoxygenase 활성보다는 12-lipoxygenase를 주로 또는 독점적으로 가지고 있다.따라서 인간 ALOX15는 현재 아라키돈산염-15-리포시겐아제-1, 15-리포시겐아제-1, 15-LOX-1, 15-LO-1, 인간 12/15-리포시겐아제, 백혈구형 아라키돈산염 12-리포시겐아제나아제, 아라키돈산염 오메가6리포게네아제로 불린다.The second discovered human 15-lipoxygenase, a product of the ALOX15B gene, is termed ALOX15B, arachidonate 15-lipoxygenase 2, 15-lipoxygenase-2, 15-LOX-2, 15-LO-2, arachidonate 15-lipoxygenase type II, arachidonate 15-lipoxygenase, second type, and arachidonate 15-lipoxygenase; and mouse, rat, and rabbit rodent orthologs of human ALOX15, which s인간 효소를 가진 산토끼 74-81% 아미노산 정체성은 일반적으로 알록스15, 12/15-립포시제나 12/15-LOX 또는 12/15-LO)[5][6]라고 불린다.
인간 ALOX15와 ALOX15B 유전자는 모두 17번 염색체에 위치하며, 그들의 제품 단백질은 아미노산 염기서열 정체성이 ~38%에 불과하며, 또한 기판으로서 선호하는 다불포화 지방산이 다르고 동일한 기판에 작용했을 때 다른 제품 프로파일을 나타낸다.[6][7]
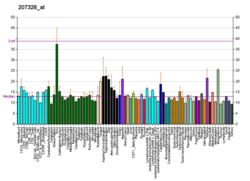
조직 분포
인간 ALOX15 단백질은 순환혈액인 어시노필과 망막세포, 세포, 기관지 기도상피세포, 유방상피세포, 호지킨 림프종의 리드-스테른베르크 세포, 각막상피세포, 둔피세포에서 고도로 발현되며, 치조대 대식세포, 조직마스트세포, 조직섬유세포, 조직섬유세포에서 발현상으로 발현성이 떨어진다.순환하는 혈액 중성미자, 혈관 내피 세포, 관절 세포막 세포, 정액 세포, 전립선 상피 세포, 유방 관상피 세포.[8][9][10][11]
인간 이하의 영장류에서 알록스15의 분포와 특히 설치류의 분포는 인간 ALOX15의 분포와 크게 다르다. 이는 각기 다른 주요 제품 형성(예: 15-HTE가 아닌 12-HETE)과 함께 랫드, 마우스 또는 토끼 모델에서 알록스15 함수의 발견을 랫드, 마우스 또는 토끼 모델에서 알록스15 함수의 추정하기 어렵게 만들었다.인간들.[6]
효소활동
리폭시겐화효소 활성
ALOX15와 Alox15 효소는 비heme, 철분 함유 이산화질소다.그들은 일반적으로 인간 ALOX15의 경우 마지막 PUFA의 메틸 끝에서 거꾸로 계산하거나 오메가(Ω) 탄소를 계산하여 10과 9와 7과 6 사이에 위치한 두 개의 탄소 탄소-탄소 이중 결합을 포함하는 PUFA(Poly 불포화 지방산)에 과산화 잔류물로 분자 산소 O를
2 부착하는 촉매 작용을 한다.ns는 Ω-10 및 Ω-9 및 Ω-7 및 Ω-6이라고도 한다.Ω-13과 Ω-12 카본 사이에 세 번째 탄소-탄소 이중 결합이 없는 PUFA에서 인간 ALOX15는 Ω-6 과산화 중간체를 형성하고, 이 세 번째 이중 결합을 가진 PUFA에서 인간 ALOX15는 Ω-6 과산화 중간을 만들지만 또한 Ω-9 과산화 중간을 만든다.반면에 설치류 알록스15 효소는 거의 독점적으로 Ω-9 과산화 매개체를 생산한다.동시에 ALOX15와 설치류 Alox15 효소는 탄소-탄소 이중 결합을 재조정하여 1S-히드록시-2E,4Z-다이엔 구성으로 가져온다.ALOX15와 Alox15 효소는 S 스테레오아소머 구성에서 수산화 잔류물을 위치시키는 제품을 형성하기 위해 높은 수준의 스테레오스펙티로 작용한다.[12]
리포하이드로페록시디아제 활동
인간 ALOX15는 또한 과산화 PUFA 중간을 3원자 링, 즉 물 분자에 의해 공격되어 에폭시-하이드록시 PUFA 제품을 형성하는 에폭시드 중간을 순환 에테르로 변환할 수 있다.[6]Eoxins는 생체외 인간 혈관 내피 모델 시스템에서 혈관 투과성을 자극한다.[13]
백혈병 싱타아제 활동
ALOX15 - eoxin A4에 의해 만들어진 arachidonic acid의 PUFA 에폭시드는 또한 eoxin C4와 eoxin D4에 추가 대사될 수 있는 eoxin B4를 형성하기 위해 글루타티온과 결합될 수 있다.[6]
기질, 기질 대사물 및 대사물 활동
그들의 생리학적 기질 중에서 인간과 설치류인 AlOX15 효소는 리놀레산, 알파-리놀렌산, 감마-리놀렌산, 아라키돈산, 에이코사펜타에노산, 도코사헥사에노산 등에 작용한다.인간의 효소는 특히 리놀레산에 활발히 작용하여 아라키돈산보다 리놀레산을 선호한다.인용된 지질 내에 에스테르인 PUFA에서는 덜 활동적이다.[6]
아라키돈산
아라키돈산(AA)은 탄소의 5-6, 8-9, 11-12, 14-15 사이에 이중 결합을 가지고 있다. 이러한 이중 결합은 시스에 있다(트랜스 또는 E 구성과는 반대로 시스-트랜스 이소머리즘 또는 Z 참조).ALOX15 adds a hydroperoxy residue to AA at carbons 15 and to a lesser extent 12 to form 15(S)-hydroperoxy-5Z,8Z,11Z,13E-eicosatetraenoic acid (15(S)-HpETE) and 12(S)-hydroperoxy-5Z,8Z,10E,14Z-eicosatetraenoic acid (12(S)-HpETE); the purified enzyme makes 15(S)-HpETE and 12(S)-HpETE in a product ratio of ~4-9 to 1.[14]두 제품 모두 유비쿼터스 셀룰러 글루타티온 과산화효소 효소에 의해 해당 하이드록시 아날로그, 15(S)-HETE(15-Hydroxyeosatetraenoic acid 참조), 12(S)-HETE(12-Hydroxyeosatraeno acid 참조)에 의해 빠르게 감소할 수 있다.15(S)-HpETE 및 15(S)-HETE는 백혈구 B4 수용체 2와 결합하여 활성화하고, 페록시솜 증식기 활성 수용체 감마를 활성화하며, 고농도에서 세포가 유독 활성산소 종을 생성하게 한다. 이러한 효과 중 하나 이상이 최소한 염증 반응을 촉진하고, t를 변화시키는 능력에 부분적으로 책임이 있을 수 있다.he growth of various times of human cancer cell lines, contract various types of blood vessels, and stimulate pathological fibrosis in pulmonary arteries and liver (see 15-Hydroxyicosatetraenoic acid#15(S)-HpETE and 15(S)-HETE). 15(S)-HpETE and 15(S)-HETE are esterified into membrane phospholipids where they may be stored and subsequently released세포 자극 중에이 처리의 한 측면으로서, 두 제품은 적혈구가 성숙하는 동안 미토콘드리아 막인산화질소에 점진적으로 에스테르화되므로(에리트로포이시스 참조) 미토콘드리아의 분해와 이러한 전구체가 생쥐의 적혈구로 성숙하는 신호로 작용할 수 있다.이 경로는 두 개의 다른 미토콘드리아 제거 경로와 함께 작동하므로 생쥐 적혈구 성숙에 필수적인 것으로 보이지 않는다.[6]
15-(S)-HpETE 및 15(S)-HETE는 다음을 포함한 다양한 생체활성 제품에 추가로 대사될 수 있다.
- 리판신(LX)A4, LXB4, AT-LXA4, AT-LXB4, AT-LXB4; 이들 대사물은 동물 모델 및 잠재적으로 인간에서 염증 반응 및 염증 기반 질환의 해결에 기여하는 항염증제 전문 프로레졸링 중재자 등급의 일원이다(전문 프로번들 매개자 및 리판신 참조).
- Hepoxilin isomers (e.g. 1S-hydroxy-14S,15S-epoxy-5Z,8Z,12E-eicosatrienoic acid [14,15-HXA3] and 13R-hydroxy-14S,15S-epoxy-5Z,8Z,11Z-eicosatrienoic acid [14,15-HXB3]) which may contribute to the regulation of inflammation responses and insulin secretion (see hepoxilins).
- 항염증 작용이 있고 심한 천식, 아스피린 유도 천식 발작 및 기타 알레르기 반응에 기여하는 Eoxins(예: eoxin C4, 14,15-eoxin D4, eoxin E4); 호지킨스 질환의 병리학에도 관여할 수 있다(Eoxins 참조).
- 8(S),15(S),15(S)-디히드록시-5Z,9E,llZ,13E-eicosatetraenoic acid (8(S),15(S)-diHETE), 인간 혈소판 집적의 억제제(Dihydroxy-E,Z,E-PUFA 참조).
- 5(S), 15(S), 15(S)-디히드록시-6Z,8E,llE,13Z-eicosatetraenoic acid (5(S),15(S)-diHETE) 및 5-케톤 아날로그 5-oxo-15(S)-히드록시-ETE.이것들은 각각 약하고 강력한 것으로서 인간 어시노필, 중성미자, 모노키테 화학작용을 자극하여 인간의 알레르기 및 비알렉트릭 염증 반응에 기여할 수 있다(5-Hydroxicosatetraenoic acid# 참조).염증 및 5-히드록시코사테트라에노산#알레르기).
- 15- 배양된 인간 탯줄 정맥 내피 세포와 다양한 인간 암 세포 라인의 성장을 억제하는 Oxo-ETE. 또한 THP1 세포 라인 세포에 대한 활동을 통해 염증 및 산화 스트레스 반응의 억제제로 작용할 수 있음을 시사한다(15-Hydroxicosatetraeno acid#15-oxo-ETE 참조).
ALOX15, 12-(S)-HpETE 및 12(S)-HETE의 마이너 제품은 광범위한 활동을 가지고 있다.One or both of these compounds stimulates cells by binding with and activating two G protein-coupled receptors, GPR31 and the Leukotriene B4 receptor 2; 12S-HETE also acts as a receptor antagonist by binding to but not stimulating the Thromboxane receptor thereby inhibiting the actions of Thromboxane A2 and Prostaglandin H2 (see 12-Hydroxyeicosate사다리노산#수용체 대상 및 작용 메커니즘).적어도 이러한 수용체 주도 작용의 부분적인 결과로서, 두 가지 ALOX15 제품 중 하나 또는 둘 다 동물 모델에서 친인플레이션, 당뇨병 유발 및 혈관확장 활동, 배양된 인간 암세포에 대한 암 촉진 활동 및 기타 활동(12-Hydroxyeosatraenoic acid# 참조)을 나타낸다.활동 및 가능한 임상적 중요성).또한 두 제품은 다음을 포함한 다양한 생체활성 제품에 추가로 대사된다.
- 허산실린 A3 및 허산실린 B3와 각각의 3-하이드록실 대사물인 트리오실린 A3 및 트리오실린 B3와 함께.이들 대사물은 항염증 활성, 혈관확장 활동, 통증 인식 촉진, 세포의 산화 스트레스 역진, 동물 모델 시스템에서 인슐린 분비를 촉진하는 것으로 보고되었다(허바실린 참조).
- 12-Oxo-ETE는 12S-HETE와 함께 로이코트리엔 B4 수용체 2(BLT2)를 활성화하지만, 그것의 로이코트리엔 B4 수용체 1(BLT1)은 활성화하지 않는다.이를 통해 12-oxo-ETE가 BLT2가 조절하는 친염증 및 기타 활동에 기여할 수 있다(12-HETE#인플레이션 및 염증성 질환과 Rigeotrien B4 수용체 2 참조).[15]
도코사헥사에노산
Human ALOX15 metabolizes docosahexaenoic acid (DHA) to 17S-Hydroperoxy-4Z,7Z,10Z,13Z,15E,19Z-docosahexaenoic acid (17S-HpDHA) and 17S-hydroxy-4Z,7Z,10Z,13Z,15E,19Z-docosahexaenoic acid (17S-HDHA).[16]이러한 제품 중 하나 또는 두 가지 모두 인간의 가슴과 전립선 세포 라인을 자극하여 배양 증식을 촉진하며, 17S-HDHA는 강력한 전문 프로브롤링 중재자 활동을 보유하고 있다(전문 프로브롤링 중재자 참조).DHA에서 파생된 Resolvins).[17][18][19][20]이들 제품 중 하나 또는 둘 다 다음과 같이 효소화 될 수 있다.
- Resolvin Ds(RvDs), 즉 RvD-1, RvD2, RvD3, RvD4, RvD5 및 RvD6(Rvolvin 및 전문 프로리졸빙 중재자 참조)DHA에서 유래된 Resolvins) 및 보호 대상 Ds(PD), 즉 PD1, PDX, 20-hydroxy-PD1, 17-epi-PD1, 10-epi-PD1(신경보호제 D1 및 전문 프로리졸브 매개자 참조) 및 보호 대상 Ds(PDs)DHA에서 유래한 프로텍터/뉴로프 프로텍틴).이 제품들은 대사물의 전문 프로리졸브 매개체 등급의 구성원이며 광범위한 활동 범위를 가지고 있다.
에이코사펜타에노산
Human ALOX15 metabolizes eicosapentaenoic acid to 15S-hydroperoxy-5Z,8Z,11Z,13E,17E-eicosapentaenoic acid (15S-HpEPA) and 15S-hydroxy-5Z,8Z,11Z,13E,17E-eicosapentaenoic acid (15S-HEPA); 15S-HEPA inhibits ALOX5-dependent production of the pro-inflammatory mediator, LTB4, in cells, and may thereby serve an anti-inflammatory function.[21]이러한 제품은 다음과 같이 추가로 대사될 수 있다.
n-3 도코사이에노산
인간 세포와 생쥐 조직은 전문 프로레솔빈 매개체로 분류된 일련의 제품에 n-3 도코사펜타에노산(즉, 7Z, 10Z, 13Z, 16Z, 19Z-도코사펜타에노산, Clupanodonic acid 참조)을 대사한다.D를 해결하기 위한 도코사헥사에노산 대사와 유사하게, 인간의 ALOX15 가능성이 가장 높은 15리포섹제나제가 이러한 대사에 기여하는 것으로 추정된다.이러한 제품들은 n-3 Resolven D(RvDn-3's)라고 불리며 다음과 같다.
리놀레산
Human 15-LOX-1 prefers linoleic acid over arachidonic acid as its primary substrate, oxygenating it at carbon 13 to form 13(S)-hydroperoxy-9Z,11E-octadecaenoic acid (13-HpODE or 13(S)-HpODE) which may then be reduce to the corresponding hydroxy derivative, 13(S)-HODE or 13-HODE (see 13-Hydroxyoctadecadienoic acid).In addition to 13(S)-HpODE, non-human 15-LOX1 orthologs such as mouse 12/15-LOX and soybean 15-LOX metabolize linoleic acid to 9-hydroperoxy-10E, 12Z-octadecaenoic acid (9-HpODE or 9(S)-HpODE), which is rapidly converted to 9(S)-HODE (9-HODE) (see 9-Hydroxyoctadecadienoic acid)).[22][23]13(S)-HODE는 Peroxisome 증식기 활성 수용체와 TRPV1 수용체와 인간 GPR132 수용체를 통해 작용하여 단세포 성숙, 지질대사, 뉴런 활성화와 관련된 다양한 반응을 자극한다(13-Hydroxyoxyoxidecadienoic acid# 참조).#13-HODE); 9(S)-HODE는 산화적 스트레스를 수반하는 질병의 표식이며, 통증 인식과 아테롬성 경화증에도 기여할 수 있다(9-Hydroxyctadecadienoic acid##9-HOD의 생물학적 및 임상적 관련성 참조).The two HODEs can be further metabolized to their ketones, 13-oxo-9Z,11E-octadecaenoic acid and 9-oxo-10E, 12Z-octadecaenoic acid; these ketones have been implicated as biomarkers for and possible contributors to the inflammatory component of atherosclerosis, Alzheimer's disease, Steatohepatitis, and other pathological conditions.[24]
디호모시리놀렌산
Human neutrophils, presumably using their ALOX 15, metabolize Dihomo-γ-linolenic acid (8Z,11Z,14Z-eicosatrienoic acid) to 15S-hydroperoxy-8Z,11Z,13E-eicosatrienoic acid and 15S-hydroxy-8Z,11Z,13E-eicosatrienoic acid (15S-HETrE). 15S-HETrE possesses anti-inflammatory activity.[21][25]
유전자 조작 연구
12/15-Lipoxygenase 유전자(Alox15)가 결핍된 생쥐는 각막 손상, 기도 염증, 복막염의 실험 모델에서 병리적으로 강화된 염증 반응의 다양한 측면과 함께 염증 반응이 장기화된다.이 쥐들은 또한 아테롬성 동맥경화증의 진행속도가 빨라진 반면 12/15-리포스겐화효소를 과다하게 누르기 위해 만들어진 쥐들은 아테롬성 동맥경화증의 발생속도가 지연되는 것을 보여준다.알록스15 과다압박토끼는 치주염 모델에서 조직파괴 감소와 뼈 손실을 보였다.마지막으로, 제어 생쥐는 12/15 리포섹스 결핍 생쥐는 아니지만 자궁내막증 모델에서 병변의 수를 줄임으로써 아이코스펜타에노산 투여에 반응했다.[26]이러한 연구는 염증 억제가 설치류에서 생성되는 12/15 리포록시제네아제의 주요 기능이며, 설치류 12/15 리포록시제네아제는 PUFA 대사물 프로파일에서 생성되는 인간 ALOX15와 다르지만(예: 조직 분포) 다른 파라미터의 주요 기능임을 나타낸다.이러한 유전자 연구는 인간 ALOX15와 그것이 생산하는 전문 프로레졸링 매개체가 인간에게 유사한 주요 항염증 기능을 할 수 있도록 한다.
임상적 유의성
염증성 질환
AA 동물 모델에 대한 많은 연구가 증가하고 있는 가운데 15-LOX-1과 이의 리판신, 분해능 및 보호 대사물(전문 프로리졸링 매개체 참조)이 치주염, 과립염, 패혈증, 기타 병원체 유발 염증 반응을 포함한 다양한 염증성 질환을 억제, 제한 및 해결할 수 있는 것으로 나타났다. 습진, 관절염,천식, 낭포성 섬유증, 아테롬성 동맥경화증, 지방 조직 염증, 당뇨병 및 대사 증후군과 관련된 비만에서 발생하는 인슐린 저항성, 알츠하이머병에서 발생한다.[27][28][29][30][31]이러한 연구결과들이 아직 인간의 질병으로 전이되는 것으로 밝혀진 것은 아니지만, 자연적인 아날로그와는 달리 대사불활성화에 비교적 강한 1, 2세대 합성보철소와 리박신은 동물모델에서 염증억제제로 만들어 실험하고 있다.[32]이러한 합성 아날로그는 인용된 인간의 염증성 질환을 치료하는데 임상적으로 유용한 것으로 판명될 수 있다.
By metabolizing the ω-3 polyunsaturated fatty acids, eicosapentaenoic acid and docosahexaenoic acid, into 17-HpDHA, 17-HDHA, and the resolvins and protectins, 15-LOX-1's metabolic action is thought to be one mechanism by which dietary ω-3 polyunsaturated fatty acids, particularly fish oil, act to ameliorate inflammation, inflammation-related diseases, 그리고 특정 암.[11][27]
천식
15-LOX-1과 5-oxo-15-hydroxy-ETE 및 eoxin 대사물이 인간 알레르겐 유도 천식, 아스피린 유도 천식 및 기타 알레르기 질환에 대한 향후 연구 및 치료에 대한 잠재적 기여자로 제안되어 왔다.[33][34]
암
대장암, 유방암, 신장암의 경우, 15-LOX-1 수준은 암의 정상 조직과 비교하여 낮거나 없거나 암이 진행됨에 따라 급격히 감소한다.[10][27][35]쥐의[36] 대장암에 대한 15-LOX-1 트랜스젠 연구는 이러한 결과를 시사하지만 15-LOX-1이 종양 억제기라는 것을[37] 증명하지는 못한다.
Ω-3 폴리불포화지방산, 에이코사펜타에노산, 도코사헥사에노산을 리판신과 리졸빈으로 대사시킴으로써 15-LOX-1은 식이 요법 Ω-3 폴리불포화지방산, 특히 어유 등이 특정 암의 발병률 및/또는 진행을 감소시키는 작용을 하는 하나의 메커니즘으로 생각된다.[27]Indeed, the ability of docosahexaenoic acid to inhibit the growth of cultured human prostate cancer cells is totally dependent upon the expression of 15-LOX-1 by these cells and appears due to this enzyme's production of docosahexaenoic acid metabolites such as 17(S)-HpETE, 17(S)-HETE, and/or and, possibly, an isomer of protectin DX (10S, 17S-dih이드록시-4Z,[11][16] 7Z, 11E, 13Z, 15E, 19Z-도코사헥사에노산)
Kelavkar et.al have shown that aberrant overexpression of 15-LO-1 occurs in human PCa, particularly high-grade PCa, and in high-grade prostatic intraepithelial neoplasia (HGPIN), and that the murine orthologue is increased in SV40-based genetically engineered mouse (GEM) models of PCa, such as LADY and TRansgenic Adenocarcinoma of Mouse Prostate.마우스 전립선에 h15-LO-1(인간 PCa와 HGPIN에서 과도하게 압축된 유전자)을 과대압하는 것은 상피확산과 mPIN 발달을 촉진하기에 충분하다.이러한 결과는 15-LO-1이 전립선 종양 시작에 대한 역할을 하고 식이 요법이나 기타 예방 전략의 초기 목표로서 역할을 하는 것을 뒷받침한다.또한 FLiMP 마우스 모델은 PCa 진행에 필요한 분자 변경의 조합을 추가로 정의하기 위해 다른 GEM 모델과 교차할 때 유용해야 한다.[38]
메모들
이 글의 2015년 버전은 이중 출판 모델에 따라 외부 전문가에 의해 갱신되었다.해당 학술적 동료 검토 기사는 진에 게재되었으며, 다음과 같이 인용할 수 있다. Igor Ivanov; Hartmut Kuhn; Dagmar Heydeck (26 July 2015). "Structural and functional biology of arachidonic acid 15-lipoxygenase-1 (ALOX15)". Gene. Gene Wiki Review Series. 573 (1): 1–32. doi:10.1016/J.GENE.2015.07.073. ISSN 0378-1119. PMC 6728142. PMID 26216303. Wikidata Q21710694. |
참고 항목
참조
- ^ a b c GRCh38: 앙상블 릴리스 89: ENSG00000161905 - 앙상블, 2017년 5월
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000018924 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b Funk CD, Funk LB, FitzGerald GA, Samuelsson B (May 1992). "Characterization of human 12-lipoxygenase genes". Proceedings of the National Academy of Sciences of the United States of America. 89 (9): 3962–6. Bibcode:1992PNAS...89.3962F. doi:10.1073/pnas.89.9.3962. PMC 525611. PMID 1570320.
- ^ a b c d e f g h Ivanov I, Kuhn H, Heydeck D (November 2015). "Structural and functional biology of arachidonic acid 15-lipoxygenase-1 (ALOX15)". Gene. 573 (1): 1–32. doi:10.1016/j.gene.2015.07.073. PMC 6728142. PMID 26216303.
- ^ Brash AR, Boeglin WE, Chang MS (June 1997). "Discovery of a second 15S-lipoxygenase in humans". Proceedings of the National Academy of Sciences of the United States of America. 94 (12): 6148–52. Bibcode:1997PNAS...94.6148B. doi:10.1073/pnas.94.12.6148. PMC 21017. PMID 9177185.
- ^ Claesson HE (September 2009). "On the biosynthesis and biological role of eoxins and 15-lipoxygenase-1 in airway inflammation and Hodgkin lymphoma". Prostaglandins & Other Lipid Mediators. 89 (3–4): 120–5. doi:10.1016/j.prostaglandins.2008.12.003. PMID 19130894.
- ^ Jiang WG, Watkins G, Douglas-Jones A, Mansel RE (April 2006). "Reduction of isoforms of 15-lipoxygenase (15-LOX)-1 and 15-LOX-2 in human breast cancer". Prostaglandins, Leukotrienes, and Essential Fatty Acids. 74 (4): 235–45. doi:10.1016/j.plefa.2006.01.009. PMID 16556493.
- ^ a b Shureiqi I, Wu Y, Chen D, Yang XL, Guan B, Morris JS, Yang P, Newman RA, Broaddus R, Hamilton SR, Lynch P, Levin B, Fischer SM, Lippman SM (December 2005). "The critical role of 15-lipoxygenase-1 in colorectal epithelial cell terminal differentiation and tumorigenesis". Cancer Research. 65 (24): 11486–92. doi:10.1158/0008-5472.can-05-2180. PMC 1564070. PMID 16357157.
- ^ a b c Hu Y, Sun H, O'Flaherty JT, Edwards IJ (January 2013). "15-Lipoxygenase-1-mediated metabolism of docosahexaenoic acid is required for syndecan-1 signaling and apoptosis in prostate cancer cells". Carcinogenesis. 34 (1): 176–82. doi:10.1093/carcin/bgs324. PMC 3584949. PMID 23066085.
- ^ Kuhn H, Banthiya S, van Leyen K (April 2015). "Mammalian lipoxygenases and their biological relevance". Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. 1851 (4): 308–30. doi:10.1016/j.bbalip.2014.10.002. PMC 4370320. PMID 25316652.
- ^ Feltenmark S, Gautam N, Brunnström A, Griffiths W, Backman L, Edenius C, Lindbom L, Björkholm M, Claesson HE (2008). "Eoxins are proinflammatory arachidonic acid metabolites produced via the 15-lipoxygenase-1 pathway in human eosinophils and mast cells". Proceedings of the National Academy of Sciences of the United States of America. 105 (2): 680–5. Bibcode:2008PNAS..105..680F. doi:10.1073/pnas.0710127105. PMC 2206596. PMID 18184802.
- ^ Bryant RW, Bailey JM, Schewe T, Rapoport SM (June 1982). "Positional specificity of a reticulocyte lipoxygenase. Conversion of arachidonic acid to 15-S-hydroperoxy-eicosatetraenoic acid". The Journal of Biological Chemistry. 257 (11): 6050–5. doi:10.1016/S0021-9258(20)65103-1. PMID 6804460.
- ^ Yokomizo T, Kato K, Hagiya H, Izumi T, Shimizu T (April 2001). "Hydroxyeicosanoids bind to and activate the low affinity leukotriene B4 receptor, BLT2". The Journal of Biological Chemistry. 276 (15): 12454–9. doi:10.1074/jbc.M011361200. PMID 11278893.
- ^ a b O'Flaherty JT, Hu Y, Wooten RE, Horita DA, Samuel MP, Thomas MJ, Sun H, Edwards IJ (2012). "15-lipoxygenase metabolites of docosahexaenoic acid inhibit prostate cancer cell proliferation and survival". PLOS ONE. 7 (9): e45480. Bibcode:2012PLoSO...745480O. doi:10.1371/journal.pone.0045480. PMC 3447860. PMID 23029040.
- ^ Hu Y, Sun H, O'Flaherty JT, Edwards IJ (2013). "15-Lipoxygenase-1-mediated metabolism of docosahexaenoic acid is required for syndecan-1 signaling and apoptosis in prostate cancer cells". Carcinogenesis. 34 (1): 176–82. doi:10.1093/carcin/bgs324. PMC 3584949. PMID 23066085.
- ^ O'Flaherty JT, Wooten RE, Samuel MP, Thomas MJ, Levine EA, Case LD, Akman SA, Edwards IJ (2013). "Fatty acid metabolites in rapidly proliferating breast cancer". PLOS ONE. 8 (5): e63076. Bibcode:2013PLoSO...863076O. doi:10.1371/journal.pone.0063076. PMC 3642080. PMID 23658799.
- ^ Ramon S, Baker SF, Sahler JM, Kim N, Feldsott EA, Serhan CN, Martínez-Sobrido L, Topham DJ, Phipps RP (2014). "The specialized proresolving mediator 17-HDHA enhances the antibody-mediated immune response against influenza virus: a new class of adjuvant?". Journal of Immunology. 193 (12): 6031–40. doi:10.4049/jimmunol.1302795. PMC 4258475. PMID 25392529.
- ^ Kim N, Ramon S, Thatcher TH, Woeller CF, Sime PJ, Phipps RP (2016). "Specialized proresolving mediators (SPMs) inhibit human B-cell IgE production". European Journal of Immunology. 46 (1): 81–91. doi:10.1002/eji.201545673. PMC 4710564. PMID 26474728.
- ^ a b Ziboh VA, Miller CC, Cho Y (2000). "Metabolism of polyunsaturated fatty acids by skin epidermal enzymes: generation of antiinflammatory and antiproliferative metabolites". The American Journal of Clinical Nutrition. 71 (1 Suppl): 361S–6S. doi:10.1093/ajcn/71.1.361s. PMID 10617998.
- ^ Rankin SM, Parthasarathy S, Steinberg D (March 1991). "Evidence for a dominant role of lipoxygenase(s) in the oxidation of LDL by mouse peritoneal macrophages". Journal of Lipid Research. 32 (3): 449–56. doi:10.1016/S0022-2275(20)42068-1. PMID 1906087.
- ^ Veldink GA, Vliegenthart JF, Boldingh J (February 1970). "Proof of the enzymatic formation of 9-hydroperoxy-10-trans, 12-cis-octadecadienoic acid from linoleic acid by soya lipoxygenase". Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism. 202 (1): 198–9. doi:10.1016/0005-2760(70)90235-3. hdl:1874/5546. PMID 5461374.
- ^ Yuan ZX, Rapoport SI, Soldin SJ, Remaley AT, Taha AY, Kellom M, Gu J, Sampson M, Ramsden CE (2013). "Identification and profiling of targeted oxidized linoleic acid metabolites in rat plasma by quadrupole time-of-flight mass spectrometry". Biomedical Chromatography. 27 (4): 422–32. doi:10.1002/bmc.2809. PMC 3552117. PMID 23037960.
- ^ Chilton-Lopez, Surette ME, Swan DD, Fonteh AN, Johnson MM, Chilton FH (1996). "Metabolism of gammalinolenic acid in human neutrophils". Journal of Immunology. 156 (8): 2941–7. PMID 8609415.
- ^ Serhan CN, Chiang N, Dalli J (2015). "The resolution code of acute inflammation: Novel pro-resolving lipid mediators in resolution". Seminars in Immunology. 27 (3): 200–15. doi:10.1016/j.smim.2015.03.004. PMC 4515371. PMID 25857211.
- ^ a b c d López-Vicario C, Rius B, Alcaraz-Quiles J, García-Alonso V, Lopategi A, Titos E, Clària J (May 2015). "Pro-resolving mediators produced from EPA and DHA: Overview of the pathways involved and their mechanisms in metabolic syndrome and related liver diseases". European Journal of Pharmacology. 785: 133–143. doi:10.1016/j.ejphar.2015.03.092. PMID 25987424.
- ^ Romano M, Cianci E, Simiele F, Recchiuti A (August 2015). "Lipoxins and aspirin-triggered lipoxins in resolution of inflammation". European Journal of Pharmacology. 760: 49–63. doi:10.1016/j.ejphar.2015.03.083. PMID 25895638.
- ^ Cole BK, Lieb DC, Dobrian AD, Nadler JL (Jul 2013). "12- and 15-lipoxygenases in adipose tissue inflammation". Prostaglandins & Other Lipid Mediators. 104–105: 84–92. doi:10.1016/j.prostaglandins.2012.07.004. PMC 3526691. PMID 22951339.
- ^ Russell CD, Schwarze J (February 2014). "The role of pro-resolution lipid mediators in infectious disease". Immunology. 141 (2): 166–73. doi:10.1111/imm.12206. PMC 3904237. PMID 24400794.
- ^ Serhan CN, Chiang N, Dalli J (May 2015). "The resolution code of acute inflammation: Novel pro-resolving lipid mediators in resolution". Seminars in Immunology. 27 (3): 200–15. doi:10.1016/j.smim.2015.03.004. PMC 4515371. PMID 25857211.
- ^ Orr SK, Colas RA, Dalli J, Chiang N, Serhan CN (May 2015). "Proresolving actions of a new resolvin D1 analog mimetic qualifies as an immunoresolvent". American Journal of Physiology. Lung Cellular and Molecular Physiology. 308 (9): L904–11. doi:10.1152/ajplung.00370.2014. PMC 4421783. PMID 25770181.
- ^ James A, Daham K, Backman L, Brunnström A, Tingvall T, Kumlin M, Edenius C, Dahlén SE, Dahlén B, Claesson HE (2013). "The influence of aspirin on release of eoxin C4, leukotriene C4 and 15-HETE, in eosinophilic granulocytes isolated from patients with asthma". International Archives of Allergy and Immunology. 162 (2): 135–42. doi:10.1159/000351422. PMID 23921438. S2CID 29180895.
- ^ Neighbour H (2014). "Mechanisms of aspirin-intolerant asthma: identifying inflammatory pathways in the pathogenesis of asthma". International Archives of Allergy and Immunology. 163 (1): 1–2. doi:10.1159/000355949. PMID 24247362.
- ^ Gohara A, Eltaki N, Sabry D, Murtagh D, Jankun J, Selman SH, Skrzypczak-Jankun E (October 2012). "Human 5-, 12- and 15-lipoxygenase-1 coexist in kidney but show opposite trends and their balance changes in cancer". Oncology Reports. 28 (4): 1275–82. doi:10.3892/or.2012.1924. PMID 22825379.
- ^ Zuo X, Peng Z, Wu Y, Moussalli MJ, Yang XL, Wang Y, Parker-Thornburg J, Morris JS, Broaddus RR, Fischer SM, Shureiqi I (May 2012). "Effects of gut-targeted 15-LOX-1 transgene expression on colonic tumorigenesis in mice". Journal of the National Cancer Institute. 104 (9): 709–16. doi:10.1093/jnci/djs187. PMC 3341308. PMID 22472308.
- ^ Umar A (May 2012). "Is 15-LOX-1 a tumor suppressor?". Journal of the National Cancer Institute. 104 (9): 645–7. doi:10.1093/jnci/djs192. PMID 22472307.
- ^ Kelavkar UP, Parwani AV, Shappell SB, Martin WD (2006). "Conditional expression of human 15-lipoxygenase-1 in mouse prostate induces prostatic intraepithelial neoplasia: the FLiMP mouse model". Neoplasia. 8 (6): 510–22. doi:10.1593/neo.06202. PMC 1601466. PMID 16820097.
- Kelavkar UP, Badr KF (1999). "Effects of mutant p53 expression on human 15-lipoxygenase-promoter activity and murine 12/15-lipoxygenase gene expression: evidence that 15-lipoxygenase is a mutator gene". Proceedings of the National Academy of Sciences of the United States of America. 96 (8): 4378–83. Bibcode:1999PNAS...96.4378K. doi:10.1073/pnas.96.8.4378. PMC 16340. PMID 10200270.
추가 읽기
- Kelavkar UP, Badr KF (1999). "Effects of mutant p53 expression on human 15-lipoxygenase-promoter activity and murine 12/15-lipoxygenase gene expression: evidence that 15-lipoxygenase is a mutator gene". Proceedings of the National Academy of Sciences of the United States of America. 96 (8): 4378–83. Bibcode:1999PNAS...96.4378K. doi:10.1073/pnas.96.8.4378. PMC 16340. PMID 10200270.
- Kelavkar U, Glasgow W, Eling TE (June 2002). "The effect of 15-lipoxygenase-1 expression on cancer cells". Current Urology Reports. 3 (3): 207–14. doi:10.1007/s11934-002-0066-8. PMID 12084190. S2CID 21497252.
- Sigal E, Dicharry S, Highland E, Finkbeiner WE (April 1992). "Cloning of human airway 15-lipoxygenase: identity to the reticulocyte enzyme and expression in epithelium". The American Journal of Physiology. 262 (4 Pt 1): L392–8. doi:10.1152/ajplung.1992.262.4.L392. PMID 1566855.
- Izumi T, Rådmark O, Jörnvall H, Samuelsson B (December 1991). "Purification of two forms of arachidonate 15-lipoxygenase from human leukocytes". European Journal of Biochemistry. 202 (3): 1231–8. doi:10.1111/j.1432-1033.1991.tb16495.x. PMID 1662607.
- Conrad DJ, Kuhn H, Mulkins M, Highland E, Sigal E (January 1992). "Specific inflammatory cytokines regulate the expression of human monocyte 15-lipoxygenase". Proceedings of the National Academy of Sciences of the United States of America. 89 (1): 217–21. Bibcode:1992PNAS...89..217C. doi:10.1073/pnas.89.1.217. PMC 48207. PMID 1729692.
- Lei ZM, Rao CV (February 1992). "The expression of 15-lipoxygenase gene and the presence of functional enzyme in cytoplasm and nuclei of pregnancy human myometria". Endocrinology. 130 (2): 861–70. doi:10.1210/en.130.2.861. PMID 1733732.
- Izumi T, Rådmark O, Samuelsson B (1991). "Purification of 15-lipoxygenase from human leukocytes, evidence for the presence of isozymes". Advances in Prostaglandin, Thromboxane, and Leukotriene Research. 21A: 101–4. PMID 1825526.
- Sloane DL, Leung R, Craik CS, Sigal E (November 1991). "A primary determinant for lipoxygenase positional specificity". Nature. 354 (6349): 149–52. Bibcode:1991Natur.354..149S. doi:10.1038/354149a0. PMID 1944593. S2CID 4352315.
- Nadel JA, Conrad DJ, Ueki IF, Schuster A, Sigal E (April 1991). "Immunocytochemical localization of arachidonate 15-lipoxygenase in erythrocytes, leukocytes, and airway cells". The Journal of Clinical Investigation. 87 (4): 1139–45. doi:10.1172/JCI115110. PMC 295116. PMID 2010530.
- Kroschwald P, Kroschwald A, Kühn H, Ludwig P, Thiele BJ, Höhne M, Schewe T, Rapoport SM (April 1989). "Occurrence of the erythroid cell specific arachidonate 15-lipoxygenase in human reticulocytes". Biochemical and Biophysical Research Communications. 160 (2): 954–60. doi:10.1016/0006-291X(89)92528-X. PMID 2719708.
- Sigal E, Nadel JA (December 1988). "Arachidonic acid 15-lipoxygenase and airway epithelium. Biologic effects and enzyme purification". The American Review of Respiratory Disease. 138 (6 Pt 2): S35–40. doi:10.1164/ajrccm/138.6_pt_2.s35. PMID 3202520.
- Sigal E, Craik CS, Highland E, Grunberger D, Costello LL, Dixon RA, Nadel JA (December 1988). "Molecular cloning and primary structure of human 15-lipoxygenase". Biochemical and Biophysical Research Communications. 157 (2): 457–64. doi:10.1016/S0006-291X(88)80271-7. PMID 3202857.
- Sigal E, Grunberger D, Craik CS, Caughey GH, Nadel JA (April 1988). "Arachidonate 15-lipoxygenase (omega-6 lipoxygenase) from human leukocytes. Purification and structural homology to other mammalian lipoxygenases". The Journal of Biological Chemistry. 263 (11): 5328–32. doi:10.1016/S0021-9258(18)60719-7. PMID 3356688.
- Nassar GM, Morrow JD, Roberts LJ, Lakkis FG, Badr KF (November 1994). "Induction of 15-lipoxygenase by interleukin-13 in human blood monocytes". The Journal of Biological Chemistry. 269 (44): 27631–4. doi:10.1016/S0021-9258(18)47031-7. PMID 7961680.
- Kritzik MR, Ziober AF, Dicharry S, Conrad DJ, Sigal E (June 1997). "Characterization and sequence of an additional 15-lipoxygenase transcript and of the human gene". Biochimica et Biophysica Acta (BBA) - Gene Structure and Expression. 1352 (3): 267–81. doi:10.1016/s0167-4781(97)00005-5. PMID 9224951.
- Brinckmann R, Schnurr K, Heydeck D, Rosenbach T, Kolde G, Kühn H (January 1998). "Membrane translocation of 15-lipoxygenase in hematopoietic cells is calcium-dependent and activates the oxygenase activity of the enzyme". Blood. 91 (1): 64–74. doi:10.1182/blood.V91.1.64. PMID 9414270.
- Kelavkar U, Wang S, Montero A, Murtagh J, Shah K, Badr K (July 1998). "Human 15-lipoxygenase gene promoter: analysis and identification of DNA binding sites for IL-13-induced regulatory factors in monocytes". Molecular Biology Reports. 25 (3): 173–82. doi:10.1023/A:1006813009006. PMID 9700053. S2CID 13147031.
- Roy B, Cathcart MK (November 1998). "Induction of 15-lipoxygenase expression by IL-13 requires tyrosine phosphorylation of Jak2 and Tyk2 in human monocytes". The Journal of Biological Chemistry. 273 (48): 32023–9. doi:10.1074/jbc.273.48.32023. PMID 9822675.
- Kratky D, Lass A, Abuja PM, Esterbauer H, Kühn H (January 1999). "A sensitive chemiluminescence method to measure the lipoxygenase catalyzed oxygenation of complex substrates". Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. 1437 (1): 13–22. doi:10.1016/s0005-2760(98)00176-3. PMID 9931410.
- Kelavkar UP, Badr KF (April 1999). "Effects of mutant p53 expression on human 15-lipoxygenase-promoter activity and murine 12/15-lipoxygenase gene expression: evidence that 15-lipoxygenase is a mutator gene". Proceedings of the National Academy of Sciences of the United States of America. 96 (8): 4378–83. Bibcode:1999PNAS...96.4378K. doi:10.1073/pnas.96.8.4378. PMC 16340. PMID 10200270.
외부 링크
- UCSC 게놈 브라우저의 인간 ALOX15 게놈 위치 및 ALOX15 유전자 세부 정보 페이지.